水分活度概念自从1957年被提出之后,在食品保藏方面得到很多应用[1]。水分活度定义为物质中水分含量的活性部分或者说自由水。水分活度被认为是产品稳定性的一个重要指标[2]。通过适当的方法(包括干燥、大量的糖或者盐与水的化学结合)控制水分活度在低水平达到产品长期保存,这种方法在民间被人类长期使用。从微生物的角度来说,控制水分活度可以抑制微生物的生长。这就能解释蜂蜜、蜜饯、咸菜为什么不容易长菌。而且控制水分活度不止能控制微生物的生长,产品的化学和物理性能也得到了很好的保存。
药品从微生物风险控制的角度可以分为无菌药品和非无菌药品。非无菌药品基于产品属性、给药途径及目标人群,最终产品要求达到相应的微生物限度标准。其中非无菌含药材原粉的固体口服给药制剂因为含有药材原粉,微生物限度标准最宽。在生产过程中,原料水、药品原料、生产设备、操作人员和生产环境都会引入微生物污染。采用过分的微生物控制将增加复杂性或成本,合理的非无菌药品的微生物负载控制是保证产品质量的关键因素[3]。低水活度、高或低pH的药品原料、本身有抗菌性或含有防腐剂的药品原料微生物增殖的风险较低。控制水分活度可以提高药品的稳定性。
1 水分含量与干燥失重结果并不能代表水分活度药品中的水分含量一直是药品质量控制的重要部分。由于剂型的限制,在《中国药典》2015版中,只有表 1中列出剂型通过水分测定(通则0832)或干燥失重(通则0831)来检测药品中的水分含量[4]。
|
|
表 1 不同剂型药品的水分或干燥失重标准 |
水分活度(aw)是材料中水的蒸汽压(P)与在相同温度下纯水蒸汽压(P0)的比值,公式所示aw =P/ P0=ERH(%)/100。当蒸汽和温度达到平衡状态时,水分活度也等于在一个密封的测量条件下材料周围空气的相对平衡湿度(ERH)[2]。水分活度从完全干燥的0.0 aw到纯水的1.0 aw。为了好理解,水分活度被描述为自由水,而相应的结合水就被排除在水分活度之外。但是,随着理解的加深,产品中并不存在完全自由的水,只是结合的紧密度大小而已。从这种意义来说,水分活度描述为产品中水结合紧密度的测量更为准确。
药品检测方法中水分和干燥失重反映的并不全是自由水,并不是水分活度的体现,但是其中也包括了水分活度。然而,拿以上水分含量测定中相差最大的15%和8%的药品来说,水分8%的药品未必比水分15%的药品稳定性更好。因为,水分的多少不反映水分活度的高低。有研究表明,阿莫西林克拉维酸钾颗粒容易吸潮降解,相差不大的初始含水量的2批样品由于初始水分活度的差别表现出稳定性的较大差别[5]。
2 微生物生长的水分活度要求表 2中列出了常见微生物增殖所需最低的水分活度[6-9]。大多数细菌需要在水分活度0.90以上增殖,除了需氧的金黄色葡萄球菌。大多数的霉菌和酵母在水分活度0.77以上增殖。微生物增殖的极端水分活度在0.61。在药品质量控制中,控制水分活度可以恶化微生物的生长环境、抑制微生物的繁殖,但是必须指出其中的微生物依然存在。
|
|
表 2 不同微生物的生长最低水分活度要求 |
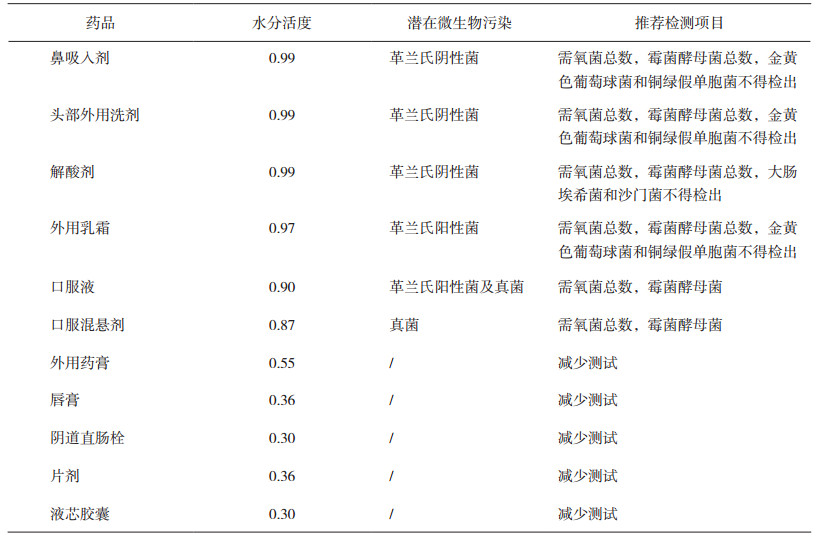
从终产品风险控制的角度来说,如果产品的水分活度在0.90以上,微生物污染的风险就有细菌、霉菌和酵母。如果在0.77~0.90之间,霉菌和酵母污染的几率更大些,但是要关注金黄色葡萄球菌的存在。如果在0.77以下甚至0.6以下,微生物污染的风险就相应变小,完全可以减少常规测试的项目。基于这种原则,在美国药典中,USP1112就是水分活度在非无菌产品监测上的应用[6],如表 3所示。
|
|
表 3 不同药品的水分活度应用 |
以口服液为例,一般的水分活度在0.90(不同厂家的生产工艺和配方有不同,具体的水分活度应该根据自己产品的测试值为准)。根据表 3,最大的潜在微生物污染是革兰氏阳性菌和真菌,推荐测试项目是需氧菌总数和霉菌酵母菌总数。这是水分活度在测试策略上的贡献。如果能通过产品工艺的优化和产品配方的变更实现水分活度降低,这是最好的情况。如果由于产品剂型限制,无法将最终产品的水分活度控制下去,从过程控制的角度来说,可以控制原材料的水分活度和监测中间产品的水分活度来控制微生物污染。
3 降低水分活度的多种方式 3.1 干燥除水从几种剂型看,颗粒剂和片剂的水分活度就比较低。例如维生素C片剂的水分活度在0.33,复合维生素片的水分活度在0.3左右。从生产过程来说,只要不影响有效成分的药效,烘干除水或者冷冻干燥除水都是可以考虑的。例如抗真菌药膏的水分活度在0.95,干燥除水做成抗真菌粉剂后水分活度为0.537,达到了0.6以下大多数微生物无法增殖的水平。培养微生物用的脱水培养基也是这个原理,通过干燥后密封包装来达到抑制微生物增殖的目的,有效期可以达到3年之久。当然,如果打开后,随着密封条件的破坏,水分活度增加,同时接触到空气中的外来微生物,污染风险会大大增加。
3.2 改变剂型如果不能进行简单的干燥除水,比如其他涉及到液体的剂型,选择之一就是改变剂型,当然这部分提到的剂型改变并不是由于干燥除水后引起的剂型改变。例如,一般的日用品肥皂的水分活度是0.740~0.757,做成发泡型肥皂后,水分活度是0.537,达到了0.6以下,即大多数微生物无法增殖的水平。
一般认为,口服液体制剂的水分活度因为本身成分中有水的存在很难有所作为。但是随着一些新剂型的出现,水分活度得到了控制。如止咳糖浆的水分活度在0.912~0.965,但是做成液心止咳糖后,水分活度也做到了0.6以下。还可以做成液芯胶囊,水分活度可以降到0.4。液芯胶囊是指将一定量的液体药物直接包封,或将固体药物溶解或分散在适宜的赋形剂中制成溶液、混悬液、乳液或半固体,密封于球形或椭圆形的软质囊材中的胶囊剂。
当两种成分混合时,水分会从水分活度高的成分向水分活度低的成分迁移。有包衣的片剂或者液芯胶囊在保存一段时间后性状就会发生一些变化,直接影响有效期[10]。可以在明胶胶囊中加入一定量的水活性调节剂(包括羧甲基纤维素钠、钙、交联羧甲基纤维素钠、部分糊化淀粉和聚乙烯基吡咯烷酮),调整胶囊内部水分活度,减少水分迁移,不影响明胶涂层提高稳定性[11]。
3.3 添加组分从提高稳定性的角度考虑,添加组分必须关注对水分活度的影响。以头孢克洛干混悬剂为例,通过对相同原料药来源的不同企业产品进行比较,发现辅料的种类和含量不同与水分活度的变化呈正相关,水分活度增长低的样品稳定性高[12]。在食品领域,无机盐类常常作为水分活度的降低剂来提高食品的保质期。一般认为,在溶液或胶体中,无机盐类可以很有效地调节该溶液的渗透压,从而对维持微生物细胞内外渗透压平衡有着重要作用。相比较高价态盐类,低价态盐类对水分活度的影响更大些[13]。在化妆品领域,也有专利通过在化妆品中添加丙二醇、二丙二醇、丁二醇、戊二醇、己二醇、甘油、双甘油、山梨(糖)醇、甜菜碱、葡萄糖、海藻糖、蔗糖、聚乙二醇-8、聚乙二醇-32、甲基葡糖醇聚醚-10、甲基葡糖醇聚醚-20、甘油聚醚-26、泊洛沙姆184的一种或他们的混合物或它们的同分异构体来控制水分活度,同时添加pH缓冲剂控制pH达到产品三年的保质期[14]。在食品和化妆品领域应用的这些水分活度降低剂也很有可能在药品中相对应的口服类剂型和外用类剂型中得到应用。
3.4 降低温度由于蒸气压和平衡相对湿度都是温度的函数,所以水分活度也是温度的函数。水分活度与温度的函数可用克劳修斯-克拉伯龙方程表示:lnaw =-△H/RT+c,T为绝对温度,R为气体常数[15]。一般认为,温度下降,水分活度下降。
4 讨论非无菌药物由于药品原料和生产加工过程没有做到无菌而一直有微生物的存在,而且有些剂型的非无菌药物就是设计成多次使用的,在使用期内也会收到微生物污染的威胁[16]。为了在整个生命周期中(生产出来至有效期结束)使药品不因微生物增殖而变质,有些药品中会添加防腐剂。同时,还有其他手段包括低pH、低氧化还原电位、尽量低的保存温度、单次剂量包装和低水分活度。其中最关键就是水分活度,其他手段如上所述与水分活度均有关系。各种微生物有最低水分活度的增殖要求,结合这些要求可以对现有剂型药品的微生物增殖风险有清晰的认识。随着质量来源于设计的思想越来越深入人心,在非无菌药品的配方开发和保质期研究引入水分活度的概念十分必要[17-18]。而且低水分活度的非无菌药品可以减少微生物检测的频率和项目,对检验成本的减少也是一大贡献。
| [1] |
SCOTT W J. Water Relations of Food Microorganisms[J]. Advances in Food Research, 1957(7): 83-127. |
| [2] |
Rockland L B, Nishi S K. Influence of Water Activity on Food Product Quality and Stability[J]. Food Technology, 1980, 34: 42-51. |
| [3] |
General Information/ < 1115 > Bio-burden Control of Nonsterile Drug Substances and Products[S]. USP38-NF33, 2015, Volume 1: 1185-1191.
|
| [4] |
中国药典[S]. 2015: 0100制剂通则3-29.
|
| [5] |
薛晶, 朱克旭, 崇小萌, 等. 水分对阿莫西林克拉维酸钾颗粒稳定性的影响[J]. 中国药学杂志, 2016, 51(3): 224-229. |
| [6] |
General Information/ < 1112 > Application of Water Activity Determination to Non-sterile Pharmaceutical Products[S]. USP38-NF33, 2015, Volume 1: 1178-1180.
|
| [7] |
Cundell T. The Role of Water Activity in the Microbial Stability of Non-sterile Drug Products[J]. European Pharmaceutical Review, 2015, 20(1): 58-63. |
| [8] |
Friedel RR, Cundell AM. The Application of Water Activity Measurement to the Microbiological Attributes Testing of Non-sterile Over-the-counter Drug Products[J]. Pharmacopeial Forum, 1998, 24: 6087-6090. |
| [9] |
Farakos S, Hicks J, Frye J, et al. Relative Survival of Four Serotypes of Salmonella Enterica in Low-water Activity Whey Protein Powder Held at 36 and 70:C at Various Water Activity Levels[J]. Journal of Food Protection, 2014, 77: 1198-2000. DOI:10.4315/0362-028X.JFP-13-327 |
| [10] |
Kolcák J, Stuchlík M, Rabisková M. Migration of Water in Soft Gelatin Capsules[J]. Ceska A Slovenska Farmacie, 2003, 52(4): 181-185. |
| [11] |
SHIONOGI & CO., LTD. Gelatin Capsule with Adjusted Water Activity: EP 0818195 A1[P]. 1998.
|
| [12] |
周晓溪, 秦爱方, 田方. 水分活度对头孢克洛干混悬剂稳定性的影响[J]. 中南药学, 2017, 15(8): 1041-1043. DOI:10.7539/j.issn.1672-2981.2017.08.005 |
| [13] |
王满生, 曾新安, 孙大文. 不同盐类对固体培养基水分活度的影响[J]. 食品与机械, 2014, 30(6): 3-6. |
| [14] |
邱玉想, 蒋丽刚. 一种抑制美白化妆品变黄的方法: 中国, CN103385806A[P]. 2013.
|
| [15] |
迟玉杰. 食品化学[M]. 北京: 化学工业出版社, 2012.
|
| [16] |
Tim S. The Importance of Water Activity for Risk Assessing Pharmaceutical Products[J]. Journal of Pharmaceutical Microbiology, 2016, 2(1): 1-2. |
| [17] |
Lawrence X. Yu. Pharmaceutical Quality by Design:Product and Process Development, Understanding and Control[J]. Pharmaceutical Research, 2008, 25(4): 781-791. DOI:10.1007/s11095-007-9511-1 |
| [18] |
Hussong D. Water Activity Applications in the Pharmaceutical Industry[M]. USA: Davis Healthcare International Publishing, LLC. River Grove, IL, 2009: 253-257.
|
 2018, Vol. 32
2018, Vol. 32