2. 中国食品药品检定研究院, 北京 102629
2. National Institutes for Food and Drug Control, Beijing 102629, China
丝素蛋白防粘连凝胶是一种丝素蛋白基生物材料。该材料具备良好的理化性质,被广泛应用于血管组织再生、粘连预防、皮肤伤口敷料、药物输送和骨组织支架等领域[1-7]。丝素蛋白是一种具备良好生物相容性的天然高分子纤维蛋白[8],含有18种氨基酸,其中甘氨酸、丙氨酸和丝氨酸含量约占87%[9]。丝素蛋白凝胶是丝素蛋白溶液在外力作用下形成由β-折叠为物理交联点的三维网状结构凝胶,其特殊的凝胶结构能用于预防粘连,且实现直接注射使用[10]。粘连是外科术后常发生情况,可导致严重的临床问题,例如硬膜和神经根周围的粘连,使硬膜囊受压,直接导致手术失败[11]。2014年,梁敏[3]通过动物实验证明了丝素蛋白凝胶具有良好的防粘连效果,后期效果理想。聚乳酸防粘连凝胶对腹部手术后预防肠粘连、产妇术后预防盆腹腔粘连均有明显作用,临床效果得到较好的验证[12-13]。将丝素蛋白防粘连凝胶应用于医疗,要充分考虑材料的生物安全性,而局部反应是评价材料生物安全性的重要指标之一。
2 实验方法本研究采用丝素蛋白防粘连凝胶进行局部反应研究,对实验动物模型、植入部位、植入时间、取材部位等实验条件及实验过程进行详细的描述。实验方法参考国家标准GB/T16886.6-2015[14](医疗器械评价第6部分:植入后局部反应实验)进行生物相容性评价。
2.1 实验材料及制备实验样品:丝素蛋白防粘连凝胶(苏州丝美特生物技术有限公司)为无菌产品,室温下保存于注射器中;实验前紫外灭菌10 min,直接用于皮下植入。对照样品:聚乳酸防粘连凝胶(河北瑞诺医疗器械股份有限公司,规格2 mL/支),室温保存;实验前紫外灭菌10 min,直接用于皮下植入。实验样品与对照品均在有效期内,以保证实验结果的有效性。
2.2 实验动物新西兰家兔12只,体重2.5~2.8 kg(中国食品药品检定研究院动物繁育场提供)。
2.3 实验方法 2.3.1 皮下植入实验选用新西兰家兔12只,采用皮下植入实验,背部脊柱左侧皮下注射对照样品,右侧皮下注射实验样品,每侧皮下注射4个点,每个注射点为0.5 mL,每点间隔2 cm。同一时间点注射后,分别在1周、4周、12周、26周4个时间点两侧分别取皮下包裹注射样品的组织,左侧取材组织为对照样品组,右侧取材组织为实验样品组,每个时间点随机取3只家兔。
2.3.2 取样及切片制备植入1周时,随机取3只新西兰家兔实施二氧化碳安乐死。对其背部左右两侧实验部位创口进行肉眼观察和评价,切取包括植入材料及周围足够多的未受影响的皮下组织,每组共取10块不同部位的皮下组织。将其置10%福尔马林溶液中固定。在植入4周、12周、26周时,分别重复植入1周时的处理步骤。将固定在福尔马林溶液中的皮下组织制备石蜡组织切片并进行HE染色。
2.3.3 组织病理学半定量评价每组每个时间点选取质量合格的切片8张,每张切片随机选取10个视野观察,记录视野中材料周边细胞的种类及数量。参照GB/T16886.6-2015[14]炎性反应分级、纤维囊腔形成分级、组织学评价系统(细胞类型/反应每项得分参考“5.3组织学评价系统——细胞类型/反应”;反应每项得分参考“5.4组织学评价系统——反应”)等标准半定量评价系统进行打分,根据实验样品组织学评分与对照样品组织学评分的差值进行判定。差值在0.0~2.9判定为无刺激;差值在3.0~8.9判定为轻微刺激;差值在9.0~15.0判定为中度刺激;差值>15判定为重度刺激;负差值记录为零进行判定。
3 结果 3.1 肉眼观察植入后3天,观察实验样品及对照样品植入部位皮肤情况,未见皮肤红肿、出血等现象。1周至26周每个实验取材时间点观察实验样品、对照样品植入部位皮肤创口部位均无红肿、感染或出血等现象,且创口均已愈合。取材时,植入物周围组织质地颜色均正常。26周时,实验样品与对照样品植入部位均肉眼观察不到植入样品残留。
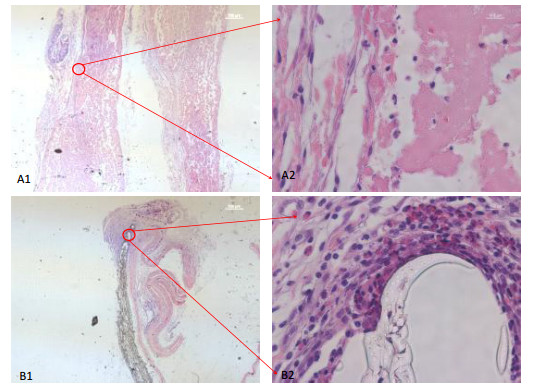
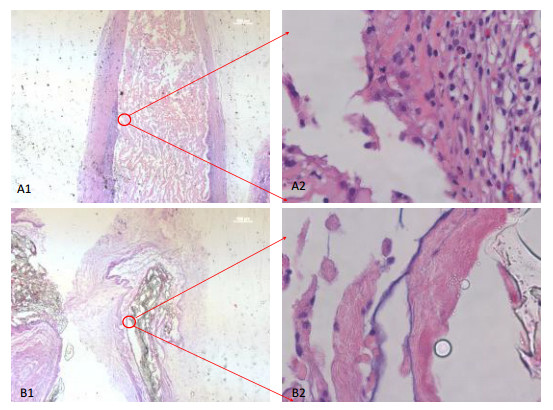
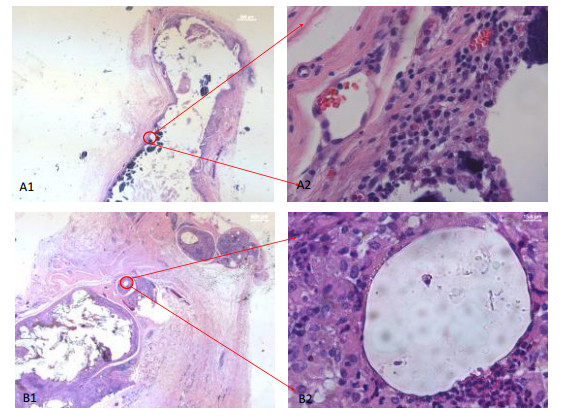
3.2 组织病理学观察 3.2.1 观察结果植入材料在不同时间点存在变化。实验样品组:1周时,丝素蛋白防粘连凝胶植入部位可见粉红团状埋植物,与周围组织存在明显界限,见图 1-A;4周时,可见粉红色埋植物,团块变细变小,见图 2-A;12周时,植入部位有深紫色样品残留,残留物明显减少,吞噬细胞增多,纤维化边缘变薄,见图 3-A;26周时,植入部位仅见皮下疏松结缔组织,未见植入物残余,见图 4-A。对照样品组:1周时,聚乳酸防粘连凝胶植入部位可见透明状物,纤维成网格状长入埋植物中间,成纤维细胞较多,见图 1-B;4周时,可见不规则形状无色透明物,纤维囊外层加厚,巨噬细胞由纤维囊外进入囊内,被纤维囊包裹,大小不等的球面物边缘有淋巴细胞附着,见图 2-B;12周时,植入物部分可着色,材料部分降解,纤维化厚度大于实验样品组,可见植入物成大小不等的圆球状,周围有多核细胞、吞噬细胞、淋巴细胞、成纤维细胞、毛细血管围绕,见图 3-B;26周时,除皮下疏松结缔组织外,有一块切片尚可见小团残余植入物包囊,见图 4-B。
|
A1.实验样品组(12.5×);A2.实验样品组(400×);B1.对照样品组(12.5×);B2.对照样品组(400×)。 图 1 植入1周后皮下组织病理切片组织学观察结果 |
|
A1.实验样品组(12.5×);A2.实验样品组(400×);B1.对照样品组(12.5×);B2.对照样品组(400×)。 图 2 植入4周后皮下组织病理切片组织学观察结果 |
|
A1.实验样品组(12.5×);A2.实验样品组(400×);B1.对照样品组(12.5×);B2.对照样品组(400×)。 图 3 植入12周后皮下组织病理切片组织学观察结果 |
|
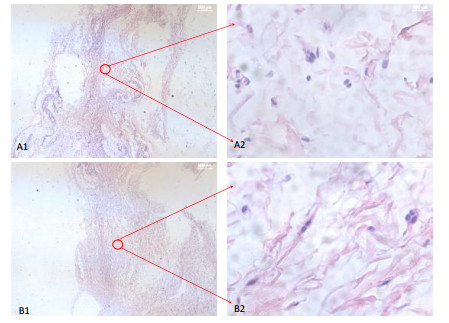
A1.实验样品组(12.5×);A2.实验样品组(400×);B1.对照样品组(12.5×);B2.对照样品组(400×)。 图 4 植入26周后皮下组织病理切片组织学观察结果 |
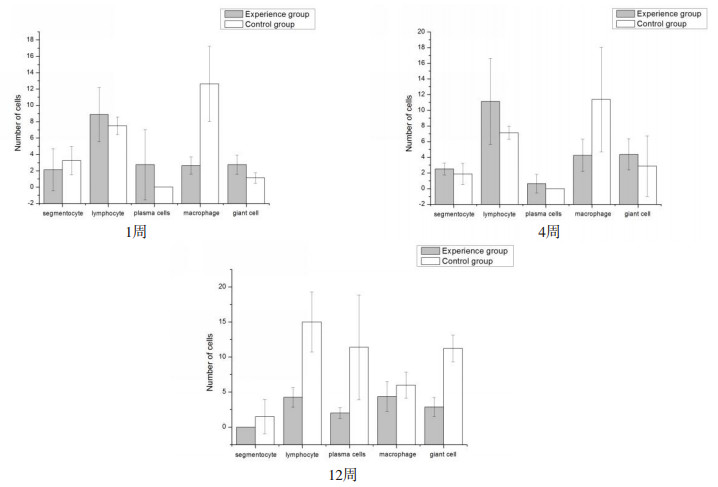
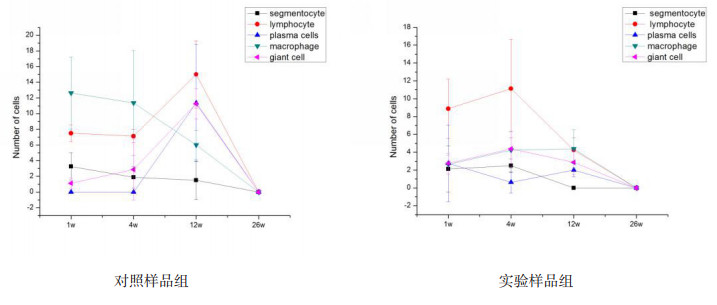
分析各时间点组织病理切片情况,实验样品组与对照样品组炎性细胞种类均可见多形核白细胞、淋巴细胞、浆细胞、巨噬细胞及巨细胞。与对照样品组比较,1周、4周、12周,实验样品组巨噬细胞数量均显著低于对照样品组。12周时,实验样品组各炎性细胞数量均低于对照样品组,见图 5。对照样品组巨噬细胞和多形核白细胞在1周时最多,4个取材时间点数量呈逐渐下降趋势;而淋巴细胞、巨细胞、浆细胞则在12周时超过1周数量,达到最大值。实验样品组淋巴细胞、巨细胞、巨噬细胞、多形核白细胞4周时数量超过1周,达到最大值。实验样品组和对照样品组的共同点是在26周时,上述各种细胞的数量均降为0,见图 6。
|
图 5 对照样品组与实验样品组细胞数量情况 |
|
图 6 各取材点细胞数量变化情况 |
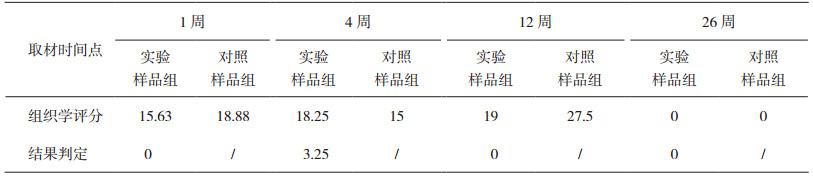
组织病理学半定量评价得分见表 1,1周、12周、26周评分结果均为0,判定为无刺激;4周时评分结果为3.25,判定为轻微刺激。
|
|
表 1 组织病理学观察结果及判定 |
本研究中的丝素蛋白防粘连凝胶是目前国内首例用丝素基生物材料作为防粘连材料的医疗器械。该材料是理想的防粘连凝胶,具备良好的组织生物相容性,方便使用,可以成膜依附在组织或创口表面[15]。本实验将材料植入家兔皮下研究局部反应得出组织病理学和细胞分类结果,现对结果分析如下。
4.1 组织病理学及半定量评价结果分析对照样品采用上市产品聚乳酸钠防粘连凝胶,已被临床研究证明其局部炎性反应在安全范围内。本研究中发现对照样品炎性反应在12周时为高峰期,26周炎性反应几乎不可见。半定量分析结果显示,实验样品与对照样品比较,4周时存在轻微刺激,其余时间均可判定为无刺激。分析1周、4周时实验样品植入部位的炎性反应,丝素蛋白主要来源于家蚕,对于新西兰家兔属于外源物,必然会引起炎症反应,与对照样品不同,实验样品的炎性反应高峰期在4周,即植入初期丝素蛋白凝胶引起的局部组织反应较明显。26周时,对照品组与实验样品组的植入物均基本降解完成,且炎性细胞数量均为零。4个时间点的局部病理结果显示,丝素蛋白防粘连凝胶具有良好的局部生物相容性。
4.2 组织细胞分类及统计结果分析通过对对照样品组与实验样品组细胞类型及数量统计分析发现,对照样品组与实验样品组主要细胞类型相同,均为多形核白细胞、淋巴细胞、浆细胞、巨噬细胞、巨细胞。细胞数量变化趋势存在明显差异。在1周时,对照样品组巨噬细胞高于实验样品组,巨噬细胞的趋化性可使响应因子向异物移动,启动免疫反应。直至12周,对照样品组各类细胞数量均已高于实验样品组,对照样品组出现炎性反应高峰期。对照样品组各阶段细胞类型以巨噬细胞为主,实验样品组以淋巴细胞为主。在GB/T16886.20-2015《医疗器械生物学评价第20部分医疗器械免疫毒理学试验原则和方法》明确提出,材料/组织界面反应以巨噬细胞为主涉及到异物反应,而以淋巴细胞为主涉及到与免疫毒性相关的慢性炎症反应。虽然两种材料在26周时都完全降解,根据主要细胞类型及变化趋势可判断对照样品组与实验样品组局部反应过程不同,提示两种材料在体内降解反应的机制可能不同。这种分类量化的方法能够从细胞水平对更加全面地评价机体局部组织对材料产生的反应,为进一步探讨可降解防粘连材料体内降解过程及机制提供支持。
5 结语本研究通过分类量化的方法比较丝素蛋白基质材料与聚乳酸防粘连材料植入后材料降解的过程及引起炎症细胞的变化,从细胞水平评价机体局部组织对材料产生的反应,对评价丝素蛋白基质凝胶材料的防粘连效果、稳定性和产品安全性都有重要的意义,为进一步探讨可降解防粘连材料体内降解过程及机制提供支持。
| [1] |
王琳婷, 朱良均, 闵思佳, 等. 丝素蛋白在生物医学领域的应用研究[J]. 北方蚕业, 2009, 30(3): 1-3. DOI:10.3969/j.issn.1673-9922.2009.03.001 |
| [2] |
Nakazawa Y, Sato M, Takahashi R, et al. Development of Small-Diameter Vascular Grafts Based on Silk Fibroin Fibers from Bombyx Mori for Vascular Regeneration[J]. Journal of Biomaterials Science, Polymer Edition, 2011, 22(1-3): 195-206. DOI:10.1163/092050609X12586381656530 |
| [3] |
梁敏.丝素蛋白凝胶预防硬膜外粘连的实验研究[D].哈尔滨医科大学, 2014. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2670343
|
| [4] |
Roh D H, Kang S Y, Kim J Y, et al. Wound Healing Effect of Silk Fibroin/Alginate-blended Sponge in Full Thickness Skin Defect of Rat[J]. Journal of Materials Science Materials in Medicine, 2006, 17(6): 547-552. DOI:10.1007/s10856-006-8938-y |
| [5] |
Zhao Z, Li Y, Xie M B. Silk Fibroin-based Nanoparticles for Drug Delivery[J]. International Journal of Molecular Sciences, 2015, 16(3): 4880-4903. DOI:10.3390/ijms16034880 |
| [6] |
Mandal B B, Grinberg A, Gil E S, et al. High-strength Silk Protein Scaffolds for Bone Repair[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(20): 7699-7704. DOI:10.1073/pnas.1119474109 |
| [7] |
Zhang H, Li L, Dai F, et al. Preparation and Characterization of Silk Fibroin as a Biomaterial with Potential for Drug Delivery[J]. Journal of Translational Medicine, 2012, 10(1): 117. DOI:10.1186/1479-5876-10-117 |
| [8] |
Rnjak-Kovacina J, Desrochers T M, Burke K A, et al. The Effect of Sterilization on Silk Fibroin Biomaterial Properties[J]. Macromolecular Bioscience, 2015, 15(6): 861-874. DOI:10.1002/mabi.v15.6 |
| [9] |
Zhu B, Wang H, Leow WR, et al. Silk Fibroin for Flexible Electronic Devices[J]. Adv Mater, 2016, 28(22): 4250-4265. DOI:10.1002/adma.v28.22 |
| [10] |
潘岳林, 杨明英, 朱良均.丝素在药物缓释领域中的研究进展[C].中国蚕学会青年学术研讨会, 2014.
|
| [11] |
戎利民, 蔡道章. 纤维蛋白凝胶预防硬膜外粘连的实验研究[J]. 中国现代医学杂志, 2001, 11(10): 13-14. DOI:10.3969/j.issn.1005-8982.2001.10.006 |
| [12] |
徐伟全. 聚乳酸防粘连凝胶及透明质酸钠预防术后肠粘连效果的对比分析[J]. 中国现代医生, 2013, 51(14): 71-72. |
| [13] |
谭文换. 剖宫产术应用聚乳酸防粘连凝胶的临床分析[J]. 医学理论与实践, 2017(1): 88-89. |
| [14] |
国家标准GB/T16886.6-2015《医疗器械评价第6部分: 植入后局部反应实验》[S]. 2015.
|
| [15] |
黄训亭.丝素蛋白材料的生物降解性研究[D].复旦大学, 2007. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1168650
|
 2019, Vol. 33
2019, Vol. 33