活血止痛散和活血止痛胶囊由当归、三七、乳香(制)、冰片、土鳖虫、自然铜(煅)六味药组成,具有活血散瘀、消肿止痛的作用,用于跌打损伤、淤血肿痛。活血止痛散和活血止痛胶囊现行标准收载于《中华人民共和国药典》2015年版一部[1],主要包括当归、三七、土鳖虫的显微鉴别,自然铜的理化鉴别,冰片、当归、三七的薄层鉴别和当归的含量测定项。三七是活血止痛制剂中一味贵细原料药,具有止血活血的药理活性[2-5],在方中起到补血、散瘀定痛的作用[6]。近年来,随着三七价格的不断走高,出现了以价格较低的人参(红参)或三七茎叶冒充三七投料的现象[7-9]。现行标准采用薄层色谱法鉴别三七,分离度低,斑点(条带)重叠,专属性差。三七与其充伪品亲源关系相近,化学成分相似,可采用分子鉴定[10-13]或液相色谱[14-15]等技术进行鉴别。三七与三七茎叶可通过显微法加以区分。但上述方法操作繁琐,分析时间较长,所用仪器、试剂昂贵,对分析人员的要求也较高,故需要建立一种简便、快捷的鉴别方法。本文采用高效薄层色谱法,针对三七、人参、三七茎叶的特有成分,建立了活血止痛制剂中三七的专属性鉴别方法,并采用高分离度快速液相色谱-三重串联四极杆质谱(RRLC-QQQ/MS)对结果加以验证。
1 仪器与试药 1.1 仪器CAMAG Linomat-5半自动点样台,CAMAG REPORTSTAR薄层色谱摄像系统,METTLER AE240百万分之一电子天平,Agilent 1200高分离度快速液相色谱-6410B三重四极杆质谱联用系统。
1.2 试药当归对照药材(批号:120927-201014)、三七对照药材(批号:1 2 0 9 4 1 - 2 0 0 8 0 7)、乳香(埃塞俄比亚乳香)对照药材(批号:120970-200904)、土鳖虫(地鳖)对照药材(批号:121533-200702)、人参对照药材(批号:1 2 0 9 1 7 - 2 0 0 6 0 9)、红参对照药材(批号:121045-200604)、冰片(批号:110743-200905)、三七皂苷R1对照品(批号:110745- 200607)、人参皂苷Rg1对照品(批号:110703- 200726)、人参皂苷Re对照品(批号:110754- 200822)、人参皂苷Rf对照品(批号:111719- 200703)、人参皂苷Rb1对照品(批号:110704- 200318)、人参皂苷Rb3对照品(批号:111686- 200501),均来自中国食品药品检定研究院;人参皂苷Rd对照品(批号:171101)、人参皂苷Rc对照品(批号:170507)购于吉林大学,纯度均大于98%;自然铜、三七茎叶购于同仁堂药店。3个厂家(编号分别为A、B、C)的活血止痛散6批、3个厂家(编号分别为D、E、F)的活血止痛胶囊87批,均为国家药品评价抽验样品。预制高效硅胶薄层板(HPTLC Silica gel 60,20×10 cm)购于Merk公司。分析纯乙醚、二氯甲烷、甲醇、无水乙醇、正丁醇、硫酸、五氧化二磷、醋酸铵购于北京化学试剂公司,色谱纯乙腈购于Merck公司,水为超纯水。
2 方法与结果 2.1 供试品溶液的制备取活血止痛散/胶囊2 g,加乙醚40 mL,超声处理(功率:300 W,频率:40 kHz)10 min,滤过,药渣挥去乙醚,加甲醇30 mL,超声处理(功率:300 W,频率:40 kHz)15 min,滤过,滤液蒸干,残渣加水10 mL使溶解,用水饱和的正丁醇振摇提取2次,每次15 mL,合并正丁醇液,用水洗涤2次,每次10 mL,正丁醇液蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。
2.2 三七对照药材溶液的制备取三七对照药材0.5 g,加甲醇30 mL,按“2.1”方法同法制成对照药材溶液。
2.3 人参、红参、三七茎叶对照溶液的制备取人参、红参、三七茎叶粉末各0.5 g,加甲醇30 mL,按“2.1”方法分别制成人参、红参和三七茎叶对照溶液。
2.4 缺三七阴性对照溶液的制备取当归、乳香、冰片、土鳖虫、自然铜,按处方制得缺三七阴性样品,照“2.1”方法制得缺三七阴性对照溶液。
2.5 投人参、投红参、投三七茎叶假阳性对照溶液的制备取人参对照药材、红参对照药材、三七茎叶粉末,加当归、乳香、冰片、土鳖虫、自然铜,按处方分别制得投人参、投红参、投三七茎叶假阳性对照样品,按“2.1”方法制得相应假阳性对照溶液。
2.6 对照品溶液的制备取三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rf、人参皂苷Rb1、人参皂苷Rb3、人参皂苷Rd、人参皂苷Rc对照品适量,加甲醇分别制得浓度为0.2 mg·mL-1的对照品溶液。
2.7 高效薄层色谱条件[16]固定相:高效硅胶G薄层板。点样量:1 μL,点样后薄层板置五氧化二磷干燥器中真空干燥2 h以上。展开剂:二氯甲烷-无水乙醇-水(70:45:6.5),层析缸预平衡15 min,在相对湿度16%、温度18℃条件下展开。显色剂:10%硫酸乙醇溶液,105℃加热至条带清晰。检视:分别置紫外光灯(365 nm)和日光下检视。
2.8 RRLC-QQQ/MS条件色谱条件:色谱柱:Agilent Rapid Resolution HT SB-C18(2.1 mm× 100 mm,1.8 μm),柱温:30℃,流动相:5 mmol·L-1醋酸铵溶液-乙腈梯度洗脱(0~20 min,乙腈15%→45%;20~ 30 min,乙腈45%→75%),流速:0.4 mL·min-1,进样量:1 μL。
质谱条件:离子化模式:ESI-,离子源温度:120℃,毛细管电压:3500 V,干燥气温度:300℃,干燥气流速:9 L·min-1,雾化气压力:30 Psi。扫描方式:全扫描(SCAN),锥孔电压:30 V,碰撞能量:100 V。
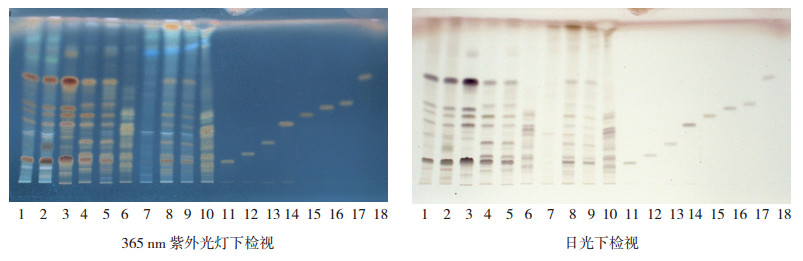
2.9 三七、人参、红参、三七茎叶的HPTLC薄层鉴别特征取活血止痛散和活血止痛胶囊供试品溶液各1份,三七对照药材溶液,人参、红参、三七茎叶对照溶液,缺三七阴性对照溶液,投人参、投红参、投三七茎叶假阳性对照溶液,人参皂苷Rb1、人参皂苷Rb3、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、三七皂苷R1、人参皂苷Rf和人参皂苷Rg1对照品溶液,点样,展开,色谱图见图 1。由表 1可见,三七皂苷R1是三七的特征成分,三七与人参(红参)的区别在于三七可检出三七皂苷R1,未检出人参皂苷Rb3或人参皂苷Rf;人参和红参可检出人参皂苷Rb3和人参皂苷Rf,未检出三七皂苷R1。三七与三七茎叶的区别在于三七可检出三七皂苷R1和人参皂苷Rg1,未检出人参皂苷Rb3;三七茎叶可检出人参皂苷Rb3,未检出三七皂苷R1或人参皂苷Rg1。采用本文的高效薄层色谱条件,以三七对照药材、三七皂苷R1(应检出)和人参皂苷Rb3(不得检出)为对照,可实现活血止痛制剂中三七的专属性鉴别和人参(红参)或三七茎叶的非法掺杂投料检查,阴性或假阳性样品无干扰。
|
1.活血止痛散;2.活血止痛胶囊;3.三七对照药材;4.人参;5.红参;6.三七茎叶;7.缺三七阴性样品;8.投人参假阳性样品;9.投红参假阳性样品;10.投三七茎叶假阳性样品;11.人参皂苷Rb1;12.人参皂苷Rb3;13.人参皂苷Rc;14.人参皂苷Rd;15.人参皂苷Re;16.三七皂苷R1;17.人参皂苷Rf;18.人参皂苷Rg1。 图 1 三七、人参、红参、三七茎叶的HPTLC鉴别特征 |
|
|
表 1 三七、人参、红参、三七茎叶的HPTLC鉴别特征 |
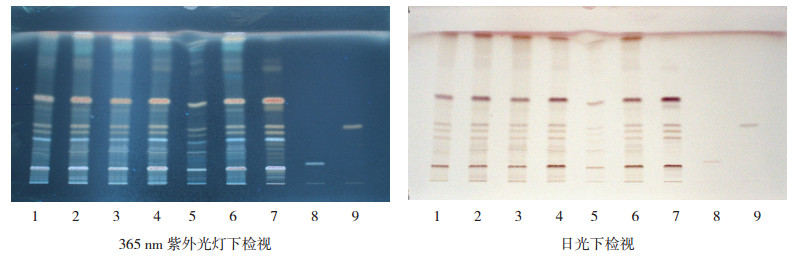
取活血止痛散和活血止痛胶囊、三七对照药材溶液、三七皂苷R1和人参皂苷Rb3对照品溶液,点样,展开,显色,检视。结果93批抽样均检出三七皂苷R1和三七对照药材对应的条带,未检出与人参皂苷Rb3对应的条带,所有批次样品均未发现人参、红参或三七茎叶非法投料,合格率为100%。不同厂家样品色谱图见图 2。
|
1~3. A、B、C 3个厂家的活血止痛散;4~6. D、E、F 3个厂家的活血止痛胶囊;7.三七对照药材;8.人参皂苷Rb3;9.三七皂苷R1。 图 2 样品检测结果 |
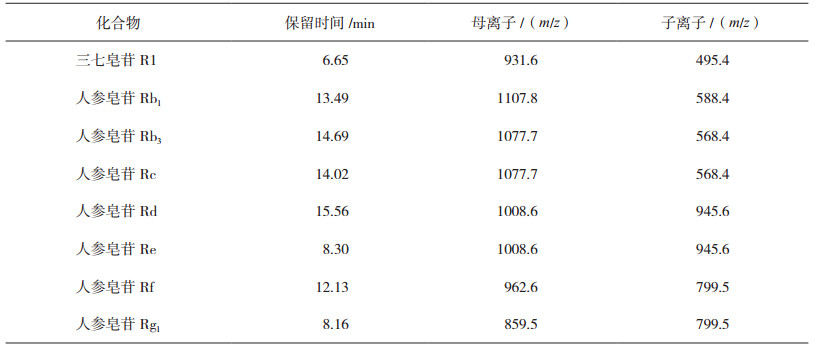
取“2.1”项下的供试品溶液和“2.6”项下的各对照品溶液,分别稀释1倍,依法测定。样品和对照品总离子流图见图 3,经与各对照品的保留时间、一二级质谱母、子离子m/z值(见表 2)比对,结果显示活血止痛散和活血止痛胶囊中均可检出人参皂苷Rb1、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、三七皂苷R1和人参皂苷Rg1,未检出人参皂苷Rb3和人参皂苷Rf,与HPTLC检测结果一致。

|
1.活血止痛散;2.活血止痛胶囊;3.三七皂苷R1对照品溶液;4.人参皂苷Rb1对照品溶液;5.人参皂苷Rb3对照品溶液;6.人参皂苷Rc对照品溶液;7.人参皂苷Rd对照品溶液;8.人参皂苷Re对照品溶液;9.人参皂苷Rf对照品溶液;10.人参皂苷Rg1对照品溶液。 图 3 RRLC-QQQ/MS总离子流图 |
|
|
表 2 各对照品保留时间和一二级质谱信息 |
试验尚对三七的主根(传统药用部位)、支根(筋条)及根茎(剪口)的皂苷类成分进行了比较,结果显示三者HPTLC薄层色谱基本一致,由于中国药典已将支根和根茎列为三七药材的合法来源,故不再继续讨论。
3.2 薄层板的选择比较了不同厂家的普通和高效薄层硅胶板的分离效果,结果普通薄层板均不能将人参皂苷Re与三七皂苷R1、人参皂苷Rb1与人参皂苷Rb3有效分离,高效薄层板中以Merk公司产品分离效果最好。
3.3 温度和湿度的影响温度和相对湿度对条带分离度影响很大,相对湿度应控制在20%以下,温度在10~25℃均可。薄层板点样后应先干燥,再立即放入平衡好的展开缸内展开。
3.4 点样量的影响三七对照药材和样品中人参皂苷Rb1含量较高,条带扩散拖尾会影响人参皂苷Rb3的检查,试验中可根据展开情况适当降低点样量,以获得最好的结果。
| [1] |
中华人民共和国药典: 一部[S]. 2015: 1292-1293.
|
| [2] |
孙雯怡, 罗旺辉, 周铖, 等. 三七总皂苷预处理对大鼠肾缺血再灌注损伤的保护作用及机制研究[J]. 湖南中医药大学学报, 2018, 38(1): 21-26. DOI:10.3969/j.issn.1674-070X.2018.01.006 |
| [3] |
李泽东, 赵荣华, 张兆传, 等. 三七皂苷合成及调控机制的研究进展[J]. 中国实验方剂学杂志, 2018, 24(14): 71-77. |
| [4] |
谭亮. 三七皂苷R1药理作用的研究进展[J]. 中国药理学通报, 2018, 34(5): 604-607. DOI:10.3969/j.issn.1001-1978.2018.05.004 |
| [5] |
陈社带, 邹燕, 赵伟国, 等. 三七总皂苷对大鼠缺血心肌血管新生及相关生长因子的影响[J]. 辽宁医学院学报, 2015, 36(1): 7-9. DOI:10.3969/j.issn.1674-0416.2015.01.003 |
| [6] |
关志宇, 濮存海, 段广勋. 活血止痛胶囊处方考证及研究进展[J]. 食品与药品, 2006, 8(2A): 17-21. |
| [7] |
刘永利, 赵振霞, 苏建, 等. 三七粉质量评价研究[J]. 中国药事, 2017, 31(4): 407-411. |
| [8] |
钟玉兰, 乐智勇. 利用近红外光谱技术快速鉴别三七粉及其伪品[J]. 江西中医药大学学报, 2018, 30(3): 70-76. |
| [9] |
李争. 三七及其混伪品鉴别方法研究[J]. 亚太传统医药, 2017, 13(13): 27-28. |
| [10] |
陈康, 蒋超, 金艳, 等. 人参属中药材高分辨率熔解曲线鉴定及其方法学考察[J]. 药物分析杂志, 2017, 37(1): 64-73. |
| [11] |
刘丽, 肖炳燚, 聂平, 等. 采用RAPD技术对人参属的亲缘关系和鉴别的分析[J]. 药物分析杂志, 2016, 36(2): 255-260. |
| [12] |
刘丽, 肖炳燚, 罗晖明, 等. 三七特异性PCR真伪鉴别方法研究[J]. 药物分析杂志, 2016, 36(5): 878-886. |
| [13] |
刘丽, 肖炳燚, 罗晖明, 等. 多重PCR方法同时鉴别人参、西洋参、三七[J]. 药物分析杂志, 2016, 36(4): 668-677. |
| [14] |
韩丽丽, 孙俊英, 马全龙. 三七粉及其一种伪品的鉴别检验研究[J]. 时珍国医国药, 2016, 27(12): 2932-2933. |
| [15] |
徐倩. HPLC法鉴别两种三七片伪品的应用分析[J]. 药品评价, 2016, 13(14): 40-50. DOI:10.3969/j.issn.1672-2809.2016.14.006 |
| [16] |
颜玉贞, 余琼希, 谢培山. 三七药材高效薄层色谱指纹图谱分析:色谱条件优化的再研究[J]. 中药新药与临床药理, 2007, 18(4): 303-305. DOI:10.3321/j.issn:1003-9783.2007.04.018 |
 2019, Vol. 33
2019, Vol. 33