国家药品标准物质是药品按标准进行检验的物质基础, 是提高药品检验检测能力的必备条件, 对于有效控制药品生产及流通领域的质量具有重要意义。中国食品药品检定研究院(以下简称中检院)是负责药品、医疗器械国家标准物质的计划、研究、制备、标定、审核、分发和管理工作的唯一法定机构[1-2]。
长期以来, 中检院标准物质工作不断提升研制生产和供应管理能力水平, 围绕组织相关标准物质的生产和审评, 扩大品种数量和覆盖范围, 提高标准物质制备生产和仓储能力, 加快标准物质供应模式升级, 优化管理、畅通渠道, 持续提升一级供应能力和服务水平等方面, 力求为监管提供更丰厚的物质保障[3-5]。随着标准物质涉及的学科、规模迅速发展, 目前, 能够对外供应的各类别国家药品标准物质数量已经达到了4036个品种。目前, 中检院为了实现对国家药品标准物质的全过程信息化管理, 建立了一套完善的信息管理系统[6], 对国家药品标准物质从计划立项、原料登记、分装、标定、报告审核、包装[7]、入库、一直到供应的全部流程进行信息化、自动化管理, 为保障标准物质供应提供了现代化管理手段。本文建立的国家药品标准物质保障供应综合数据平台, 是信息管理系统中最关键和最重要的组成部分之一。
1 建设国家药品标准物质保障供应综合数据平台的必要性和设计思路 1.1 管理工作中面临的实际需求国家药品标准物质的缺断货问题, 是国际国内同行共同面对的问题。尽管我们采取了许多措施也取得了显著成效, 但是, 依然有部分品种由于政策限制、原料获取困难、换批制备时的衔接而产生断货情况。因此, 保障药品、医疗器械国家标准物质供应一直是我院相关部门的核心任务和工作目标, 满足药品监管需求和促进行业发展要求给我们的工作提出了更高要求, 不断研制新品种和做好已有品种在换批制备时的无缝衔接, 这也将是一项长期的、持续改进的工作[8]。同时, 如何处理好品种需求数量、质量与如何高效利用有限生产资源的关系, 做到按需研制供给, 也是标准物质生产者所要面对的重大现实问题。
1.2 平台建设的必要性随着国家药品标准物质日益增长的质量、数量需求, 以及国际标准ISO 17034标准物质生产者能力认可的新要求[9-12]已经成为近年来药品标准物质工作的重中之重。对标准物质进行严格的全面质量控制, 结合信息化手段进行全流程数字化、智能化管理, 同时, 加大研制技术力量和设施设备投入, 提升研发、生产、储藏和供应能力, 使品种数量、覆盖领域及保障供应率逐年增长。应用信息化管理和分析方法与现有的标准物质管理相结合, 将会给标准物质的管理工作再带来一次深刻性的革命, 以管理和生产制备过程的数据为基础, 建立开放型平台, 对管理过程的影响因素采用量化的方法进行界定, 指导管理体系提升, 为对接国际标准ISO 17034奠定重要基础。
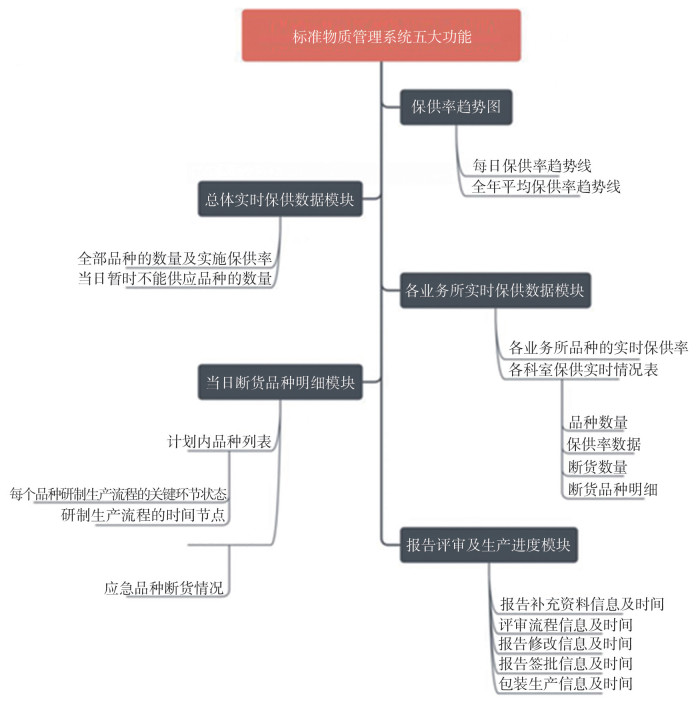
1.3 平台设计思路对于国家药品标准物质保障供应综合数据平台的基本构成的设计, 既需要满足管理部门对保障供应等信息获取的及时性、准确性, 又需要满足技术部门对品种研制阶段关键里程碑的掌握, 精确展现断货情况和各研制生产环节的责任主体, 技术路线及内容组成详见国家药品标准物质综合数据平台建设思维导图(图 1)。平台的主要建设过程包括以下四个阶段:1)全面梳理标准物质工作流程大数据; 2)查找现阶段工作流程的缺陷并进行调整优化; 3)调研实际需求, 建设中检院标准物质综合数据平台, 供管理部门和技术部门使用; 4)为标准物质对外供应平台提供准确数据源做好储备。
|
图 1 国家药品标准物质综合数据平台建设思维导图 |
国家药品标准物质保障供应综合数据平台的建设, 是利用先进的科学管理理念和建设方法对基础数据库进行整理和开发, 并以此为基础建立了科学性、可监督性的里程碑式管理模式。该平台共涵盖与国家药品标准物质保障供应相关的五大主要功能, 经过不断优化、改进、完善, 最终顺利上线运行。
2.1 保供率趋势图该功能可按选定时间、范围展现标准物质保障供应数据的总体趋势, 横轴为时间, 纵轴为供国家药品标准中使用的3078个标准物质品种的保障供应率。其中, 每日保供率趋势线展示一个月内每天的保供率变化; 全年平均保供率趋势线是以自然年为时间周期计算所得的平均值。
2.2 全品种实时保供数据模块该模块提供全部供国家药品标准中使用的标准物质品种和当日暂时不能供应的品种的实时数量, 计算并展示全部品种的实时保障供应率。
2.3 各责任部门实时保供数据模块该模块展示各责任部门的实时保供率和情况明细表, 包括品种数量、断货数量、保供率数据、断货品种明细等信息, 用以共享各品种的保障供应情况, 以便各级管理人员和研制人员进行查询跟踪。
2.4 当日断货品种明细模块该模块显示当天断货品种的全部研制生产流程的关键环节状态和时间节点, 为管理部门和技术部门的计划与生产工作调整提供依据。
2.5 报告评审及生产进度模块该模块展示技术部门提交报告后的补充资料信息、评审流程信息、研制报告修改信息、签批信息、包装生产信息及上述各步骤启动及完成的时间节点, 便于管理人员进行跟踪督办。同时, 从该模块中获取的评审及生产信息, 也成为编制"国家药品标准物质供应新情况"平台, 向用户提供品种上市预告及停用等信息的重要数据源。
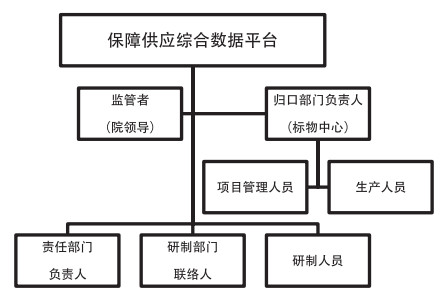
3 结论与讨论国家药品标准物质的供应保障是中检院的职能职责, 其研制生产的过程控制与协调, 直接影响工作效率和责任追溯。国家药品标准物质保障供应综合数据平台承载了标准物质的保障供应情况, 以精细化、规范化、信息化的方法和手段, 详细展示了各个品种的工作周期和生产进度的责任者, 目的是真正实现全程监控国家药品标准物质的生产流程, 该平台的基础数据库的数据容量约为3万条, 包含我院标准物质的全部必供品种的编号、批号、所属部门、断货情况、研制生产阶段、报告评审阶段、审评审批阶段、销售数据等全部基础信息。并以每天平均8000条数据的频次对上述3万条基础数据进行更新、同步和备份。同时, 通过信息互联互通, 分享给平台使用者, 目前的平台用户主要是我院内部工作人员, 包括我院内部涉及国家药品标准物质工作的全部管理人员和研制人员(图 2), 从平台建成至今, 每日最高访问量可达100人次, 成为各部门标准物质相关工作人员共享信息的有力工具, 也为保障国家药品标准物质供应的现代化信息管理提供了技术支持。自平台建成后, 对于断货品种起到了预测、密切监控和实时督办的显著成果, 以人参皂苷Re为例, 该品种属于我院对外供应的大品种之一, 涉及用户多, 使用量大, 使用范围广, 仅在2015年版《中国药典》中, 人参皂苷Re就在75个药典标准中用作鉴别及含量测定。2018年初, 根据平台数据预测, 该品种的110754-201626批将于今年内断货, 我院立即将该品种列入研制计划, 平台立即对该品种启动监控。2018年4月2日, 该品种新批原料征集到位并完成备案; 5月22日, 新批完成分装; 8月18日, 预测批断货; 8月20日, 研制部门完成新批研制工作并提交报告; 2018年8月22日, 报告资料补充齐全, 启动受理、审查审评; 8月24日, 报告完成签发; 9月1日, 完成包装入库, 对外供应, 新旧批次的交接在12天完成。保供平台在该品种的预测及研制生产过程中, 明确各阶段责任主体, 严密掌控各阶段流程信息, 对于各部门之间的信息公开共享和督办工作都起到了很好的效果。
|
图 2 国家药品标准物质综合数据平台主要使用人员 |
随着本系统开发重点的完成, 平台的主要功能已经投入使用, 下一步的建设重点是在保证日常使用、维护现有功能的基础上继续完善, 更好的为使用者提供更便捷、更详细、更准确的信息。同时, 整合了国家药品标准物质工作的数据资源, 实现了管理部门、业务部门的信息交换和实时数据共享, 为向终端用户提供重要进展数据奠定基础, 为进一步提升生产策划的科学性、正确性, 为合理安排和调整全局工作提供重要参考。
| [1] |
国家食品药品监督管理总局.国家食品药品监督管理局局令第28号药品注册管理办法[S]. 2007.
|
| [2] |
陈亚飞, 李晓东, 刘明理, 等. 药品标准物质基本特性与规范生产有关质量管理要求[J]. 中国药事, 2017, 31(2): 134-138. |
| [3] |
曹丽梅, 马双成, 马玲云, 等. 中检所药品、医疗器械标准物质管理新模式-从分散多头管理走向集中统一管理[J]. 药物分析杂志, 2010, 30(10): 1993-1995. |
| [4] |
苏丽红, 姚玲文, 马双成. 国家药品标准物质供应工作现状与探讨[J]. 中国药事, 2012, 26(1): 38-40. DOI:10.3969/j.issn.1002-7777.2012.01.013 |
| [5] |
王丹, 许明哲, 马玲云, 等. 国内外药品标准物质的管理概况[J]. 中国药事, 2014, 28(2): 185-189. |
| [6] |
曹丽梅, 刘明理, 赵宗阁, 等. 国家药品标准物质管理系统的建立及介绍[J]. 中国药事, 2017, 31(8): 882-886. |
| [7] |
王雅君, 赵宗阁, 肖新月. 国家药品标准物质标签及其说明书管理规范的建立与探讨[J]. 中国药事, 2016, 30(9): 895-899. |
| [8] |
谢晶鑫, 刘明理, 李澄, 等. 国家药品标准物质的项目化管理模式研究[J]. 中国药师, 2015(8): 1370-1371, 1425. DOI:10.3969/j.issn.1008-049X.2015.08.041 |
| [9] |
中国合格评定国家认可委员会. CNAS CL-04标准物质/标准样品生产者能力认可准则[S]. 2017.
|
| [10] |
International Organization for Standardization. ISO 17034: 2016 General Requirements for the Competence and Consistent Operation of Reference Material Producers[S]. 2016.
|
| [11] |
陈亚飞, 肖新月, 李波. 国外药品标准物质质量管理介绍及对我国的启示[J]. 中国药事, 2013, 27(12): 1258-1261. |
| [12] |
陈亚飞, 肖新月, 何平, 等. 标准物质稳定性考察规范解读和有效期管理方式的研究[J]. 中国药事, 2018, 32(3): 317-322. |
 2019, Vol. 33
2019, Vol. 33 
