2. 河南省食品药品检验所, 郑州 450008
2. Henan Provincial Institute of Food and Drug Control, Zhengzhou 450008, China
聚乙二醇是由环氧乙烷与水缩合而成的一种聚合物,在化学、纺织、造纸、农药和医药领域具有广泛应用[1-2]。聚乙二醇因聚合度不同可分为PEG300、PEG400、PEG600、PEG800、PEG1000、PEG1500等。不同分子量的PEG因性质不同在药用辅料中的用途也各不相同,低分子量的液态聚乙二醇常用作注射剂的溶剂,其比例可高达30%;高分子量的固体聚乙二醇可用作片剂包衣剂、乳膏基质等,其分子量和分子量分布需严格控制[3]。目前,《中国药典》2015年版收录PEG300(供注射用)和PEG400(供注射用)的分子量测定方法为端基分子量测定法,无法获知分子量分布信息,且化学滴定法测定分子量容易受多种因素影响,如水浴温度、滴定终点判定等[4]。近年来,高效凝胶渗透色谱法(HPGPC)与多检测器联用常用于化工行业的高分子化合物的质量控制,而该法用于药用辅料分子量及其分布的测定标准尚处于起步阶段。分子量等功能性指标可影响药用辅料的物理性能[5-7],从而影响最终药物制剂的释药行为[8-9]。本研究采用HPGPC法检测聚乙二醇分子量,可同时测定其分子量分布,并对影响分子量测定结果的关键参数如色谱柱类型、进样浓度、对照品来源进行系统考察。同时,将优化后的方法进行3家实验室间结果比对,结果表明本文建立的HPGPC法可用于测定PEG400分子量及其分布测定,为药物制剂一致性评价中辅料聚乙二醇的质量控制积累研究数据。
1 仪器与试药Agilent 1260高效液相色谱仪(示差折光检测器,美国Agilent公司);XS205DU型电子分析天平(METTLER TOLEDO公司);Millipore超纯水;色谱柱shodex Ohpak SB-802.5HQ和SB-803HQ(日本Shodex公司)。不同分子量的聚乙二醇对照品分别购于美国SP2公司(批号:20151201),德国PSS公司(批号:pegkit-05);叠氮钠购自天津南开允公合成技术有限公司(批号:20110708);硝酸钠购自国药集团化学试剂有限公司(批号:20131206);邻苯二甲酸酐购自天津博迪化工股份有限公司(批号:2011913);吡啶购自国药集团化学试剂有限公司(批号:20150504);0.5 mol·L-1氢氧化钠滴定液购自国家化学试剂质检中心(批号:201607);样品24批次来自国内6家辅料生产企业。
2 方法与结果 2.1 色谱条件色谱柱:Shodex OHpak SB-802.5HQ(300 mm×8 mm),Shodex OHpak SB-803HQ(300 mm×8 mm),流动相:0.1 mol·L-1硝酸钠溶液(含0.02%叠氮钠),并对影响HPGPC分子量测定的关键因素如供试品浓度、对照品来源、色谱柱、流速等进行优化。
2.2 溶液的制备 2.2.1 对照品溶液精密称取不同分子量的PEG标样,加流动相溶解,混匀,静置过夜,即得2 mg·mL-1的系列分子量对照品溶液。
2.2.2 供试品溶液精密称取适量样品,加流动相溶解,制得不同浓度的供试品溶液(10、5、2、1.5、1、0.5 mg·mL-1),混匀,静置过夜,进样前,用0.22 μm的微孔滤膜过滤。
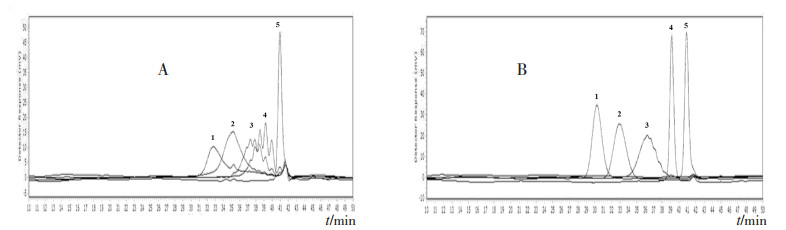
2.3 色谱条件考察 2.3.1 不同对照品的考察目前,聚乙二醇对照品供应商较多,考虑到聚乙二醇为聚合物,聚合物具有多分散性的特点,对照品质量会影响标准曲线计算的准确性。因此,比较了2个对照品公司的聚乙二醇对照品建立的标准曲线。试验条件同“2.1”节。结果表明:美国SP2公司标样低分子量部分的峰形呈现锯齿峰,德国PSS公司生产的聚乙二醇标样无锯齿峰(见图 1)。因标准曲线的建立是依据峰尖分子量的对数与保留时间作图所得,因此,锯齿多峰的对照品影响标准曲线的建立。最终选择德国PSS公司对照品建立标准曲线,计算供试品分子量。
|
图 1 不同公司PEG对照品叠加色谱图 A.美国SP2公司对照品(峰1~5分别为PEG960、PEG590、PEG320、PEG220、PEG108);B.德国PSS公司对照品(峰1~5分别为PEG1962、PEG982、PEG430、PEG194、PEG106)。 |
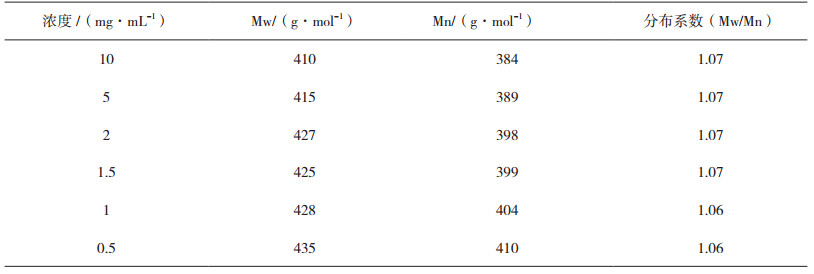
取“2.2.2”节不同浓度的供试品溶液,在“2.1”节色谱条件下,进样分析。对于不同浓度PEG400样品,在浓度1~2 mg·mL-1时,分子量测定结果进入平台期,示差检测器为浓度型检测器,对于低分子量的供试品溶液建议适当增加供试品溶液浓度,因此,选择2 mg·mL-1作为优化后的供试品溶液浓度。
|
|
表 1 不同浓度PEG400分子量HPGPC测定结果 |
依据“2.3.1”节测定结果,选择德国PSS标样配制不同分子量的标准溶液。取“2.2.1”节配制的PEG106、PEG194、PEG430、PEG982、PEG1960的对照品溶液,按“2.1”节色谱条件进样分析,以PEG标样峰尖分子量对数(logM)对其出峰时间(t)作图,得线性回归方程:logM =-0.0003874t3+ 0.03959t2-1.454t+21.77,相关系数r=0.9999。
2.3.4 色谱柱考察目前,尚无国家标准规定聚乙二醇分子量测定用色谱柱,本试验选择分子量分离范围适宜的SB系列色谱柱(SB-802.5HQ和SB-803HQ串联)和TSK系列色谱柱(TSK gel G2500PWxl和TSK gel G3000PWxl串联),在“2.1”节色谱条件下,依据“2.3.3”节线性回归方程,计算24批次样品PEG400的分子量Mw及分子量分布系数,并对比端基分析滴定法,测定结果见表 2。
|
|
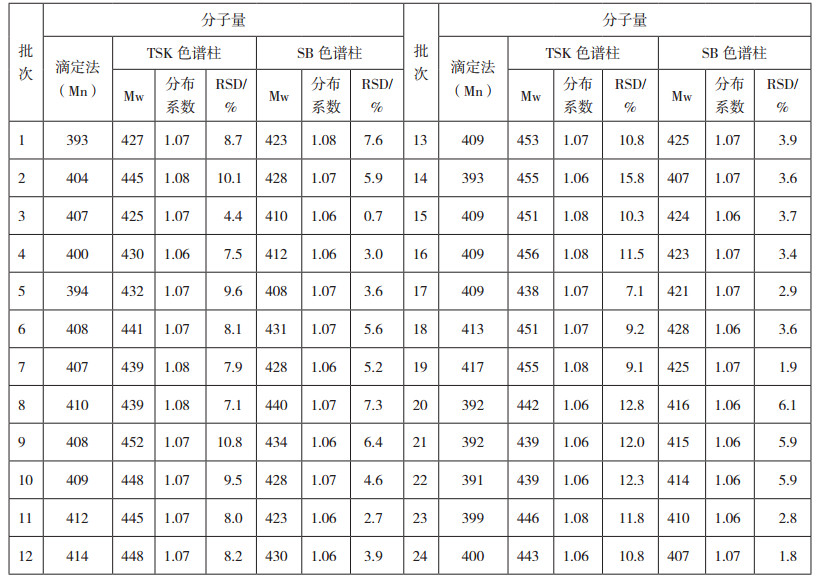
表 2 滴定法和HPGPC法测定24批次PEG400分子量结果 |
表 2结果表明,以滴定法测定的各批次PEG400分子量分别与HPGPC法使用TSK和SB色谱柱得到的重均分子量计算平均RSD分别为9.7%和4.2%,说明HPGPC法选用SB色谱柱测定聚乙二醇400分子量与端基分析滴定法结果较为接近。
3 方法学考察及结果 3.1 精密度考察取批次4的PEG供试品,按“2.1”节色谱条件进样,重复进样5次,计算重均分子量的RSD值为0.2%,结果表明仪器精密度良好。
3.2 重复性考察因聚合物溶胀程度不同,会影响分子量测定结果,因此,按优化后的色谱条件平行配制5份PEG供试品溶液,按“2.1”节色谱条件进样,记录色谱图,依据标准曲线,计算重复性样品的重均分子量,RSD为2.89%,说明优化后的PEG400分子量测定方法重复性好。
3.3 稳定性考察取同一份供试品溶液,按优化后的色谱条件进样,考察0、12、24 h的稳定性,记录色谱图,依据标准曲线计算供试品的重均分子量,计算24 h内供试品分子量的相对标准偏差RSD为0.66%,说明样品在24 h内稳定性良好。
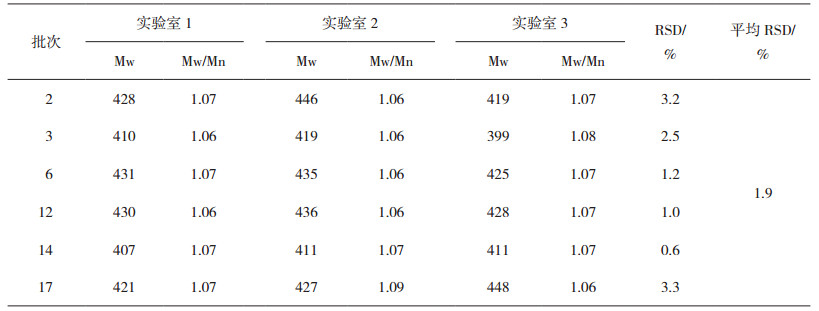
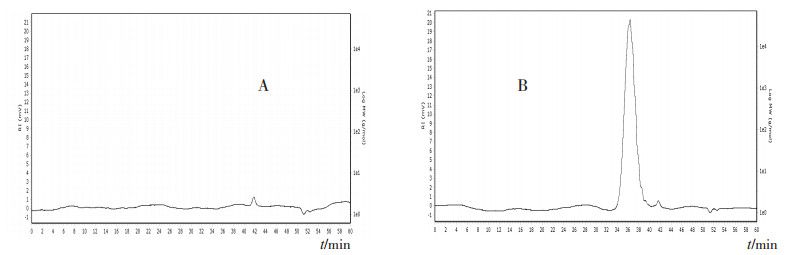
3.4 重现性考察将色谱条件优化后的PEG400分子量测定方法分别于3家实验室共同测定,典型色谱图见图 2,测定结果见表 3,各实验室间测定结果的平均相对标准偏差RSD为1.9%。
|
图 2 HPGPC法测定PEG400色谱图 A.空白溶液;B.供试品溶液(批次14)。 |
|
|
表 3 实验室间测定PEG400分子量结果比较 |
采用HPGPC方法测定聚合物分子量,该方法依据不同分子量对照品分子量对数对出峰时间作图,建立标准校正曲线,计算供试品的平均分子量。因此,首先,应选择对照品与待测物具有相同或相似的结构,才能获得准确的分子量测定结果;其次,应考虑色谱柱类型、对照品来源、柱温等色谱条件对测定结果的影响。本试验对HPGPC方法进行优化,发现不同公司的对照品质量和色谱柱可明显影响PEG400分子量测定结果,柱温(25~35℃)和流速(0.5~0.7 mL·min-1)范围内变化,不影响分子量测定结果;并尝试将优化后的方法测定其他聚合度的PEG如PEG600、PEG1000、PEG1500,均可获得满意的结果。
4.2 不同分子量测定方法分析《中国药典》2015年版收录的不同聚合度聚乙二醇标准中分子量测定法为端基分析法,端基分析法的测定原理是依据重复基团的化学反应摩尔数,计算得到待测化合物的平均分子量。因此,该方法随聚合物分子量的增大,供化学反应的端基基团比例下降,测定准确度降低[10];且化学滴定易受反应温度和滴定终点判定等因素的影响。因此,需要建立准确度高的分子量测定方法用于不同聚合度的聚乙二醇分子量测定。聚乙二醇400(供注射用)与各种溶剂具有广泛相容性,是很好的溶剂和增溶剂,有报道聚乙二醇分子量大于600会出现固液共存的现象[3],因此,需要严格控制聚乙二醇400(供注射用)的分子量和分子量分布。本试验建立的聚乙二醇HPGPC分子量测定方法具有供试品与对照品结构相同、测定准确、快速的优点,适合多批次、不同聚合度聚乙二醇分子量质量控制分析,除获知待测样品的分子量信息外,还可得到样品分子量分布、其他杂质峰等丰富信息,可作为中国药典的补充替代方法。
| [1] |
谢富春, 朱长春, 张玉清. 聚乙二醇合成工艺[J]. 化学推进剂与高分子材料, 2005, 3(4): 6-9. DOI:10.3969/j.issn.1672-2191.2005.04.002 |
| [2] |
汪多仁. 聚乙二醇的应用与合成进展[J]. 化学工业与工程技术, 2000, 21(5): 21-23. DOI:10.3969/j.issn.1006-7906.2000.05.007 |
| [3] |
Handbook of Pharmaceutical Excipients[M]. 7th Edition. London: pharaceutical press. 2012: 585-591.
|
| [4] |
中国药典: 四部[S]. 2015: 612-613.
|
| [5] |
Guo Q, Lei N, Li L, et al. Estimation of the Critical Quality Attributes for Hydroxypropyl Methylcellulose with Near-infrared Spectroscopy and Chemometrics[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2017, 177: 158-163. |
| [6] |
Palcsó B, Zelkó R. Different Types, Applications and Limits of Enabling Excipients of Pharmaceutical Dosage Forms[J]. Drug Discovery Today:Technologies, 2018. |
| [7] |
Nakajima T, Takeuchi I, Ohshima H, et al. Push-Pull Controlled Drug Release Systems:Effect of Molecular Weight of Polyethylene Oxide on Drug Release[J]. Journal of Pharmaceutical Sciences, 2018, 107(7): 1896-1902. DOI:10.1016/j.xphs.2018.02.022 |
| [8] |
王淼, 伍伟聪, 张东升. 羟丙甲纤维素对头孢克洛缓释片释放度的影响[J]. 中国生化药物杂志, 2015, 35(10): 127-130. |
| [9] |
王浩, 栾瀚森, 梅蕾, 等. PLGA的结构和分子量对纳曲酮微球体外释药的影响[J]. 中国医药工业杂志, 2005, 36(7): 405-407. DOI:10.3969/j.issn.1001-8255.2005.07.011 |
| [10] |
金日光, 华幼卿. 高分子物理[M]. 北京: 化学工业出版社, 2000: 89-92.
|
 2018, Vol. 32
2018, Vol. 32