抗生素是微生物次级代谢的产物。工业上通过对特定微生物进行调控发酵,使其形成特定的抗生素等代谢物[1],再采用溶媒浸泡提取或固液分离等手段从发酵物中获取目标产物,同时形成发酵菌渣[2]。在抗生素菌渣中除含有大量的生产菌菌体,发酵中未完全被利用的各种不溶性成分,如淀粉和黄豆粉等复合碳氮源、不溶性盐、微量元素和大量的水分(大于70%)外,通常还含有未被完全提取的抗生素及其他代谢产物[2-7]。据文献[4]报道,在青霉素、链霉素、土霉素、四环素和盐酸林可霉素发酵产生的湿菌渣中,残留效价分别约为3000、4700、9000、26000 U·g-1和720 U·g-1。作为固体垃圾未经处理的发酵菌渣,不仅其中残留的抗生素等可溶性代谢产物会随着渗滤液和污水排放到环境中,且由于发酵菌渣中含有丰富的蛋白质等营养成分,习惯上被作为动物饲料/饲料添加剂利用。对发酵菌渣的不合理处理方式,会导致抗生素对环境的污染、诱导耐药基因的产生[8-9],进而加剧耐药微生物的产生,影响人类的健康。为此,2002年2月,农业部、卫生部、国家药品监督管理局在第176号公告中明令禁止在饲料和动物饮用水中使用抗生素菌渣[10]。自2002年8月23日起,将干菌渣作为饲料生产、销售被确认是违法、违规经营活动,将受到相应的处罚。2008年6月6日,环保部、国家发改委又将抗生素菌渣列入《国家危险废物名录》 [11]。2012年3月,在环保部颁布的2012年第18号公告的附件3《制药工业污染防治技术政策》中,第五条“固体废物处置和综合利用”第二款明确规定:“生产维生素、氨基酸及其他发酵类药物产生的菌丝废渣经鉴别为危废的,按照危险废物处理”,同时鼓励研究、开发、推广“发酵菌渣在生产工艺中的再利用技术、无害化处理技术、综合利用技术,危险废物厂内综合利用技术” [12]。
目前,除采用传统焚烧和填埋的方式处理抗生素发酵菌渣外,各大制药企业、科研机构等在抗生素发酵菌渣的无害化和资源化再利用方面开展了大量的探索性研究。已报道的无害化处理手段包括:高温处理、化学处理、微生物降解和酶法降解等[13-15],经无害化处理后的菌渣可以作为发酵原料替代品、饲料添加剂、有机肥料、生物吸附剂,以及用于提取活性物质、生产石膏缓凝剂或可降解生物薄膜等[4, 13, 16-17]。虽然采用堆肥或厌氧消化等微生物技术处理抗生素菌渣[2, 18-21],可同时实现无害化和资源再利用之目的;处理后的抗生素发酵菌渣已在畜牧业和农业生产中大量使用[6, 22-24];但我国至今尚未建立抗生素发酵菌渣无害化处理与再利用的安全控制标准[2, 4, 16, 18, 25-27],且在国际范围内有关抗生素发酵菌渣的评估指标体系也无公认的参照标准。已有文献报道,施用经无害化、资源化处理的抗生素发酵菌渣为肥料的蔬菜地土壤中残留抗生素的量高于单独施用化肥的蔬菜地[28]。
据统计,2013年我国抗生素原料产量约12.12万吨,通常获得1吨抗生素会产生40吨湿菌渣[2],据此,仅2013年产生的抗生素发酵菌渣就达485万吨左右。我国由生产β-内酰胺类抗生素产生的发酵菌渣约占总菌渣的77.88%[29],即约380万吨左右。β-内酰胺类抗生素主要包括青霉素类和头孢菌素类,两者占比约为9︰1[4],即头孢菌素类发酵菌渣占抗生素生产发酵总菌渣的7.8%。由此估算,仅2013年产生的头孢菌素C菌渣约38万吨。本研究以收集到的经3种不同微生物无害化处理的头孢菌素C发酵菌渣为研究对象,利用抗生素微生物检定法对其残留的抗菌活性进行评估,采用HPLC方法分析样品中可能残留的活性成分,并通过LC-MS推测其可能结构,进而对不同的无害化处理方法进行评价。
1 材料和方法 1.1 仪器Waters高效液相色谱仪(包括Waters 2690 Separations Module、Waters 996 Photodiode Array Detector和Millennium 32 Software);LC-MS仪器:资生堂Nano-Space S1-2色谱系统;AB Qtrap3200 MS/MS/MS系统;CHB-1抗生素效价测量仪;GRP- 9270型隔水式恒温培养箱;高压灭菌锅。
1.2 试剂青霉素对照品(批号:130437-201306,含量:93.1%,效价:1578 u·mg-1),霉素酶对照品(批号:130441-201701,效价:≥6000000单位/2 mL/h),抗生素检定用培养基Ⅱ(pH 6.5~6.6),金黄色葡萄球菌ATCC29213、大肠埃希菌ATCC25922和灭菌水均由中国食品药品检定研究院提供。乙腈、甲醇、甲酸均为色谱纯。
1.3 菌渣样品FS1菌渣(批号:201506、201508、201601),FS2菌渣(批号:201601-1、201601- 2、201601-3),FS3菌渣(批号:201506、201508-1、201508-2、201508-3)和FS4菌渣(批号:201506、201508-1、201508-2、201508-3、201508-4),均由挪威Cambi公司提供。
1.4 供试液的制备称取FS1菌渣5 g,加灭菌水50 mL,充分震摇,离心,取上清液作为供试液T-FS1;将FS2菌渣、FS3菌渣、FS4菌渣分别直接离心取上清液作为供试液T-FS2、T-FS3、T-FS4。诸供试液均分成2份:1份用于效价、HPLC和LC-MS测定;另1份按体积比20︰1加入青霉素酶后用于效价测定。
1.5 方法 1.5.1 效价测定方法按《中国药典》2015年版四部1201抗生素微生物检定法第一法(管碟法),以金黄色葡萄球菌ATCC29213作为试验菌株,进行效价测定[30]。由于头孢菌素C及7-氨基头孢烷酸(7-ACA)的抑菌活性太弱,故选择青霉素作为评价尺度(青霉素对ATCC29213的MIC值为0.25~2 μg·mL-1[31])。方法的浓度测定范围:以青霉素活性单位计为1.2~81.1 u·mL-1;以青霉素重量单位计为0.7~47.9 μg·mL-1;最低检出限以青霉素活性单位计为3.08 u·mL-1;以青霉素重量单位计为1.82 μg·mL-1。
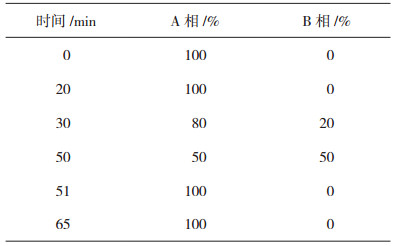
1.5.2 HPLC方法在文献HPLC方法[32]的基础上,建立新的梯度洗脱方法。流速:1.0 mL·min-1;检测波长:210 nm;柱温:30℃;色谱柱:CAPCELL PAK C18 MGⅡ(250 mm×4.6 mm,5 μm);进样体积:100 μL;按梯度洗脱表 1 [流动相A:水-乙腈(95︰5),流动相B:乙腈]进行分析。
|
|
表 1 常规HPLC分析梯度洗脱程序 |
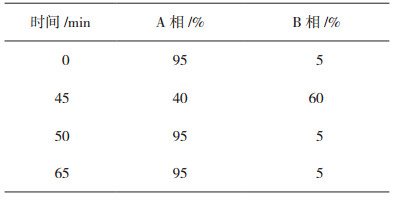
色谱条件:流动相:甲醇-0.1%甲酸水溶液(50︰50);流速:0.6 mL·min-1;柱温:40℃;色谱柱:资生堂MGII(150 mm×4.6 mm,5 µm);进样体积:20 µL。按梯度洗脱表 2进行分析。
|
|
表 2 LC-MS分析梯度洗脱程序 |
质谱条件:DP:50;CE:20;CES:10;GAS1:50;GAS2:50;IS:5500。
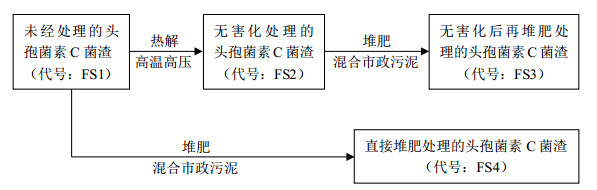
2 结果与讨论 2.1 对头孢菌素C菌渣抗菌活性的评价添加市政污泥堆肥处理抗生素残渣技术的实质是利用污泥中的厌氧微生物对有机物进行降解的过程[2]。头孢菌素C菌渣的无害化处理流程见图 1,对其残渣的抑菌活性进行评估,可直观有效地评价无害化处理效果。
|
图 1 头孢菌素C菌渣无害化处理流程 |
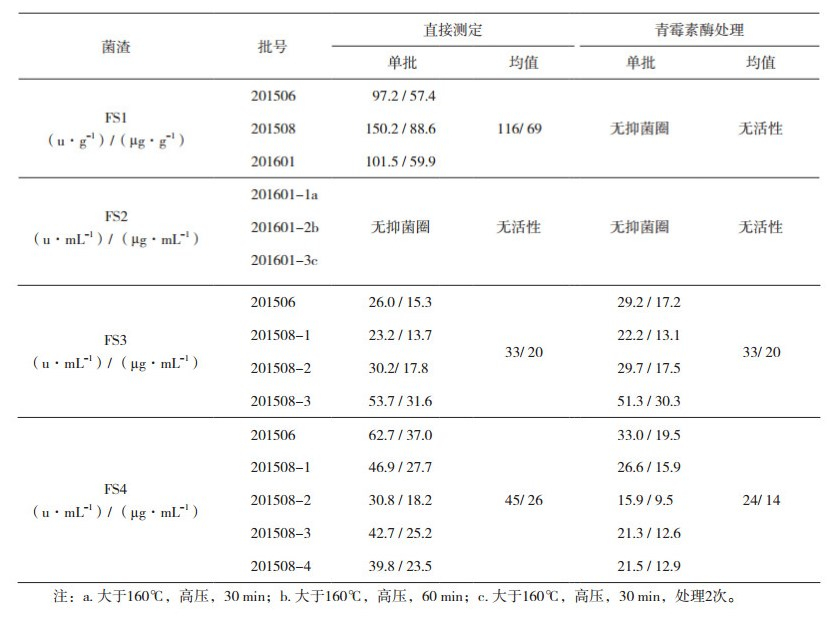
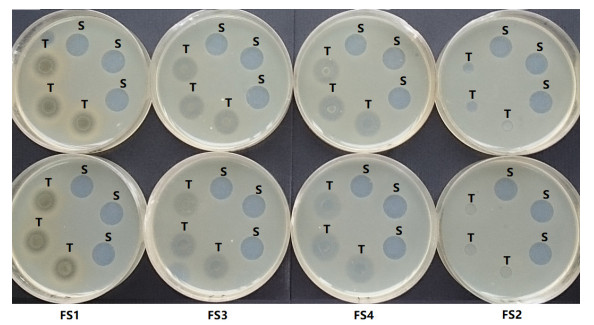
分别采用代表性的革兰阳性敏感菌株(金黄色葡萄球菌ATCC29213)和革兰阴性敏感菌株(大肠埃希菌ATCC25922)检测菌渣的抗菌谱。由试验结果可知,所研究菌渣仅对金黄色葡萄球菌ATCC29213具有抑菌作用,对大肠埃希菌ATCC25922基本无抑菌作用。进一步采用抗生素微生物检定法第一法(管碟法),以金黄色葡萄球菌ATCC29213为试验菌株,测定4种菌渣的残留抗菌活性(效价),同时对其耐青霉素酶的特性进行评估。4种头孢菌素C菌渣的抑菌情况见图 2,各菌渣样品的残留效价及其耐青霉素酶特性见表 3:FS1为未经处理的头孢菌素C菌渣,按青霉素计,其干品效价约为116 u·g-1或69 μg·g-1,经青霉素酶处理后其抑菌活性消失,提示菌渣中的抑菌活性物质为β-内酰胺类化合物。FS2为FS1菌渣经高温(>160℃)、高压(<20 MPa)处理后的菌渣,经高温、高压30 min灭活处理后,FS2菌渣不具抑菌活性。FS3和FS4的共同特点是菌渣与市政污泥混合进行堆肥处理;无抑菌活性的FS2菌渣在堆肥过程中产生了具有新抑菌活性物质的FS3菌渣,按青霉素计,其效价约为33 u·mL-1或20 μg·mL-1,且对青霉素酶不再敏感;FS1菌渣经堆肥处理得到的FS4菌渣的效价约为45 u·mL-1或26 μg·mL-1,经青霉素酶处理后效价降低至FS3菌渣近似水平(24 u·mL-1或14 μg·mL-1),提示堆肥过程中不仅产生了与FS3菌渣相同的新抑菌活性物质,且FS1菌渣中残留的-内酰胺类化合物未完全分解。
|
图 2 各类头孢菌素C菌渣中活性物质的抑菌/杀菌情况 注:S.青霉素对照品溶液所致抑菌圈;T. FS1~4菌渣供试液所致抑菌圈;平行试验2份。 |
|
|
表 3 头孢菌素C菌渣中抗菌活性物质对革兰氏阳性菌的效价测定结果(以青霉素计) |
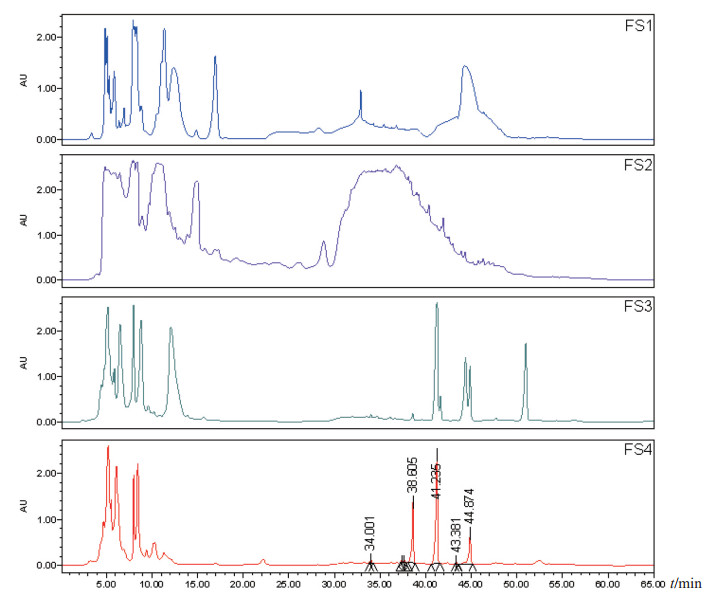
采用HPLC法分析菌渣中可能存在的非β-内酰胺类抑菌活性成分。可见,各类菌渣的HPLC色谱图存在明显差异,在经堆肥处理的FS3、FS4菌渣色谱图中,明显可见4~5个新形成的色谱峰(图 3)。
|
图 3 不同处理下菌渣的典型HPLC色谱图(常规梯度) |
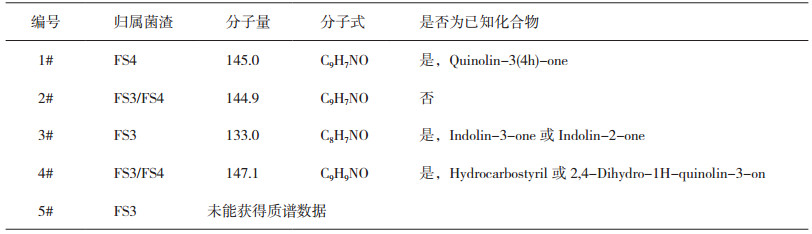
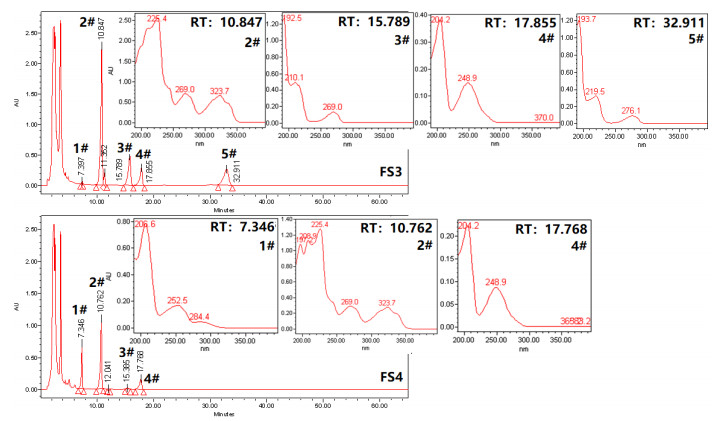
采用LC-MS对FS3和FS4菌渣色谱图中新形成的各色谱峰进行分析,根据保留时间将FS3、FS4菌渣中新形成的成分分别命名为1#、2#、3#、4#、5#(图 4),分别采集诸色谱峰的紫外光谱和质谱数据,推测各成分的结构,并以Mass Frontier 7.0对预测结果进行验证。除5#物质未能获得MS数据无法推测其结构外,对其他4种成分的MS推测见图 5~ 图 8,其结构信息见表 4。
|
图 4 经堆肥处理的不同菌渣的典型HPLC色谱图和紫外吸收光谱图(LC-MS梯度) |
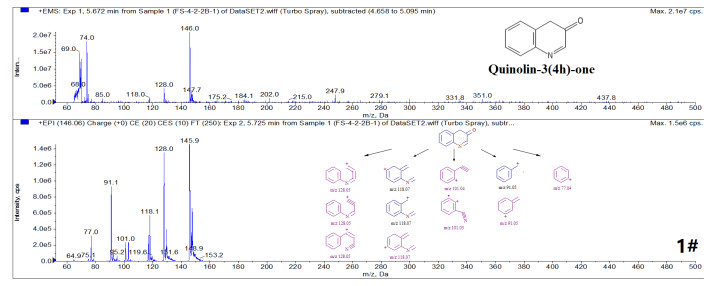
|
图 5 菌渣中1#物质的质谱信息和结构推测结果 |
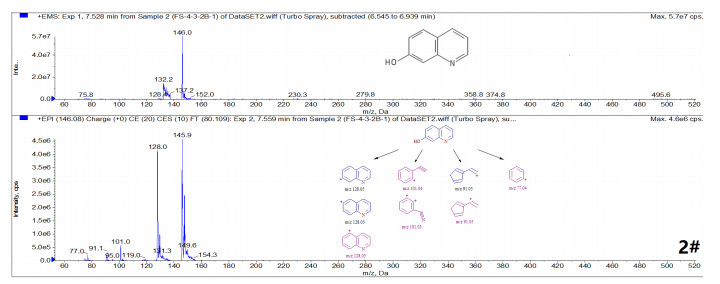
|
图 6 菌渣中2#物质的质谱信息和结构推测结果 |
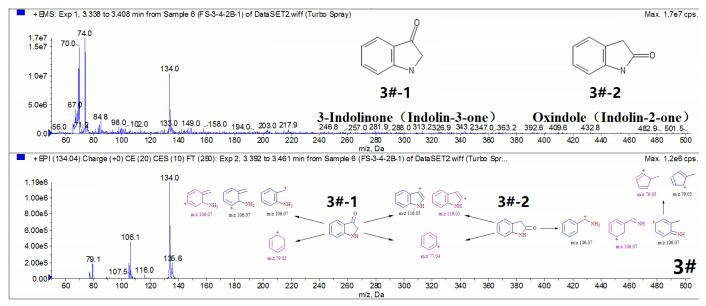
|
图 7 菌渣中3#物质的质谱信息和结构推测结果 |
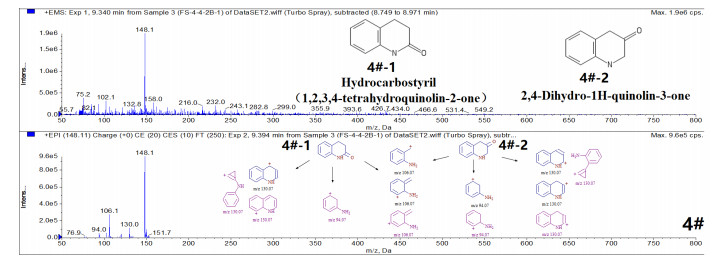
|
图 8 菌渣中4#物质的质谱信息和结构推测结果 |
|
|
表 4 堆肥处理后头孢菌素C菌渣新形成物质的结构信息 |
通过PubChem结构搜索查询:1#物质为Quinolin-3(4H)-one(MW:145.161g·moL-1),专利报道其具有抗菌活性[33];3#物质为3-Indolinone (Indolin-3-one)(MW:133.15g·moL-1),文献报道其为抗肿瘤抗生素[34];4#物质为Hydrocarbostyril(1, 2, 3, 4-tetrahydroquinolin-2- one)(MW:147.177 g·moL-1),欧洲化学品管理局(European Chemicals Agency,ECHA)已公布了其口服急性毒性、皮肤腐蚀性/刺激性、皮肤致敏性、严重眼损伤/眼睛刺激性、单次暴露的特定靶器官毒性、呼吸道刺激性等方面的安全和危险警示信息[35]。
3 结论采用代表性的革兰阳性敏感菌株和革兰阴性敏感菌株对无害化处理的抗生素菌渣的抗菌活性进行筛查,利用HPLC-MS对菌渣中残留/转化组分的结构进行推断,再结合利用相关化合物数据库对残留组分生物学/安全性信息的检索,是快速评价菌渣无害化处理效果的有效手段。
采用堆肥或厌氧消化等微生物技术处理抗生素菌渣,可同时实现无害化和资源再利用之目的。在对无害化处理效果进行评价时,除利用菌渣中特定的残留抗生素为评价指标外,还应考虑堆肥过程中菌渣残留成分的生物转化问题。
作为全球抗生素的生产大国,我国每年都会产生数百万吨的抗生素发酵菌渣,由已发表的文献报道推算仅2013年产生的抗生素发酵菌渣就达485万吨左右。从实际消化能力、减少二次污染、提高经济效益等角度考虑,如何将这些菌渣变废为宝对整个制药行业提出了挑战。目前,由于我国尚无菌渣无害化处理与再利用的安全控制标准,无法准确评价无害化菌渣是否已经达到了安全级别,不利于新的无害化、资源化技术的研发。呼吁相关部门尽快针对抗生素发酵菌渣的再利用出台相关技术标准。
| [1] |
陈代杰. 微生物药物学[M]. 北京: 化学工业出版社, 2008.
|
| [2] |
朱培, 张建斌, 陈代杰. 抗生素菌渣处理的研究现状和建议[J]. 中国抗生素杂志, 2013, 38(9): 647-651, 673. DOI:10.3969/j.issn.1001-8689.2013.09.002 |
| [3] |
贡丽鹏, 郭斌, 任爱玲, 等. 抗生素菌渣理化特性[J]. 河北科技大学学报, 2012, 33(2): 190-196. |
| [4] |
赵卫凤, 鲍晓磊, 张媛, 等. 河北省发酵类抗生素菌渣处置现状及存在的问题[J]. 安徽农业科学, 2013, 41(31): 12417-12421. DOI:10.3969/j.issn.0517-6611.2013.31.064 |
| [5] |
苑丽梅, 王梦梦, 王璞, 等. 头孢菌渣理化性质研究[J]. 哈尔滨商业大学学报:自然科学版, 2015, 31(6): 691-693, 703. |
| [6] |
王璞, 刘惠玲, 王冰, 等. 青霉素菌渣资源化为饲料原料的营养价值研究[J]. 环境保护科学, 2015, 41(1): 75-79. DOI:10.3969/j.issn.1004-6216.2015.01.016 |
| [7] |
肖艳春, 黄婧, 林香信, 等. 抗生素菌渣饲料化工艺技术[J]. 能源与环境, 2016(5): 25-26. DOI:10.3969/j.issn.1672-9064.2016.05.012 |
| [8] |
Corvaglia AR, Demarta A, Gaia V, et al. Role of Residual Antibiotics in Aquatic Environment on the Selection and Diffusion of Bacterial Resistances of Aeromonas, Acinetobacter and Legionella[J]. Arch Sci, 2008, 61(2): 89-100. |
| [9] |
Anderson AD, Nelson JM, Rossiter S. Public Health Consequences of Use of Antimicrobial Agents in Food Animals in the United States[J]. Microb Drug Resist, 2003, 9(4): 373-379. DOI:10.1089/107662903322762815 |
| [10] |
农业部, 卫生部, 国家药品监督管理局. 农业部公告第176号[S]. 中华人民共和国卫生法规汇编(2001-2003), 北京: 法律出版社, 2004: 301-304.
|
| [11] |
环境保护部. 国家危险废物名录[S]. 2008.
|
| [12] |
环境保护部公告2012年第18号制药工业污染防治技术政策[S]. 2012.
|
| [13] |
陈立文, 方森海, 王明兹. 抗生素发酵废菌渣的无害化及资源再利用研究进展[J]. 生物技术通报, 2015, 31(5): 13-19. |
| [14] |
张光义, 马大朝, 彭翠娜, 等. 水热处理抗生素菌渣制备固体生物燃料[J]. 化工学报, 2013, 64(10): 3741-3749. |
| [15] |
王斌, 董玉平, 毛叶兵, 等. 抗生素菌渣的流化床快速热解特性[J]. 化工学报, 2017, 36(3): 1113-1119. |
| [16] |
艾晗, 石鹏, 王辉, 等. 抗生素制药菌渣处理处置技术评价与分析[J]. 环境工程学报, 2016, 10(2): 906-914. |
| [17] |
王冰, 刘惠玲, 王璞. 青霉素菌渣理化特性及其资源化利用研究现状[J]. 环境工程, 2014, 32(2): 139-142. DOI:10.3969/j.issn.1671-1556.2014.02.029 |
| [18] |
公丕成, 蔡辰, 张博, 等. 我国抗生素菌渣资源化研究新进展[J]. 环境工程, 2017, 35(5): 107-111. |
| [19] |
温沁雪, 陈希, 张诗华, 等. 城市污泥混合青霉素菌渣堆肥实验[J]. 哈尔滨工业大学学报, 2014, 46(4): 43-49. |
| [20] |
王慧, 习彦花, 崔冠慧, 等. 头孢菌素菌渣中温厌氧资源化处理[J]. 中国沼气, 2016, 34(1): 19-24. DOI:10.3969/j.issn.1000-1166.2016.01.004 |
| [21] |
蒋明烨, 宋思奇, 付欢, 等. 厌氧发酵处理红霉素菌渣的效能及红霉素降解规律研究[J]. 环境保护科学, 2017, 43(4): 62-67. |
| [22] |
段子恒, 刘惠玲, 刘晴靓, 等. 青霉素菌渣肥对西红柿根际土壤微生物和酶活性的影响[J]. 环境工程, 2015, 33(11): 115-119. |
| [23] |
王悦, 孟昭虹, 刘惠玲, 等. 青霉素菌渣肥对土壤环境及萝卜品质的影响[J]. 环境科学研究, 2017, 30(5): 737-743. |
| [24] |
饶硕, 习彦花, 崔冠慧, 等. 头孢菌素C菌渣厌氧发酵沼液对黄瓜种子萌发的影响[J]. 中国沼气, 2017, 35(6): 10-14. DOI:10.3969/j.issn.1000-1166.2017.06.002 |
| [25] |
韩洪军, 陈凌跃, 马文成, 等. 我国微生物制药菌渣管理现状分析[J]. 环境工程, 2015, 33(1): 120-122, 89. |
| [26] |
刘华. 微生物制药菌渣管理现状[J]. 职业技术, 2017, 16(4): 120-121. |
| [27] |
王丽君. 抗生素菌渣利用处置技术现状及对策建议[J]. 绿色科技, 2017, 18: 152-154. |
| [28] |
鲍陈燕, 顾国平, 徐秋桐, 等. 施肥方式对蔬菜地土壤中8种抗生素残留的影响[J]. 农业资源与环境学报, 2014, 41(4): 313-318. |
| [29] |
刘园园. 我国抗生素菌渣处置技术现状[J]. 中国环保产业, 2017(8): 66-68. DOI:10.3969/j.issn.1006-5377.2017.08.012 |
| [30] |
国家药典委员会. 中国药典: 四部[S]. 北京: 中国医药科技出版社, 2015: 160-162.
|
| [31] |
Clinical and Laboratory Standards Institute. Performance Standards for Antimicrobial Susceptibility Testing: 28th Edition[S]. 2018: 162.
|
| [32] |
代长元, 于浩. HPLC法测定头孢菌素C钠盐的含量[J]. 黑龙江科技信息, 2009(7): 182. |
| [33] |
Macielag MJ, Weidner-wells MA, Lin SC. C-7 Is Oxazolinyl Quinolone/Naphthyridine Derivatives Useful as Antibacterial Agents: 美国, US7902227[P]. 2011-07-28.
|
| [34] |
Jia HY, Pan GJ, Wang YQ, et al. Design, Synthesis and Primary Biological Evaluation of the Novel Antitumor Agent Indoline-3-One and Its Derivatives[R]. Proceedings of the 2012 International Conference on Applied Biotechnology (ICAB 2012). Berlin: Springer, 2013: 875-882.
|
| [35] |
European Chemicals Agency-ECHA. 621-863-5: 1, 2, 3, 4-tetrahydroquinolin-2-one[DB/OL]. [2018-06-01]. https://www.echa.europa.eu/web/guest/information-onchemicals/cl-inventory-database/-/discli/details/155244.
|
 2018, Vol. 32
2018, Vol. 32