恶性梗阻性黄疸(Malignant Obstructive Jaundice,MOJ)是指由恶性肿瘤导致不同部位胆道狭窄或闭塞引起的梗阻性病变,是恶性肿瘤本身阻塞、压迫或淋巴结转移肿大压迫胆道,胆道梗阻引起胆红素逆流入血,引起的全身皮肤、黏膜及巩膜黄染的一类疾病[1]。该病是肝胆外科常见的病症,在我国的发病率有明显增加的趋势[2]。外科手术是目前治疗MOJ最有效的方法之一,而胆道感染是其术后主要的并发症之一[3]。由于抗菌药物是目前临床应用最多、最广泛的药物,部分医师对抗菌药物的药效学和药动学知识存在欠缺,导致抗感染治疗中存在用药不合理问题[4];而临床药师通过发挥药学专业优势,协助医师优化药物治疗方案,同时开展药学监护,可提高临床疗效和减少药物不良反应。现将我院临床药师参与1例MOJ术后并发感染的治疗药学实践报道如下。
1 病例资料患者,女,56岁,体重62 kg,因“发现黄疸1月伴胆管包块半月余”入院。患者3月前无明显诱因出现上腹部疼痛不适,可耐受,未予特殊处理。2月前出现皮肤巩膜黄染,感恶心、间断呕吐,呕吐物为黄色液体,偶有腹泻,至当地医院治疗后,未见明显好转,为求进一步诊治于2017年4月13日收入我院普通外科治疗。既往史:20余年前曾行结扎手术;4年前行阑尾切除术,1年前行泌尿系结石取石术。长期不规律服用阿莫西林、头孢克洛预防尿路感染。入院检查:体温:37.1 ℃,心率:76次/分,呼吸:20次/分,血压:103/64 mmHg。巩膜皮肤黄染,腹部稍有膨隆。腹部CT可见:肝门区胆管癌并高位梗阻征象,慢性胆囊炎并胆囊底部息肉。辅助检查:白细胞计数(WBC):10.5×109/L,中性粒细胞百分率(N%):66.3%,降钙素原(PCT):0.1 μg·L-1,C反应蛋白(CRP):20.5 mg·L-1;血肌酐(SCr):76 μmol·L-1,尿素氮(BUN):4.9 mmol·L-1;丙氨酸氨基转移酶(ALT):67 U·L-1,天门冬酸氨基转移酶(AST):53 U·L-1,碱性磷酸酶(ALP):571 U·L-1,γ-谷氨酰转肽酶(γ-GGT):459 U·L-1,总胆红素(TBIL):160.4 μmol·L-1,直接胆红素(DBIL):106.5 μmol·L-1,间接胆红素(IDBIL):53.9 μmol·L-1。入院诊断:梗阻性黄疸,肝门区胆管癌并高位梗阻。
2 抗感染主要治疗过程患者完善相关辅助检查后,于2017年4月20日行经皮肝穿刺胆道引流术(PTCD),于2017年4月23日在全麻下行右半肝切除术+胆囊切除术+肝尾状叶部分切除术+胆管癌根治术。术后给予抗感染、保肝降酶、补液、抑酸护胃等对症支持治疗,其中抗感染是治疗的主要出发点,整个过程使用的抗菌药物包括头孢哌酮舒巴坦、头孢哌酮他唑巴坦、奥硝唑和莫西沙星。在给予1月余的抗感染治疗后,患者临床症状好转,辅助检查结果恢复至正常水平,生命体征平稳,给予出院。患者的抗感染治疗方案调整见表 1,整个治疗期间患者的辅助检查结果见表 2,引流液培养+药敏结果见表 3。
|
|
表 1 抗感染治疗方案调整情况 |
|
|
表 2 患者治疗期间辅助检查结果 |
|
|
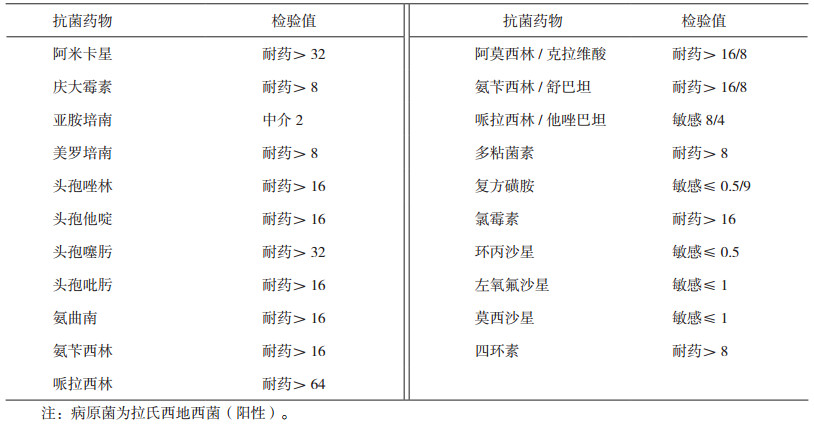
表 3 引流液培养病原菌及其药敏结果 |
胆道恶性肿瘤是诱发MOJ的重要病因之一[5],可引起包括肠道菌群移位、内毒素血症、免疫功能低下、体内酸碱失衡、肝细胞及其他细胞病变、肾功能损害及心肌功能障碍,对患者预后造成严重影响,甚至危及生命[6-7]。刘东义[8]在研究中表明:正常情况下胆道系统是无菌的,不会出现感染症状;当胆道梗阻时,胆汁不能正常分泌进入肠道,胆汁的缺乏引起肠粘膜屏障功能下降,寄生于肠道内的细菌及其毒素,越过肠粘膜屏障大量侵入肠道以外的组织,这一过程称为“肠道菌群移位”,而细菌移位是造成胆系感染以及全身感染的重要原因;胆道梗阻后,肝脏的免疫屏障功能受损,Kupffer细胞滤过入肝血流、清除其中大分子物质、免疫复合物以及细菌等功能受损,吞噬功能降低,失去应有的免疫作用;而且血清胆红素水平升高会直接损害淋巴结的功能,降低T细胞介导的免疫功能。夏卿等[9]在对120例梗阻性黄疸患者术后研究表明:术前黄疸天数过长,术前碱性磷酸酶过高是造成术后胆道感染的高危因素。乔秀丽等[10]研究表明:PTCD等有创诊疗操作可导致肠道、皮肤或外界细菌进入胆道引起感染,引流术后奥狄氏括约肌失去作用,肠内容物逆流易引起细菌感染,是胆道感染的首要独立危险因素。该患者入院诊断为MOJ,术前黄疸长达2月余伴碱性磷酸酶高,第一次行PTCD,第二次术后出现发热,血象中的感染指标较高,考虑合并胆系感染,因此需经验性抗感染治疗。胡逸群等[11]在对106例MOJ合并胆系感染的患者研究中表明:其胆汁培养阳性率为49.1%,最主要的致病菌为大肠埃希氏菌,其次分别为肺炎克雷伯菌、阴沟肠杆菌,针对革兰氏阴性菌可选用敏感性较高的头孢哌酮舒巴坦。《抗微生物治疗指南》(第46版)[12]推荐:对于继发于肿瘤、结石、狭窄的不完全性梗阻,胆汁培养的阳性率可达40%~60%,最主要的致病菌为肠杆菌科细菌,其次分别为肠球菌、拟杆菌、梭状芽胞杆菌属等;推荐的抗菌药物包括:哌拉西林他唑巴坦或氨苄西林舒巴坦、第三代头孢菌素+甲硝唑、氨曲南+甲硝唑、环丙沙星+甲硝唑、莫西沙星。综合分析,临床药师考虑初始应经验性选用可覆盖革兰氏阴性菌和厌氧菌的药物,单用头孢哌酮舒巴坦合理但欠妥,应联合使用硝基咪唑类。
3.2 感染复发后的治疗方案分析MOJ患者胆红素和内毒素进入体循环引起的高胆红素血症和内毒素血症易诱发胆系感染以及脓毒血症,导致患者免疫力低下,进而使胆系感染反复发生[13]。5月10日(第二次术后17天),患者诉间断发热,体温最高达38.2 ℃,发热时伴畏寒和寒战,大汗淋漓,血象中的感染指标较高,考虑出现了胆道再次感染征象。由于手术对患者打击较大,且该患者免疫功能低下,术后出现反复感染,且有长期不规律服用抗菌药物用药史,考虑出现条件致病菌甚至耐药菌感染的可能性较大。由于内毒素血症及革兰氏阴性菌败血症所致的多脏器功能衰竭是梗阻性黄疸并发症发生率及死亡率高的主要原因[8],因此临床药师考虑在病原菌未明确的情况下,采用降阶梯治疗策略:首先选用广谱、强效抗菌药物覆盖所有可能导致感染的病原菌;用药5天后,待病情得到控制,根据病原学结果结合先前的治疗效果,将经验性治疗调整为目标性治疗[14-15],建议给予美罗培南(1.0 g,Q 8 h,静脉滴注),给药前取血培养和引流液培养。医师未采纳,调整治疗方案为头孢哌酮舒巴坦(3.0 g,Q 8 h,静脉滴注)联合奥硝唑(0.5 g,Q12h,静脉滴注)。在治疗5天后,患者临床表现未见明显好转,提示抗感染治疗不佳。
3.3 明确病原学结果的治疗方案分析5月15日(第二次术后22天),患者仍诉发热,且引流液培养结果显示:拉氏西地西菌(阳性)。有关拉氏西地西菌感染在临床治疗中的报道甚少,在我院腹腔引流液中检出属于首次。熊祝嘉等[16]报道:西地西菌属包括戴氏西地西菌、奈氏西地西菌、拉氏西地细菌,属于发酵的革兰氏阴性杆菌和兼性厌氧菌。目前痰液和血液是检出西地西菌的主要来源,其他来源包括胆囊、手伤口和眼分泌物。西地西菌被认为是环境中正常存在的菌群,属于条件致病菌,其易感人群为免疫功能受到抑制的个体。该患者属于肿瘤患者,免疫功能低下,很容易发生条件致病菌感染。临床药师考虑该病原菌为致病菌的可能性较大。患者长期留置引流管,不排除有葡萄球菌、粪肠球菌、链球菌等革兰氏阳性菌混合感染的可能,而患者在先前的治疗过程中,均未使用可覆盖革兰氏阳性球菌的药物。临床药师根据药敏结果,建议选用亚胺培南单药治疗或头孢哌酮他唑巴坦联合莫西沙星治疗。临床医师采纳第二条治疗方案。在施行该方案8天后,患者体温及血象中的感染指标恢复至正常,复查引流液培养阴性,临床药师考虑抗感染基本控制,且患者整个抗菌药物使用周期为一个月,为减少耐药和不良反应的发生,建议停用抗菌药物,临床医师采纳。
3.4 临床药师的药物监护头孢哌酮大部分经过胆道排泄,舒巴坦和他唑巴坦大部分通过肾脏排泄,因此治疗期间需密切监测患者的肝、肾功能。头孢哌酮舒巴坦和头孢哌酮他唑巴坦均属于时间依赖性抗菌药物,其抗菌活性与两次给药时间间隔内血药浓度大于最低抑菌浓度的时间占比相关,即T%>MIC。当T%超过60%~70%时,可发挥出最大的杀菌活性[17]。Wang等[18]研究表明:头孢哌酮舒巴坦可将输注时间延长至3小时。辛栋轶[19]通过对头孢哌酮舒巴坦在不同给药方案中的临床疗效和药物经济学的研究中表明:按1.5 g,Q 6 h,静脉滴注组与3.0 g,Q 8 h,静脉滴注组的给药方案对比,两组T%>MIC的值接近,且前者治疗费用较低。因此,在初始治疗中,临床药师建议将用法用量调整为1.5 g,Q 6 h,静脉滴注,同时延长输注时间。患者免疫功能低下,治疗期间抗菌药物应用周期较长,是发生抗菌药物相关性腹泻的高危人群[20],临床药师建议加用微生态制剂双歧杆菌乳杆菌三联活菌胶囊维持肠道菌群平衡,告知患者用温开水送服,与抗菌药物应间隔3小时左右服用。莫西沙星属于氟喹诺酮类抗菌药物,其肝酶升高超过5倍正常值是其使用的禁忌。提示临床医师用药期间需密切监测患者的肝功能,同时提示护士需避光静脉输注,且时间不得少于90分钟。
4 小结临床药师在对该患者整个抗感染治疗过程中,首先分析了经验性单用头孢哌酮舒巴坦的欠妥之处;其次,针对胆道反复的感染,分析了存在条件致病菌甚至耐药菌的可能性较大,在未明确病原菌之前,需考虑以碳青酶烯类为首选的降阶梯治疗策略,在病原学结果明确之后,需依据药敏结果并结合先前的治疗效果调整用药方案;再次,通过临床药师在整个治疗过程中实施药学监护,不仅可以提高临床治疗效果,而且减少了不良反应的发生率。通过临床药师深入临床一线,充分发挥自身专业技术优势,协助医师制定治疗方案,使患者获得最大收益,还可使临床药师逐步得到临床医师的认可。
| [1] |
宋勇, 秦高平, 杜立学, 等. 胆道支架联合PTCD对恶性梗阻性黄疸患者肝功能与生活质量的影响研究[J]. 肝胆外科杂志, 2017, 25(2): 118-122. |
| [2] |
Ho CS, Warkentin AE. Evidence-based Decompression in Malignant Biliary Obstruction[J]. Korean J Radiol, 2012, 13(Suppl 1): 56-61. DOI:10.3348/kjr.2012.13.S1.S56 |
| [3] |
刘承利, 张辉, 王成, 等. 免疫营养素对恶性梗阻性黄疸胆道支架植入术后感染发生率的影响[J]. 现代生物医学进展, 2017, 17(5): 882-885. |
| [4] |
唐毅敏, 赵敏. 药师参与会诊指导感染性疾病合理用药及其病例汇总分析[J]. 实用医药杂志, 2017, 34(3): 240-243. |
| [5] |
Lacono C, Ruzzenente A, Campagnaro T, et al. Role of Preoperative Biliary Drainage in Jaundiced Patients Who are Candidates for Pancreatoduodenectomy or Hepatic Resection:Highlights and Drawbacks[J]. Ann Surg, 2013, 257(2): 191-204. DOI:10.1097/SLA.0b013e31826f4b0e |
| [6] |
何雄伟. 超声引导下经皮肝胆道穿刺引流术治疗梗阻性黄疸的应用价值[J]. 中国实用医药, 2016, 11(33): 73-74. |
| [7] |
申瑞田. 超声引导下经皮肝胆道穿刺引流术治疗梗阻性黄疸的临床应用价值[J]. 实用医技杂志, 2017, 24(5): 487-488. |
| [8] |
刘东义. 梗阻性黄疸胆汁细菌学特点的临床分析[D]. 山东: 山东大学, 2011. http://cdmd.cnki.com.cn/article/cdmd-10422-1011226449.htm
|
| [9] |
夏卿, 周新锋, 范晓翔, 等. 梗阻性黄疸患者经皮经肝胆道引流术后胆道感染相关因素研究[J]. 中华医院感染学杂志, 2017, 27(17): 3960-3963. |
| [10] |
乔秀丽, 宋文冲, 李爱君, 等. 晚期恶性梗阻性黄疸支架置入术后感染的病原学分析[J]. 实用医学杂志, 2013, 29(10): 1603-1605. DOI:10.3969/j.issn.1006-5725.2013.10.024 |
| [11] |
胡逸群, 燕善军, 孙医学, 等. 恶性梗阻性黄疸合并胆系感染106例病原菌分布及相关因素分析[J]. 蚌埠医学院学报, 2017, 42(5): 612-615. |
| [12] |
范洪伟, 王焕玲, 周宝桐, 等. 抗微生物治疗指南(第46版)[M]. 北京: 中国协和医科大学出版社, 2017: 17.
|
| [13] |
胡逸群, 燕善军. 恶性梗阻性黄疸合并胆系感染研究现状和进展[J]. 胃肠病学, 2016, 21(4): 247-249. |
| [14] |
Montero JG, Pizarraya AG, Ortega AE, et al. Deescalation of Empirical Therapy is Associated with Lower Mortality in Patients with Severe Sepsis and Septic Shock[J]. Intensive Care Med, 2014, 40: 32-40. DOI:10.1007/s00134-013-3077-7 |
| [15] |
刘慧招. 亚胺培南/西司他丁对重症肺炎的降阶梯治疗疗效分析[J]. 中外医疗, 2016, 14(5): 162-164. |
| [16] |
熊祝嘉, 李小瑛, 王晓岩. 尿液中检出戴氏西地西菌1例[J]. 中国医药导报, 2011, 8(30): 192. DOI:10.3969/j.issn.1673-7210.2011.30.083 |
| [17] |
Drusano GL. Antimicrobial Pharmacodynamics:Critical Interactions of "Bug and Drug"[J]. MICROBIOLOGY, 2004, 2(4): 289-290. |
| [18] |
WANG Q, WU Y X, CHEN B Y, et al. Drug Concentrations in the Serum and Cerebrospinal Fluid of Patients Treated with Cefoperazone/sulbactam after Craniotomy[J]. BMC Anesthesiol, 2015, 15(1): 1-8. DOI:10.1186/1471-2253-15-1 |
| [19] |
辛栋轶, 林峰, 谢觉醒, 等. 头孢哌酮舒巴坦钠不同给药方案的疗效和经济学评价[J]. 中国现代应用药学, 2016, 33(1): 111-114. |
| [20] |
Elseviers M, Van CY, Nayaert S, et al. Prevalence and Management of Antibiotic Associated Diarrhea in General Hospitals[J]. Infectious Diseases, 2015, 15(129): 1-9. |
 2018, Vol. 32
2018, Vol. 32