独一味是重要的青藏高原药用植物和常用大宗藏药,是唇形科独一味属植物(Lamiophlomis rotata Benth Kudo)的干燥地上部分,收载于《中国药典》2015年版一部中,主产于西藏、青海、甘肃、四川西部及云南西北部,生于海拔2700~4500米的高原或高山上强度风化的碎石滩中或石质高山草甸、河滩地。独一味性甘、苦、平,归肝经;具有活血止血、祛风止痛的作用,用于跌打损伤、外伤出血、风湿痹痛、黄水病[1-2]。
独一味的化学成分研究始于20世纪80年代,具有特征性的化合物主要包括环烯醚萜苷类、黄酮类、苯乙醇苷类[3-4]。现代药理实验表明,独一味中的环烯醚萜苷和苯乙醇苷类成分具有抗炎和镇痛活性[5-7];黄酮类成分具有抗炎、抗菌等作用[8-9]。独一味的含量测定有一些报道[10-13],液质联用分析报道较少[14-15]。
本研究色谱条件在《中国药典》2015年版一部独一味【含量测定】节下液相条件基础上优化而成,采用UPLC-ESI-TOF MS技术对独一味中多种成分进行分离鉴定,该法操作简便、快速、准确,为独一味的药效物质基础及质量控制提供参考。
1 仪器与材料沃特世H-CLASS型液相色谱仪,包括在线脱气机,二元泵,自动进样器,柱温箱;沃特世SYNAPT G2-S TOF MS质谱仪,配有电喷雾离子源(ESI),Masslynx液质工作站;赛多利斯十万分之一电子天平;KQ-300DA型超声清洗仪(昆山市超声仪器有限公司);ACQUITY UPLC HSS T3色谱柱(填料:十八烷基键合硅胶,2.1 mm×100 mm,1.8 μm;Waters公司)。
独一味样品来自2015年国家药品抽验计划,经中国食品药品检定研究院中药民族药检定所民族药室鉴定为唇形科独一味属植物(Lamiophlomis rotata Benth Kudo)的干燥地上部分。甲醇、乙腈、甲酸均为HPLC级(Fisher公司,USA),水为Milli-Q纯化水。
2 色谱及质谱条件 2.1 色谱条件Waters ACQUITY UPLC HSS T3色谱柱(2.1 mm×100 mm,1.8 μm);乙腈为流动相A,0.05%甲酸水溶液为流动相B,按如下比例进行梯度洗脱:0~4 min,9%A;4~12 min,9%→18%A;12~15 min,18%A;流速0.3 mL·min-1,检测,进样量1 μL,柱温为30℃。
2.2 质谱条件正离子模式,capillary 3.00 kV,sampling cone 35 V,source offset 80 V, source temperature 110℃,desolvation temperature 400℃,cone gas flow 50 L·h-1,desolvation gas flow 1000 L·h-1,Nebuliser 6.0 bar,扫描范围100~1000 m/z。
3 溶液的制备 3.1 对照品溶液的制备取山栀苷甲酯、8-O-乙酰山栀苷甲酯、绿原酸、连翘酯苷B、芦丁、马钱苷、木犀草苷、毛蕊花糖苷、木犀草素、槲皮素对照品适量,精密称定,加甲醇分别制成约40 μg·mL-1的对照品溶液。
3.2 供试品溶液的制备取粉末(过三号筛)约0.6 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定质量,加热回流1 h,放冷,再称定质量,以70%甲醇补足减失的质量、摇匀、滤过,精密量取续滤液2 mL,置10 mL容量瓶中,加甲醇至刻度、摇匀、滤过,取续滤液,即得。
4 结果与讨论 4.1 提取方法的选择提取方法参考《中国药典》2015年版一部独一味含量测定节下进行,目的在于对《中国药典》含量测定所得到的HPLC色谱图上的色谱峰进行鉴定,以明确其化学成分。
4.2 试验条件的优化液相色谱条件参考《中国药典》2015年版一部独一味节下【含量测定】项目的液相色谱条件,优化后进行。为加强质谱对化合物的响应灵敏度,在水相中添加0.05%甲酸。由于本试验采用的是超高压液相色谱柱,采用沃特世液相色谱公司提供的HPLC和UPLC色谱条件转换软件进行转换,流速降低为0.3 mL·min-1,进样量降低为1 μL。
质谱检测分别比较了正、负离子两种扫描模式,结果发现正离子模式下峰容量更大、质谱响应更强,故试验最终选择在正离子模式下进行。
4.3 独一味中主要化学成分的鉴定在优化的色谱条件下,独一味提取液的UPLCESI-TOF MS基峰色谱图(BPI)见图 1。通过对照品比对确定10个化合物,其余化合物通过如下方法确定,共鉴定30个色谱峰,包括环烯醚萜苷类、黄酮类和苯丙素类。无对照品的化合物按照以下方法鉴定:首先,根据TOF MS上所得到的精确化合物分子量信息,通过工作站自带的元素组成软件在5 ppm以内的质量偏差范围内计算其可能的元素组成,检索独一味中化学成分报道,对其进行初步鉴定,锁定1至数个化学成分,再结合出峰顺序以及质谱碎片信息,进一步推测其结构,初步确证了30个峰,结果见表 1。
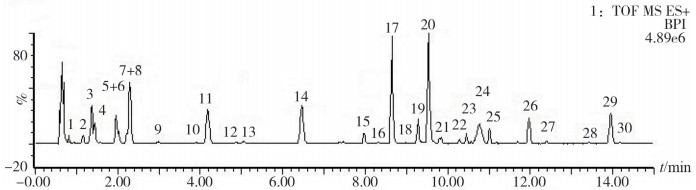
|
图 1 独一味正离子模式下UPLC-Q-TOF MS全扫描Base Peak色谱图 |
|
|
表 1 独一味中UPLC-ESI-TOF MS鉴定的化合物 |
化合物17的保留时间为8.65 min,其准分子离子峰为m/z 471.1477 [M+Na]+,可推断其分子式可能为C19H28O13,误差为-0.42 ppm。在进一步的质谱裂解过程中,其准分子离子峰脱掉一分子的乙酸形成特征碎片离子m/z 411.1265[M+Na-CH3COOH]+,再脱去一分子水、葡萄糖和钠形成特征碎片离子m/z 209.0815[M+H-C6H10O5-CH3COOH-H2O]+,再脱去一分子水或一分子甲醇形成特征碎片离子m/z 191.0708[M+H-C6H10O5-CH3COOH-2H2O]+和m/z177.0553[M+H-C6H10O5-CH3COOH-H2O-CH3OH]+。查阅相关文献[15],其与8-O-乙酰山栀苷甲酯的主要裂解特征一致,并且经对照品比对,故确定化合物17为8-O-乙酰山栀苷甲酯,质谱图及裂解方式见图 2和图 3。
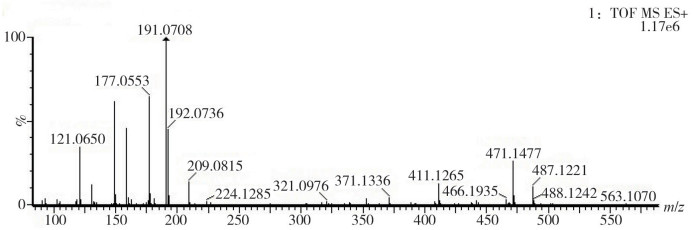
|
图 2 8-O-乙酰山栀苷甲酯质谱图 |
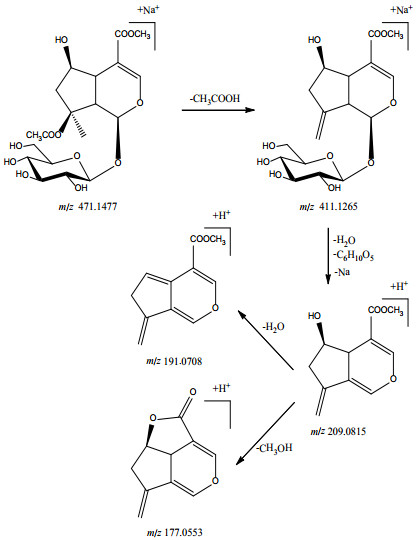
|
图 3 8-O-乙酰山栀苷甲酯裂解途径 |
化合物19的保留时间为9.27 min,其准分子离子峰为m/z 449.1099 [M+H]+,可推断其分子式可能为C21H20O11,误差为3.34 ppm。在进一步的质谱裂解过程中,其准分子离子峰脱掉一分子的葡萄糖形成特征碎片离子m/z 287.0551 [M+H-C6H10O5]+。查阅相关文献[16],其与木犀草苷的主要裂解特征一致,并且经对照品比对,故确定化合物19为木犀草苷。
化合物20的保留时间为9.85 min,其准分子离子峰为m/z 625.2578 [M+H]+,可推断其分子式可能为C29H36O15,误差为0.64 ppm。在进一步的质谱裂解过程中,其准分子离子峰脱掉一分子的鼠李糖形成特征碎片离子m/z 465.1021[M+H-C6H10O4]+,脱掉一分子的葡萄糖形成特征碎片离子m/z 303.0491[M+H-C6H10O4-C6H10O5]+。查阅相关文献[17],其与毛蕊花糖苷的主要裂解特征一致,并且经对照品比对,故确定化合物20为毛蕊花糖苷。
5 结论本试验采用UPLC-ESI-TOF MS技术,通过对照品比对和质谱碎片分析,实现了对藏药独一味中主要成分的快速定性分析,初步鉴定出30个独一味中的主要环烯醚萜苷、黄酮类和苯丙素类成分。该方法快速、灵敏、准确度高,并且液相条件参照《中国药典》2015年版一部独一味【含量测定】节下确定,对独一味及其制剂的质量控制和监管提供科学依据,同时为其他藏药的化学成分快速分析提供参考。
| [1] |
中国科学院中国植物志编辑委员会. 中国植物志:第65卷第2分册[M]. 北京: 科学出版社, 1989: 480.
|
| [2] |
中国药典: 一部[S]. 2015: 262.
|
| [3] |
沈建伟, 王锐娟, 王环, 等. 藏药独一味的研究进展[J]. 安徽农业科学, 2008, 36(5): 1920-1922. |
| [4] |
张娟红, 徐丽婷, 王荣, 等. 藏药独一味生药学及化学成分研究进展[J]. 兰州大学学报:医学版, 2015, 41(5): 57-62. |
| [5] |
郑亚男, 杜文杰, 尹雪霏, 等. 独一味不同有效部位抗炎镇痛作用比较[J]. 时珍国医国药, 2015(2): 282-284. |
| [6] |
朱斌, 龚念, 彭崇胜, 等. 独一味镇痛作用及其有效成分研究[J]. 中国药理学与毒理学杂志, 2012, 26(3): 442-446. |
| [7] |
白蓉, 郭延伟. 独一味中苯乙醇苷提取物的镇痛抗炎作用及毒性研究[J]. 华西药学杂志, 2015, 30(3): 384-385. |
| [8] |
纪兰菊, 冯丽娟, 李生萍, 等. 藏药独一味药材中不同部位木犀草素和总黄酮含量的分析[J]. 分析实验室, 2007, 26(增刊): 101-103. |
| [9] |
林天慕, 官清香, 张三奇, 等. 大孔吸附树脂分离纯化独一味总黄酮的研究[J]. 中国药学杂志, 2005, 40(4): 264-267. |
| [10] |
钟世红, 古锐, 王铃鑫, 等. HPLC法同时测定独一味中的7种成分含量[J]. 中国中药杂志, 2014, 39(22): 4373-4378. |
| [11] |
樊鹏程, 李茂星, 贾正平, 等. RP-HPLC同时测定不同产地独一味药材中4种环烯醚萜苷[J]. 中草药, 2010, 41(3): 483-485. |
| [12] |
李茂星, 张超, 乌兰, 等. 独一味、螃蟹甲、糙苏和萝卜秦艽中5个环烯醚萜苷的含量测定[J]. 中药材, 2011, 34(1): 727-729. |
| [13] |
昝珂, 焦兴苹, 过立农, 等. 藏药独一味及其伪品HPLC特征图谱和4种成分含量测定[J]. 中国中药杂志, 2016, 41(12): 2284-2290. |
| [14] |
Wu L, Li L, Wang M, et al. Target and Non-target Identification of Chemical Components in Lamiophlomis totata by LC-Q-TOF/MS Using a Three-step Protocol[J]. Rapid Commun Mass Spectrom, 2016, 30(19): 2145-2154. DOI:10.1002/rcm.7695 |
| [15] |
La M, Zhang F, Gao S, et al. Constituent Analysis and Quality Control of Lamiophlomis Rotate by LC-TOF/MS and HPLC-UV[J]. J Pharm Biomed Anal, 2015, 102: 366-376. DOI:10.1016/j.jpba.2014.09.038 |
| [16] |
Sun H, Liu M, Jiang Z, et al. Comprehensive Identification of 125 Multifarious Constituents in Shuang-huang-lian Powder Injection Power Injection by HPLC-DAD-ESⅡT-TOF-MS[J]. J Pharm Biomed Anal, 2015, 115: 86-106. DOI:10.1016/j.jpba.2015.06.013 |
| [17] |
Amessisouchemoukh N, Abureidah IM, Quirantespine R, et al. Tentative Characterisation of Iridoids, Phenylethanoid Glycosides and Flavonoid Derivatives from Globularia alypum L. (Globulariaceae) Leaves by LC-ESI-QTOF-MS[J]. Phytochem Anal, 2014, 25(5): 389-398. DOI:10.1002/pca.v25.5 |
 2018, Vol. 32
2018, Vol. 32 
 ,
, 