2. 济南大成医药发展有限公司, 济南 250100
2. Jinan Dachpharm Development Co., Ltd., Jinan 250100, China
药品是关系到人类健康的特殊商品,不仅要求质量合格、有效,更重要的是必须安全可靠[1-3]。而安全性评价的最关键指标就是其不良反应(adverse drug reaction,ADR)发生的频率和严重程度,因此,我国药品监督管理部门设立了强制性ADR监测和报告制度[4]。由2010-2013年间国家ADR监测年度报告可知,目前报告来源主要还是医疗机构,其报告ADR数约占报告总数的80%,确保药品质量的生产及经营企业报告数约18%,个人报告仅为2%左右[4-6]。然而,患者是药品的直接使用者及ADR发现的第一人,因此,患者直接报告ADR能促使药品安全性风险的更早发现,作为一种日益重要的报告来源,这种报告形式正逐渐引起各国的广泛关注和探索应用[7]。当下患者最易寻求企业帮助的途径就是药品包装上的联系电话,因此,本研究采取抽样调查方法,随机选取了500家药品生产企业,通过拨打其产品包装上的联系电话,对企业受理患者申报ADR现状进行深入考察,探究其中可能存在的困难和问题并提出相应改进措施和建议。
1 资料与方法 1.1 被调查对象的基本情况随机搜集500家医药企业产品外包装上的联系电话,包括:①国有或国有控股企业:11家为资产总值超过40000万的大型企业(占35.5%),7家为资产总值少于4000万的小型企业(占22.6%);②外资企业:中外合资37家(占3 7.4 %),外方独资15家(占15.2%),台港澳投资43家(占43.4%);其中,27家为大型医药企业(占27.3%);③其他性质企业:既有民营的,也有自然人(非自然人)投资或控股的企业;其中,42家为大型医药企业(占11.4%),152家为小型医药企业(占41.1%)。
1.2 调查方法问卷调查表内容主要涉及ADR相关事务,包括是否设有ADR专线、接线人员是否受过ADR相关知识培训、平均每月接听到多少有关ADR咨询或投诉电话、是否主动跟踪患者反馈信息等。拨打企业联系电话,按照问卷内容,对接听人员进行调查,未接通电话均为不同时间拨打2次以上,以确定无人接听。然后,对相关数据进行整理、分析。
2 结果 2.1 企业接听电话情况调研结果显示,仅有23%的企业(115家)产品上的电话号码有人接听,但其中还有32家企业在电话接通后,转为自动语音并一直无人接听,有的听到是进行问卷调查就直接挂断。因此,真正配合调查的企业只占到17%。其次,75%的企业标注在包装上的电话号码形同虚设,调查人员在不同时间段拨打多次,均无人接听。更令人吃惊的是7家企业的联系方式竟然是空号,作为消费者最直接、最重要与企业进行交流的渠道竟然如此不畅通。
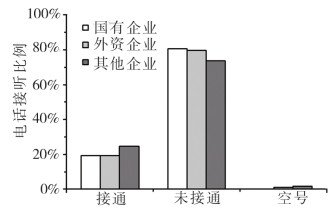
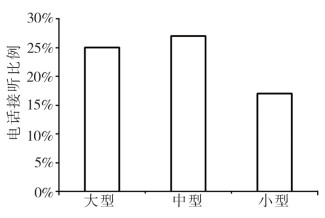
按照企业类型和规模的不同,分别对上述情况做了进一步分析,见图 1、图 2。结果发现,企业类型在电话接通比率上并无显著性差异,只是其他类型企业的电话接通率略高于国企和外资企业。相对而言,企业规模对于电话接通率影响比较明显,尽管都不是很高,但大中型企业的电话接通率明显高于小型企业。
|
图 1 不同类型企业接听电话情况 |
|
图 2 不同规模企业接通电话情况 |
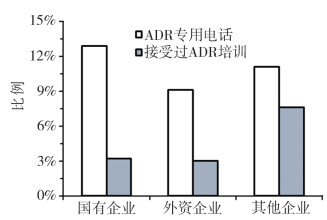
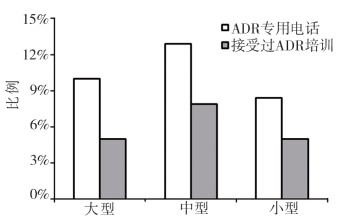
根据对接通电话企业人员进一步的调查,绘制了不同类型和不同规模企业ADR培训等相关信息(见图 3、图 4)。从图中可看出,不论企业是何种类型和规模,开设ADR专线的比率都极低(均小于15%)。进一步比较不同类型和规模企业开设专线情况发现,国有企业和中型医药企业开设ADR专线比例相对较高。
|
图 3 不同类型企业ADR培训相关信息 |
|
图 4 不同规模企业ADR培训相关信息 |
从图 3、图 4还可看出,不论企业是何种类型和规模,对于接线员进行ADR相关信息培训的比率都很低(均小于10%)。进一步比较不同类型和规模企业对接线员培训情况发现,其他类型企业和中型医药企业相对比较重视对接线员工的ADR相关知识培训。本课题组还询问了企业接听消费者咨询或反映ADR问题的频率,对于这一问题,所有企业的答案很统一:很少或极少接到消费者此类电话,1个月平均只有1~3次。
3 讨论 3.1 企业监测ADR存在的问题从上述情况可知,大部分被调查的药品生产企业对于包装上的联系方式很不重视,近80%企业公布的联系电话竟然都无人接听,其中既有国外知名的在华合资企业,也有资产过几十亿的超大型医药企业,甚至不乏老百姓耳熟能详的企业名称。然而,这一渠道是企业从消费者获取信息特别是ADR相关信息最直接、最有效的途径,充分反映出药品生产企业对公众用药安全的重视程度不够,这应该也是ADR上报数据中极少来自于生产企业的原因之一[8-9]。同时,7家企业包装上的空号问题,从另一个侧面反映出企业对该渠道搜集药品信息的忽视。此外,调查结果显示,较大比例的电话接听人员没有经过ADR相关知识培训,因此,有理由相信即便遇到消费者咨询相关问题时,工作人员因知识储备不足,也无法给消费者满意的答复,进而严重挫伤了消费者与企业间信息交流的积极性。
3.2 患者ADR报告存在的问题随着社会的进步,环境污染问题越来越严重,人类患病机会随之扩大,药品的用量也逐年增加。然而,药品是一种特殊商品,尽管ADR是其无法避免的内在属性,但如果发现及时还是可以把伤害降到最低[10]。由本项目调查数据可知,企业每年接到患者ADR报告或咨询电话的案例极少,是因为ADR发生很少吗?事实恰恰相反,有数据显示,我国每年有高于500万人次的患者因ADR而住院,其中死亡人数高达19.2万人[11]。因此,这一现象的出现主要是因为绝大多数患者对于判断何种症状属于ADR,缺乏必要的知识储备及咨询途径[12],即便身体出现不适,要么自行停药,要么直接去医院看医生。
3.3 促进药品生产企业与消费者间ADR信息报告的建议及措施1)尽快建立国家药害事故补偿机制:由国家发起建立基金,各药品生产企业按年销售额的一定比例提取ADR基金,用于受害者的救治。只有建立了补偿机制,明确生产企业在救济中的责任,才能减少药品生产企业的后顾之忧,积极搜集并上报ADR信息。进而提高ADR报告的质量,避免ADR的重复发生,使患者减少不必要的痛苦,促进临床合理用药[13-14]。同时,我国应当重视并建立个人ADR报告系统,增加相应措施来引导和鼓励公众报告ADR。
2)企业应积极构建与患者之间更通畅的交流渠道:首先,确保产品包装上联系方式的真实有效性;其次,建议企业在外包装(或说明书)上增加一项企业用于搜集产品ADR信息的网址,从而提高企业收集ADR信息的效率;同时,在说明书中尽可能多地提供有关ADR的相关信息[15-16],因为说明书是距离患者最近的不会说话的专家。此外,必须加强相关人员ADR知识培训,对于消费者反映的问题能够及时有效地回答,使其获得满意的信息,确保用药安全有效。
3)加强对患者ADR相关知识的宣传教育:患者是承担ADR风险的主体,患者自身的ADR报告对于ADR警戒有着重要作用,因此,可以通过印发ADR相关资料、举办专题讲座和培训班,以及鼓励自学等形式提高公众用药安全意识,使其能主动参与到ADR的监测中来。政府相关部门必须监督ADR法规的执行,充分调动生产企业积极性,减少漏报或瞒报现象,为保护患者用药的安全有效做出更大努力。
4 结论近年来,越来越多的ADR问题不仅给患者本人造成伤害,也给国家带来巨大的损失。因此,加强ADR监测工作非常重要。本项研究旨在通过调查药品包装上电话号码这一沟通途径的畅通性,为药品监管部门提供第一手资料,促使相关部门在制定ADR监管政策时能考虑到该环节的重要性,进一步完善相关制度。由于受到研究范围、时间及有效样本量等因素的限制,文中数据存在不足之处;但希望能为相关部门制定更有效、严格的ADR监管制度提供参考,从而更好地维护人民的身体健康。
| [1] |
巫俊强. 中国药品安全政府管制的现状、问题与对策[D]. 长春:吉林大学,2015.
|
| [2] |
王淑娟. 中国药品安全规制研究[D]. 沈阳:辽宁大学, 2010.
|
| [3] |
张甜甜. 关于完善药品不良反应监测的思考[J]. 中国当代医药, 2013, 20(24): 183,186. |
| [4] |
杨悦. 近年我国药品不良反应报告与监测总体情况分析[J]. 西北药学杂志, 2016, 31(3): 323-326. |
| [5] |
国家食品药品监督管理总局. 国家药品不良反应监测年度报告(2014年)[J]. 中国药物评价, 2015, 32(4): 252-256. |
| [6] |
张建华, 王清理, 孔蕊. 影响药物不良反应监测的因素探讨[J]. 中国现代药物应用, 2012, 6(13): 75-76. DOI:10.3969/j.issn.1673-9523.2012.13.062 |
| [7] |
李嘉伟. 药品不良反应个人报告系统构建及相关机制研究[D]. 广州:广东药学院,2015.
|
| [8] |
邵蓉, 唐吉锋. 我国药品不良反应监测体系实施效果评价[J]. 中国卫生政策研究, 2014, 7(8): 29-36. |
| [9] |
任彦润. 药品不良反应报告和监测管理办法的发展研究[D]. 郑州:郑州大学,2014.
|
| [10] |
张雪梅, 郭佳栋, 刘影, 等. 药品不良反应监测体系评估指标建立的研究[J]. 中国药事, 2017, 31(1): 107-111. |
| [11] |
李淑萍, 赵遵娥, 杨明娜. 药品不良反应与安全用药的特点探讨[J]. 中国现代药物应用, 2010(15): 136-137. DOI:10.3969/j.issn.1673-9523.2010.15.121 |
| [12] |
姜兵武, 陈新彤, 亓靖华, 等. 社区居民药学服务需求调查与分析[J]. 中国药事, 2017, 31(4): 430-434. |
| [13] |
黄登笑. 药品不良反应补偿体系研究[D]. 上海:上海交通大学,2011.
|
| [14] |
罗雪梅. 应借鉴国外经验完善我国基层不良反应监测体系建设[J]. 中国药业, 2014(10): 7-9. |
| [15] |
李名石, 任瑜, 杨悦. 美国药品说明书管理研究[J]. 中国药物警戒, 2014, 11(12): 739-742. |
| [16] |
戴菲菲. 网络环境下医患关系研究[D]. 广州:南方医科大学,2011.
|
 2018, Vol. 32
2018, Vol. 32 
