2. 中南大学药学院, 长沙 410013;
3. 中国食品药品检定研究院, 北京 100050
2. School of Pharmaceutical Sciences, Central South University, Changsha 410008, China;
3. National Institutes for Food and Drug Control, Beijing 100050, China
朱砂属于我国临床上使用较广泛的矿物类中药,可内服及外敷,常用于治疗失眠多梦、心悸易惊、癫痫发狂、疮疡肿毒等症状,具有清心镇惊、安神、明目、解毒的功效[1-3]。因此,朱砂常被用在中药成方制剂中,国家药品标准中收载的含有朱砂的中成药约有400种,《中国药典》(2015年版一部)[4]收载的含有朱砂的中成药有70个,其中9个品种采用朱砂包衣,4个品种的处方中朱砂名称为“朱砂粉”,3个品种未列入处方中,仅在制法中描述。近年来,由于我国已经开始在最主要的朱砂产区——贵州及湖南等地限制和禁止开采,从而导致国内辰砂矿石产出大幅减少,对药用天然朱砂的供应量有大幅影响。在这种情况下,市场上不断涌现出伪品朱砂,如用灰褐色或青褐色矿石小颗粒,外面涂以暗红色颜料染色冒充朱砂;用红砖粉、用化工染料大红粉与砂石粉伪作朱砂等,在扰乱药品市场有序监管的同时,也增加了人民的用药安全风险[5-8]。
针对朱砂存在染色问题而又缺乏相关检测标准的情况,本文研究并建立了朱砂饮片中颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73的检测方法[9-13],对2015年国家药品计划抽验中收集的68批样品进行检测,发现12批样品中能检出808猩红[14-15]、颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73等6种色素,占样品总量的17.8%,其中8批样品中能检出新发现的颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73等5种色素。本文通过对朱砂样本进行检验,证明本研究建立的方法可有效地应用于朱砂药材中非法添加颜料红531、颜料红571、酸性红73、偶氮玉红、胭脂红成分的鉴别。
1 试验材料 1.1 实验仪器Waters 2695液相色谱系统(996PDA检测器);Agilent 1200- 6410B Triple Quad液-质联用系统;Mettler AE240型电子天平(梅特勒-托利多仪器有限公司);KQ3200DB型数控超声波清洗器(昆山市超声仪器有限公司);Milli-Q超纯水器(美国Millipore公司)。
1.2 试剂与药品酸性红73(批号:16675),购自Accustandard;胭脂红(批号:20070828),购自天津市化学试剂研究所;偶氮玉红(批号:30107),购自Dr.Ehrenstorfer GmbH;颜料红571(批号:Z050G005),购自CNW;颜料红531(批号:R342G005),购自CNW;乙腈为色谱纯购自Fisher Chemical公司;正丁醇、冰乙酸、乙醇、甲醇、甲酸、醋酸铵等为分析纯均购自北京化工厂;硅胶G板购自merck公司;其他试剂均为分析纯。
朱砂样本:包括朱砂药材和饮片,共计68批,来源于市场抽检样品。
2 试验方法与结果 2.1 薄层色谱法取本品粉末0.1 g,加70%乙醇25 mL,超声处理20 min,滤过,取续滤液作为供试品溶液。另取颜料红531对照试剂、颜料红571对照试剂、偶氮玉红对照试剂、胭脂红对照试剂、酸性红73对照试剂,加70%乙醇制成每1 mL各含0.2 mg的混合溶液,作为对照品溶液。按照薄层色谱法《中国药典》(2015年版四部)通则0502试验程序,吸取上述溶液5~10μL,分别点于同一硅胶G薄层板上,以正丁醇-乙醇-冰乙酸-水(8:4:2:2)为展开剂,展开,取出,晾干。供试品色谱中,在与对照品色谱相应的位置上,不得显相同颜色的斑点;若出现与对照品相同颜色的斑点,则采用下列高效液相色谱法验证。
1)初筛取样品1~68及混合对照试剂,分别按上述方法试验。
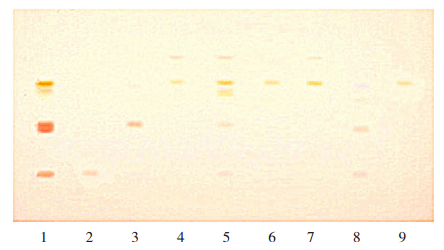
2)复筛取样品7、15、19、28、62、63、64、68及混合对照试剂,分别按上述方法试验,供试品溶液在与颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73的对照品溶液相应的位置上,有相同颜色的色谱斑点,结果如图 1所示。检测结果如表 2所示。
|
图 1 朱砂药材及饮片的薄层色谱 1. 5种色素对照试剂(从上往下:颜料红531,颜料红571,酸性红73,偶氮玉红,胭脂红);2.样品7;3.样品15;4.样品19;5.样品28;6.样品62;7.样品63;8.样品64;9.样品68。 |
采用Agilent TC-C18(4.6 mm×250 mm,5μm)色谱柱,填料:十八烷基硅烷键合硅胶;以乙腈为流动相A,以0.02 mol·L-1醋酸铵溶液为流动相B,按表 1进行梯度洗脱。检测波长:237 nm;流速1.0 mL·min-1,柱温30℃。理论板数按胭脂红色谱峰计算应不低于2000。
|
|
表 1 梯度洗脱程序 |
取颜料红531对照试剂、颜料红571对照试剂、偶氮玉红对照试剂、胭脂红对照试剂、酸性红73对照试剂适量,加70%乙醇制成每1 mL各含10μg的混合溶液,即得。
2.2.3 供试品溶液的制备取“2.1”节下的供试品溶液,即得。
2.2.4 阴性溶液的制备取朱砂阴性样品0.1 g,加70%乙醇制成每1 mL各含10μg的混合溶液,即得。
2.2.5 专属性检查精密吸取混合对照品溶液、供试品溶液及阴性样品溶液各10μL,在上述色谱条件下,分别注入色谱仪,得相应的色谱图。供试品在与颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73对照品相应的位置上,有相同保留时间的色谱峰,而阴性样品在与对照品相应位置上无色谱峰,说明阴性样品对颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73的检出无干扰。
2.2.6 仪器检出限取“2.2.2”节下的对照品溶液加乙醇稀释至颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73分别为1μg·mL-1,进样4μL,其信噪比为3:1,确定该浓度为仪器检出限。
2.2.7 耐用性试验取对照试剂、阴性样品、阳性样品溶液,按色谱条件,分别用OMNI BOND Hubble C18(4.6mm×250mm,5μm)、Aglient TC-C18(4.6mm×250mm,5μm)和Thermo Syncronis C18(4.6mm×250mm,5μm)3根不同型号的液相色谱柱进样测定,比较不同色谱柱对颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73保留时间的影响。3种色谱对颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73的保留时间没有影响,故其均可以作为色素分离的色谱柱。
2.2.8 测定法分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定。
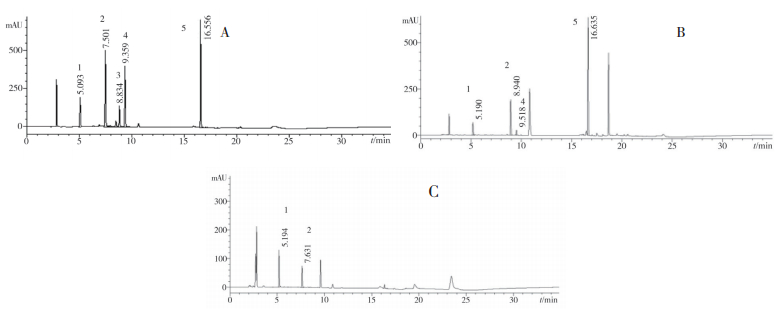
供试品色谱中,应不得出现与对照试剂色谱保留时间相同的色谱峰。若出现保留时间相同的色谱峰,则采用二极管阵列检测器比较相应色谱峰在210~650 nm波长范围的紫外-可见吸收光谱,吸收光谱应不相同;结果见表 2。同薄层色谱法检出结果一致。部分供试品及对照试剂的HPLC色谱图见图 2,UV光谱比对见图 3~7。
|
|
表 2 样品的检测结果 |
|
图 2 朱砂对照试剂及阳性样品HPLC色谱 A.混合对照品B.样品28;C.样品64;D.阳性对照;1.胭脂红;2.偶氮玉红;3.颜料红571;4.酸性红73;5.颜料红531。 |

|
图 3 胭脂红对照试剂及阳性样品UV色谱 A.胭脂红对照试剂;B.阳性样品。 |
|
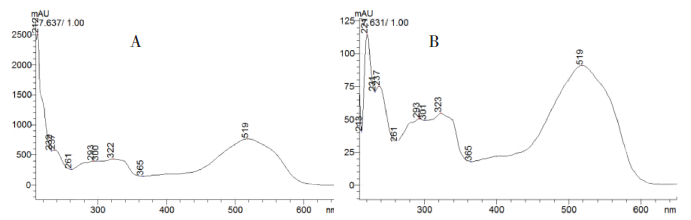
图 4 偶氮玉红对照试剂及阳性样品UV色谱 A.偶氮玉红对照试剂;B.阳性样品。 |

|
图 5 颜料红571对照试剂及阳性样品UV色谱 A.颜料红571对照试剂;B.阳性样品。 |

|
图 6 酸性红73对照试剂及阳性样品UV色谱 A.酸性红73对照试剂;B.阳性样品。 |
|
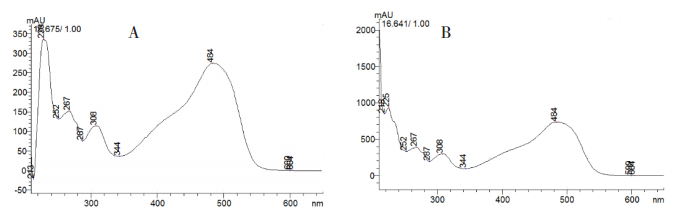
图 7 颜料红531对照试剂及阳性样品UV色谱 A.颜料红531对照试剂;B.阳性样品。 |
采用液-质联用(HPLC/MS)方法,对检测的颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73的色素及阳性样品进行进一步的确证,验证方法的准确性。
2.3.1 色谱条件和质谱检测参数色谱条件同上述高效液相色谱法;分流比约4:1。质谱检测参数:颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73分别以ESI-扫描,毛细管电压:4 kv,干燥气:氮气,干燥气温度:300℃,干燥气流速10 L·min-1,扫描范围:100~800 m/z。
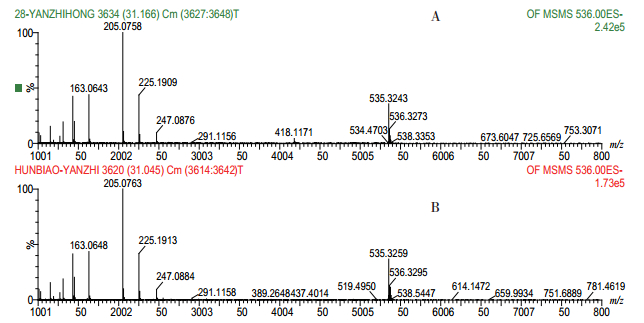
2.3.2 胭脂红的质谱特征ESI-扫描,胭脂红对照试剂,ESI-扫描一级质谱m/z 536,以m/z 536为母离子的二级质谱m/z 205、225;在阳性样品色谱中,在与胭脂红对照试剂相应保留时间色谱峰的质谱数据基本一致。见图 8。
|
图 8 胭脂红对照试剂及阳性样品ESI-二级质谱 A.胭脂红对照溶液;B.阳性样品。 |
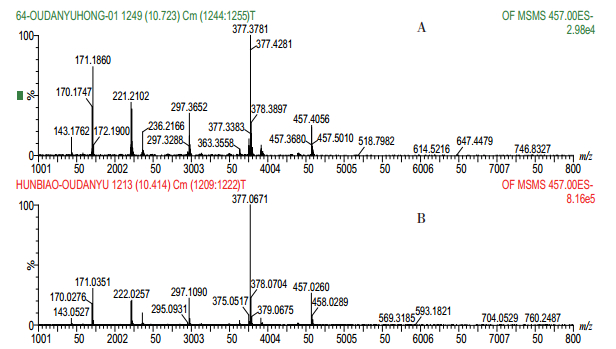
ESI-扫描,偶氮玉红对照试剂,ESI-扫描一级质谱m/z 457,以m/z 457为母离子的二级质谱m/z 377、171;在阳性样品色谱中,在与偶氮玉红对照试剂相应保留时间色谱峰的质谱数据基本一致。见图 9。
|
图 9 偶氮玉红对照试剂及阳性样品ESI-二级质谱 A.偶氮玉红对照溶液;B.阳性样品。 |
ESI-扫描,颜料红571对照试剂,ESI-扫描一级质谱m/z 387,以m/z 387为母离子的二级质谱m/z 187、170;在阳性样品色谱中,在与颜料红571对照试剂相应保留时间色谱峰的质谱数据基本一致。见图 10。

|
图 10 颜料红571对照试剂及阳性样品ESI-二级质谱 A.颜料红571对照溶液;B.阳性样品。 |
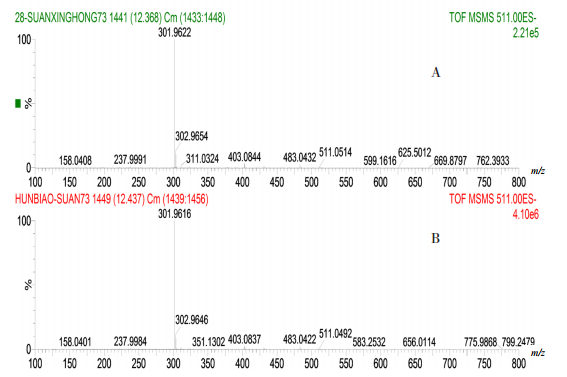
ESI-扫描,酸性红73的对照试剂,ESI-扫描一级质谱m/z 511,以m/z 327为母离子的二级质谱m/z 301、302;在阳性样品色谱中,在与酸性红73的对照试剂相应保留时间色谱峰的质谱数据基本一致。见图 11。
|
图 11 酸性红73对照试剂及阳性样品ESI-二级质谱 A.酸性红73对照溶液;B.阳性样品。 |
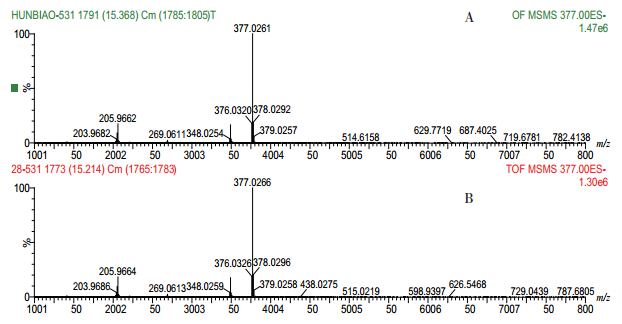
ESI-扫描,颜料红531对照试剂,ESI-扫描一级质谱m/z 377,以m/z 377为母离子的二级质谱m/z 205;348,在阳性样品色谱中,在与颜料红531对照试剂相应保留时间色谱峰的质谱数据基本一致。见图 12。
|
图 12 颜料红531对照试剂及阳性样品ESI-二级质谱 A.颜料红531对照溶液;B.阳性样品。 |
分别对颜料红531、颜料红571、偶氮玉红、胭脂红、酸性红73对照溶液进行紫外全波长扫描,最大吸收波长集中在480~510 nm处,但位于可见光区,为了方法的准确性与适用性,选择237 nm为检测波长,且该波长下各个对照品的吸收检测最佳,故最终选取237 nm为检测波长。
3.2 检测方法本方法建立拟用薄层色谱作为初筛,若筛出得到疑似的结果后可使用高效液相色谱和相应的色素对照品结合法来验证疑似品的结果,两者结果相一致时可得出阳性结论,必要时,可采用高效液相色谱-质谱联用方法加以验证。此方法可以补充检验朱砂药材中非法添加颜料红531、颜料红571、酸性红73、偶氮玉红、胭脂红5种色素。
3.3 朱砂样品检测所有试验样本均是从北京、成都、西安及湖南等地的中药饮片厂、中药材批发及零售等流通环节以及不同等级的医疗机构等收集,共计68批样品。其中,3批检出胭脂红,5批检出颜料红531,2批检出酸性红73,1批检出偶氮玉红,1批检出颜料红571。8批检出为阳性样品,均为饮片,其中2批来自医药公司,2批来自社会药房,4批来自医疗机构,样品染色率为11.8%,如果加上已有检出的9批(单一的为4批)含有猩红808的阳性样品,则朱砂的染色率为17.8%。朱砂来源于为硫化汞的天然矿石,自身就带有朱红色,检出染色朱砂色泽及饱和度均很高。市售朱砂饮片为了提高外观的色泽饱和度或者掩盖自身的质量问题而进行非法染色。因此,建议国家食品药品监督管理部门根据市场监督结果,将胭脂红、偶氮玉红、颜料红571、酸性红73、颜料红531的检测列入补充检验方法,从而更有效地打击朱砂中添加色素的违法行为。
| [1] |
黄爽. 神农本草经[M]. 北京: 中医古籍出版社, 1982: 7.
|
| [2] |
马继兴. 神龙本草经辑注[M]. 北京: 人民卫生出版社, 1995: 148.
|
| [3] |
李时珍. 本草纲目(校点本):第1册[M]. 北京: 人民卫生出版社, 1975: 517.
|
| [4] |
中国药典: 一部[S]. 2015: 137.
|
| [5] |
贺双元, 林秀玉. 谈我市中药材朱砂质量出现的新问题[J]. 北方药学, 2006, 3(1): 58-59. |
| [6] |
潘穗生. 伪朱砂粉的鉴别检验研究[J]. 河南中医学院学报, 2008, 23(1): 45-46. DOI:10.3969/j.issn.1003-5028.2008.01.026 |
| [7] |
陈秀妾, 谭家群, 钟俊良, 等. 朱砂与伪品朱砂的鉴别[J]. 职业与健康, 2000, 16(8): 121-122. |
| [8] |
孙晶, 王坤, 习超鹏, 等. 几种中药材中添加人工合成色素的研究[J]. 中国药事, 2011, 25(12): 1200-1202. |
| [9] |
邹耀华, 殷红妹, 郭怡飚, 等. HPLC-PDA法检测西红花和红花中十一种非法添加色素[J]. 中国卫生检验杂志, 2010, 20(11): 2724-2725. |
| [10] |
马长宏, 单作刚, 齐家炜, 等. 中药染色掺假的研究进展[J]. 亚太传统医药, 2011, 7(2): 153-154. |
| [11] |
刘艳, 张勤, 吕志刚, 等. 红花中非法添加色素的薄层色谱快速鉴别法[J]. 中国实验方剂学, 2014, 20(18): 95-98. |
| [12] |
邵仕萍, 奚星林, 陈洁贞, 等. 饮料和糖果中5种非法添加色素的检测[J]. 食品科学, 2011, 34(4): 189-192. |
| [13] |
徐昱婷, 张学博, 苏静, 等. 超高效液相色谱-串联四级杆质谱法测定中药材(饮片)中非法添加6种水溶性红色素通用方法的研究[J]. 世界科学技术:中医药现代化, 2016, 18(5): 911-918. |
| [14] |
国家食品药品监督管理局.药品检验补充检验方法和检验项目批准件[S]. 2008.
|
| [15] |
张春辉, 傅超, 陈安珍. 跌打丸中非法染色剂808猩红的检测[J]. 中国药事, 2015, 29(10): 1069-1073. |
 2018, Vol. 32
2018, Vol. 32