厚朴为常用中药材及饮片,为国家基本药物名录收载品种,也是国家Ⅱ级重点保护野生植物。主要分布于陕西、甘肃、浙江、江西、湖北、湖南、四川、贵州等地[1-2]。厚朴为木兰科植物厚朴Magnolia officinalis Rehd.et Wils.或凹叶厚朴Magnolia officinalis Rehd.et Wils.var.biloba Rehd.et Wils.的干燥干皮、根皮及枝皮。具有燥湿消痰、下气除满的功效。主要用于治疗湿滞伤中,脘痞吐泻,食积气滞,腹胀便秘,痰饮咳喘等症[3]。
根据原国家食品药品监督管理总局的部署安排,天津市药品检验研究院承担了2016年厚朴药材的专项抽验任务,对从全国抽取的176批样品进行了评价性检验工作,本次专项抽验的厚朴样品均为中药饮片。按照现行法定标准对所有样品进行了全项检验。通过检测过程中出现的问题,结合市场调研存在的隐患,对厚朴开展了一系列的探索性试验,包括真伪鉴别、有效性、安全性等各个方面的摸索与研究。本文对此次专项抽验工作进行详尽的阐述与分析,对全部试验结果进行汇总与评估,对现行法定标准进行了完善与补充,以期更好地运用于厚朴的检验检测,为各级监管部门提供较完备的参考依据;同时,也让相关生产厂家及企业对厚朴药材及其饮片的质量现状有更加全面的了解与认知。
1 仪器和试药 1.1 仪器METTLER TOLEDO XS205电子天平;SHIMADZU LC-20AD(SPD检测器);EU-Sulfur二氧化硫电化学法快检仪;Agilent GC 6890N气相色谱仪;电感耦合等离子体质谱仪(ICP-MS):NexIoN 300X,Perkin Elmer;德国BRUKER MPA型近红外光谱仪(1.5 m光纤探头),OPUS 5.5软件;瑞士CAMAG LINOMAT 5半自动点样仪,CAMAG REPROSTAR 3薄层色谱成像系统;BIORAD SUB-GT水平电泳仪,BIO-RAD POWERPAC HV电源,ABI Step-One实时荧光定量PCR仪,Thermo NanoDrop2000微量紫外可见分光光度仪,eppendorf微量移液器;Waters e2695 alliance HPLC-MS;超导傅里叶核磁共振波谱仪(Bruker— 400MHz)。
1.2 试药厚朴酚对照品(批号110729-201513,含量以98.8%计),和厚朴酚对照品(批号110730-201313,含量以99.1%计),厚朴对照药材(批号121285-200902),6-姜辣素(批号111833-201102)。以上对照品均为含量测定用,均购置于中国食品药品检定研究院。
α、β、γ、δ-六六六,五氯硝基苯,pp‘- DDT,op‘- DDT,pp‘- DDE,pp‘- DDD由农业部环保所提供。
铅、砷、镉、汞、铜单元素溶液标准物质均购置于中国计量科学研究院,标准值:1000μg·mL-1。
金溶液成分分析标准物质、锗、铋、铟单元素标准溶液均购置于国家有色金属及电子材料分析测试中心,规格:1000 μg·mL-1。
黄曲霉毒素B1、黄曲霉毒素B2、黄曲霉毒素G1、黄曲霉毒素G2标准品均购自SUPELCO公司(Aflatoxin Mix Kit-M,Cat.NO.46304-U)。
柠檬黄、亮黄、日落黄、金橙Ⅱ、金胺O、碱性橙、胭脂红、苋菜红、赤藓红对照试剂均购置于天津市华东试剂厂。
植物基因组DNA提取试剂盒购自TIANGEN公司;β-巯基乙醇购自Sigma公司;PrimeSTAR HS(premix)PCR扩增试剂盒购自Takara公司;GelRed核酸染料购自BIOTIUM公司;100bp DNA ladder购自Solarbio公司;琼脂糖粉末购自北京奥博星生物技术有限公司。
甲醇、乙腈、硝酸均为色谱纯,购置于德国默克(MERCK)公司;质谱调谐液:PA Factor溶液(PE公司;Lot:14-203GSX1);乙醇、乙酸乙酯、三氯甲烷等试剂均为分析纯,购置于天津康科德科技有限公司。水为Milli-Q超纯水。
2 法定标准检验 2.1 抽验分布情况按照2016年国家中药饮片专项抽验计划的要求,共收集到130家饮片生产企业的176批厚朴样品,其中厚朴饮片120批次,姜厚朴饮片54批次,制厚朴饮片2批次。抽样地域覆盖全国31个省、自治区、直辖市(港澳台除外)。抽自饮片生产单位40批次,零售单位22批次,批发单位49批次,医疗单位65批次,分别占抽样总数的22.7%、12.5%、27.8%和36.9%。
2.2 法定标准检验结果厚朴药材现行法定标准收载于《中国药典》 2015年版一部[3]。现行药典标准项目有【性状】【鉴别】【检查】【含量测定】。另有厚朴和姜厚朴两个饮片规格,除无横切面显微鉴别外,厚朴及姜厚朴饮片其余检验项目均同药材。本次国家评价性抽验共抽到176批次样品,其中按《中国药典》 2010年版一部检验的共计78批、按《中国药典》 2015年版一部检验的共计96批、按《上海市中药饮片炮制规范》(2008年版)检验的共计2批。《中国药典》2010年版与2015年版标准完全一致;《上海市中药饮片炮制规范》(2008年版)中制厚朴仅有性状检验项目。我院对所有样品进行了全项检验,其中合格样品168批次,合格率为95.5%;不合格样品8批次,不合格率为4.5%,不合格项目均为含量测定。经统计分析发现,来源为批发及零售单位的样品合格率高于来源为饮片生产企业和医疗机构的样品。
2.2.1 性状本次专项抽验根据厚朴的实际情况,按照各自样品法定标准的性状项进行检验。结果176批样品均符合规定。部分样品颜色稍深,可能与炮制程度有关。具体见图 1。

|
图 1 厚朴饮片及其炮制品性状图 |
经检验发现,176批次厚朴及姜厚朴饮片均具有标准规定的显微特征,但有些饮片存在油细胞偏少的现象,原因可能是炮制过程中挥发性成分易损失造成的。见图 2。

|
图 2 厚朴显微鉴别图 |
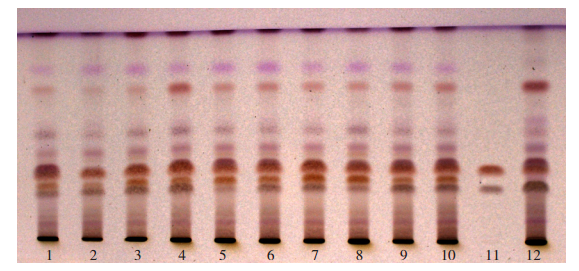
对176批次样品进行了薄层鉴别项的检验,均符合规定。此外,本试验还增加了厚朴对照药材的薄层鉴别作为补充,结果显示,均检出与厚朴对照药材相应的斑点。见图 3。
|
图 3 厚朴薄层鉴别色谱图 1~10.厚朴样品;11.厚朴酚及和厚朴酚混合对照品;12.厚朴对照药材。 |
标准规定应不得过10.0%。176批次样品水分测定结果在4.9%~10.0%,全部符合规定。直方图及正态分布图见图 4。

|
图 4 厚朴及其炮制品水分直方图及正态分布图 |
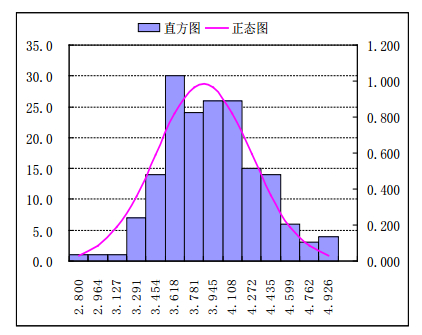
标准规定应不得过5.0%。176批次样品总灰分测定结果在2.8%~5.0%,全部符合规定。直方图及正态分布图见图 5。
|
图 5 厚朴及其炮制品总灰分直方图及正态分布图 |
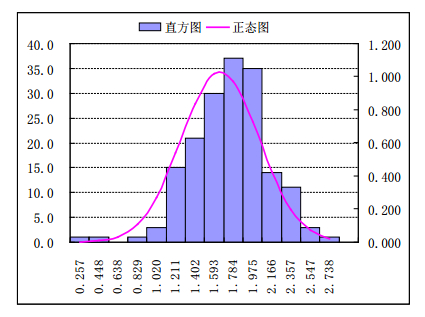
标准规定应不得过3.0%。176批次样品酸不溶性灰分测定结果在0.3%~2.8%,全部符合规定。直方图及正态分布图见图 6。
|
图 6 厚朴及其炮制品酸不溶性灰分直方图及正态分布图 |
标准规定:按干燥品计算,厚朴饮片含厚朴酚(C18H18O2)与和厚朴酚(C18H18O2)的总量不得少于2.0%;姜厚朴饮片不得少于1.6%。检验结果显示:176批样品中,168批含量测定结果均符合规定,8批不符合规定,合格率为95.5%。合格样品中2批制厚朴含量测定结果分别为3.7%和4.7%;52批姜厚朴含量测定结果在1.8%~5.6%;114批厚朴含量测定结果在2.0%~6.6%。
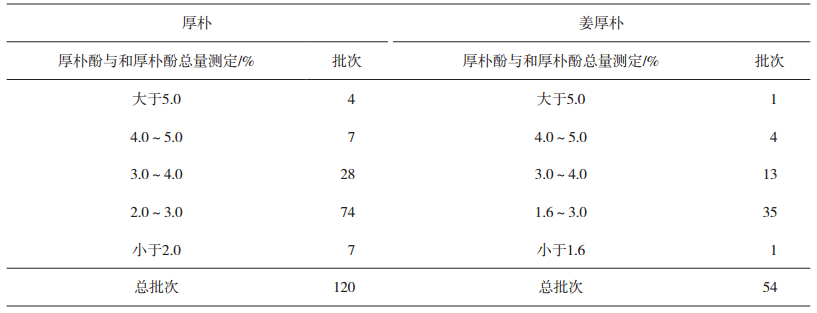
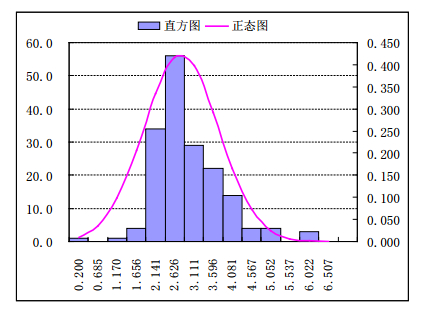
结果分析:含量测定是此次厚朴检验结果不合格的主要原因,不同样品含量差异很大,厚朴酚与和厚朴酚的总量最高达6.6%,最低仅为0.2%,具体分布情况见表 1、直方图及正态分布图见图 7。
|
|
表 1 样品含量测定结果 |
|
图 7 厚朴及其炮制品含量测定直方图及正态分布图 |
不合格的厚朴饮片有7批含量在1.1%~1.8%;姜厚朴饮片有1批不合格,含量仅为0.2%,怀疑使用的原料在炮制成姜厚朴之前已经提取过有效成分。
2.3 标准评价厚朴质量标准收载了【性状】【鉴别】(显微鉴别、薄层色谱鉴别)、【检查】(水分、总灰分、酸不溶性灰分)及【含量测定】等检测项目,标准较为完善,确切可行,能基本控制厚朴的质量,总体评价为“可行”。
3 探索性研究法定标准检验结果显示,目前我国流通使用的厚朴质量相对较好,但仍有少数厚朴饮片及炮制品存在造假掺伪[4-6]等问题,围绕质量隐患,笔者查阅了大量的文献资料[7-12],展开了一系列的研究工作。
3.1 对法定标准含量测定项中供试品提取方法的考察对《中国药典》2015年版一部厚朴含量测定项下供试品溶液的制备方法进行了考察与比较,结果显示:超声处理30分钟与浸渍24小时(药典标准)几乎相同,二者略高于加热回流30分钟。故建议修订药典标准,以提高试验效率。
3.2 显微鉴别通过对176批次厚朴饮片及其炮制品的检测发现,有4批次厚朴饮片粉末的显微鉴别检出了草酸钙簇晶。见图 8。

|
图 8 含草酸钙簇晶的厚朴饮片显微鉴别图 |
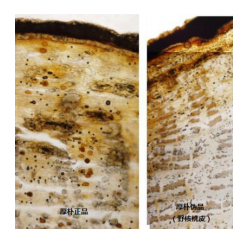
以上4批次厚朴饮片除检出草酸钙簇晶外,其余显微鉴别均与法定标准相符。此外,该4批药材均含有厚朴酚与和厚朴酚,据文献[8]报道,含簇晶的伪品均不含以上2种成分,且4批样品按法定标准检验除3批含量不合格外,其余均符合规定,1批全检合格。怀疑有掺伪的可能,因此进行了样品横切面的检验,结果发现确实存在掺伪现象,断面皮层有石细胞环带,皮层及韧皮处布满了草酸钙簇晶,判定伪品为野核桃皮,见图 9。
|
图 9 厚朴饮片正伪品横切面显微鉴别图 |
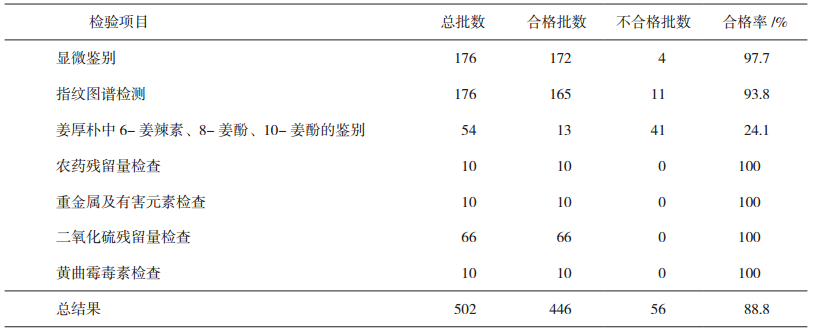
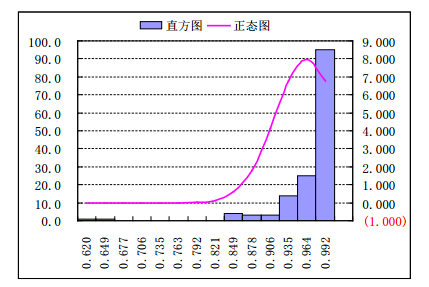
采用高效液相色谱法建立厚朴指纹图谱[13]。结果显示:176批次样品中,有165批次基本一致,占93.75%;11批次不一致,占6.25%。指纹图谱比对见图 10、直方图及正态分布图见图 11。

|
图 10 部分样品的液相指纹图谱 |
|
图 11 176批样品指纹图谱直方图及正态分布图 |
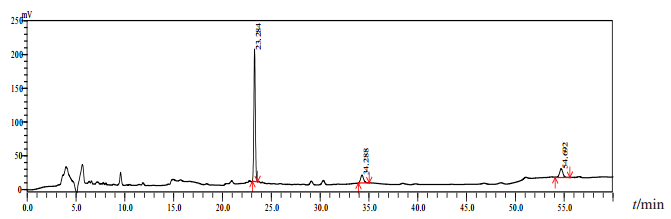
采用高效液相色谱法测定54批姜厚朴及2批制厚朴中是否含有6-姜辣素、8-姜酚、10-姜酚3种成分[3]。结果发现,有3批姜厚朴检测出这3种成分,见图 12、13;有2批次制厚朴及10批次姜厚朴检测出6-姜辣素及10-姜酚;其余均未检出该3种成分。检出生姜成分的姜厚朴约为24.1%。分析原因,可能是姜厚朴炮制过程中有加热步骤,导致生姜挥发性成分易损失破坏,从而导致不易检出。
|
图 12 生姜对照药材色谱图 |

|
图 13 姜厚朴3种成分色谱图 |
因为中药材在生长过程中不可避免地会使用或接触到各种农药,尤其是有机氯类农药,毒性较大,分解时间长,因此采用气相色谱法测定滴滴涕、六六六、五氯硝基苯等9种常用有机氯类农药的残留量。选取部分样品进行测定,结果均未检出有机氯。
3.5.2 重金属及有害元素检查采用ICP-MS方法[14]测定部分样品中的重金属及有害元素铜、汞、铅、镉、砷的残留量,结果均合格。
3.5.3 二氧化硫残留量检查随机抽取了66批厚朴抽验样品,包括含量测定不合格及含有簇晶的样品。采用电化学快检方法筛查厚朴饮片SO2残留量,结果均未检出,合格率为100%。
3.5.4 黄曲霉毒素检查参照《中国药典》2015年版四部通则2351黄曲霉毒素测定法第一法,对含量不合格、表面有霉变斑点及含有簇晶掺伪等有问题的厚朴样品进行检测,结果均未超出限度规定。
3.5.5 化工染料非法染色检查采用《药品快速检测技术研究与应用中药卷》第三节有机染料(色素)染色方法的研究中第一、二法,采用高效液相色谱法,检测全部176批次样品中是否含有黄橙色素及红色色素,结果均未检出,均符合规定。
3.6 近红外光谱测定该方法旨在快速高效准确地区分不同地域厚朴品种及其真伪[15]。对抽验的130家生产企业的176批次厚朴、姜厚朴及制厚朴饮片进行了近红外光谱扫描,并尝试用不同数学处理方法建立模型,结果均不令人满意。分析原因,可能是由于各生产厂家的厚朴饮片及其炮制品相似度很高、品种较为混乱,很难通过近红外快检方法区分不同地域生产厂家的厚朴饮片样本,有待进一步深入研究。
3.7 对厚朴饮片进行分子生物学鉴定研究根据此次全国评价性抽验工作中检测时发现的问题,比如掺伪情况,以及经调研目前市面上出现的厚朴伪品多为日本厚朴、大叶木兰、长叶木兰、野核桃皮等品种。参考《中国药典》2015年版四部通则9107“中药材DNA条形码分子鉴定法指导原则”中的引物,对厚朴饮片及其炮制品进行厚朴物种基源的鉴定[14, 16-17]。
1)采用psbA引物对46批次典型样品进行扩增,其中21个扩增成功,占样本总数的45.7%;经过测序和拼接后能进行序列比对为厚朴的样品有19个,占样本总数的41.3%。其中有2个样品能成功扩增却无法成功进行拼接,原因是扩增的条带中有非特异条带,测序时存在套峰现象。
2)46批样品中,用ITS2引物能成功扩增的样品有17个,占样本总数的37.0%;经过测序和拼接后能进行序列比对为厚朴的样品有0个,证明用ITS2引物进行厚朴基源鉴定是不可行的。
3)厚朴对照药材用psbA引物能够成功进行扩增和序列比对,但是用ITS2引物却不能成功扩增。既然用psbA引物能够成功进行扩增和序列比对,证明厚朴对照药材基因组DNA提取的质量没有问题,不会干扰PCR扩增。至于用ITS2引物不能扩增成功的原因,可能是ITS2引物的特异性问题导致的。
4)psbA引物用于厚朴药材基源鉴定的特异性偏低,结果不够准确。而ITS2引物进行扩增,虽然有部分样品能够扩增出条带,但与厚朴正品进行数据比对,皆为其他物种。原因可能是ITS2引物的特异性对厚朴物种不适用。因此,用2015年版《中国药典》通则 < 9107 > “中药材DNA条形码分子鉴定法指导原则”中的引物来对厚朴药材进行物种基源鉴定,结果专属性不强,有待进一步深入研究。
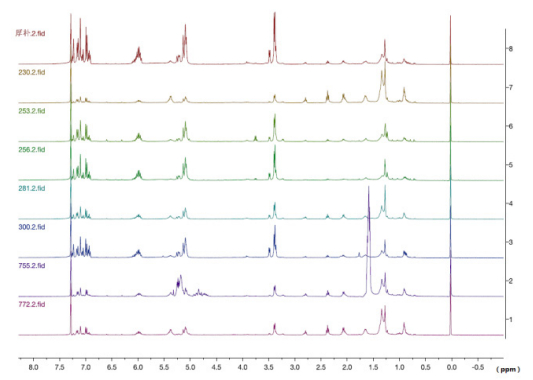
3.8 1H—NMR指纹图谱研究采用核磁共振法[18]对存在问题的部分厚朴及姜厚朴饮片进行测定,采用超导傅里叶核磁共振波谱仪(Bruker-400MHz),建立1H-NMR指纹图谱,测定厚朴样品的1H-NMR指纹图谱,见图 14。由图 14可见,含量不合格且掺伪的样品与厚朴对照药材存在明显差异。因此,建立厚朴药材及其饮片的核磁指纹图谱可有效区分掺伪样品,对厚朴的真伪鉴别提供较为科学准确的检验依据,该方法灵敏度高,可用于一般检测方法不易查见的掺伪厚朴情况。
|
图 14 厚朴特征总提取物的1H—NMR指纹图谱叠加图 |
对市场上调研的3种等级的厚朴进行了含量测定比较,分析厚朴酚与和厚朴酚的含量与等级的相关性。结果表明,性状较好、皮部较厚,尤其是切面颗粒性,有油性可见小亮星的厚朴含量较高,质量由好至坏的依次顺序:厚朴根皮>干皮>枝皮。见图 15。

|
图 15 不同等级厚朴饮片性状及含量比对图 |
探索性研究检验结果显示,目前市场上厚朴质量较好,仅个别存在含量不合格及掺伪问题。厚朴样品探索性研究结果详见表 2。
|
|
表 2 厚朴探索性研究检验结果 |
单从探索性研究的结果与标准检验结果的合格率上比较,二者相差不大。但前后检验的不合格样品中,存在交叉现象,即法定标准检验合格,探索性研究数据不合格;或法定标准检验不合格,而探索性研究数据合格。这正说明了所制定的探索性研究方法,是对法定标准检验的有益补充,二者结合,能够为厚朴的质量控制提供更有力的技术支持。
5 问题和建议 5.1 药材饮片的质量问题通过此次厚朴的专项抽验,发现我国市场上所售厚朴的质量较好,伪品相对较少。但仍存在如下几方面的问题:
1)厚朴粉末的显微鉴别中有4批饮片除按法定标准显微检验合格外,又检出了草酸钙簇晶,其他检验项目符合规定,提示可能存在既掺伪又钻法定标准空子的问题。
2)在姜厚朴的炮制过程中也存在问题。对54批姜厚朴及2批制厚朴进行检验发现,有41批次均未检出生姜成分:一方面,可能厚朴饮片在经过生姜汁炮制过程中,有加热炒干、晾晒等过程,导致生姜挥发性成分损失破坏而难以检出;另一方面,可能是在炮制过程中辅料生姜偷工减料,或采用质量较次的生姜对厚朴进行炮制,从而导致姜成分不易检测。
5.2 标准和检验方法存在的问题厚朴按现行法定质量标准检验可行,基本上可以控制厚朴的质量,但仍需对标准进行补充与完善,建立能更加全面控制厚朴质量的标准。在此次评价性抽验工作中发现,采用《中国药典》2015年版一部法定标准检验,能较好地对厚朴进行评价,但是对于一些掺伪情况仍存在漏洞,比如,各项检测按法定标准均合格,但检出簇晶,横切面与厚朴正品不同,这些都是按法定标准未规定的。与此同时,增加了分子生物学鉴定、核磁指纹图谱等其他技术手段用以佐证,均检出了掺伪样品。可见,综合全面的检测方法是对厚朴正品准确性的有益补充。
5.3 检验和监管建议厚朴作为我国传统常用中药,长期以来深受广大患者的认可。通过此次国评抽验工作发现,目前市面上大部分厚朴饮片及其炮制品合格率相对较高,极少数样品存在含量不合格的问题。因厚朴在市场上交易量和流通量较大,在近两年的全国中药材及饮片抽查工作中,厚朴也作为重点抽查对象之一。对此,提出如下建议。
1)建议多指标、多种仪器方法监控产品质量。对厚朴的基源属性、相近物种的研究已迫在眉睫,建立特异性PCR等专属性较强的方法是亟待解决的难题之一。
2)建议加强生产、流通、使用领域的监管,建立专项抽验长效机制,将专项抽验中发现的质量问题及时反馈给各生产企业。特别是对此次抽验工作中涉及不合格产品较多的地区更应加大抽验力度,对本次评价结果较差的生产企业进行追踪检查和长期跟踪监管,以保障公众用药安全有效。
| [1] |
熊璇, 于晓英, 魏湘萍, 等. 厚朴资源综合应用研究进展[J]. 林业调查规划, 2009, 34(4): 88-92. DOI:10.3969/j.issn.1671-3168.2009.04.024 |
| [2] |
曾应文, 杨成梓. 厚朴品质评价研究进展[J]. 亚太传统医药, 2012, 8(10): 202-204. DOI:10.3969/j.issn.1673-2197.2012.10.126 |
| [3] |
中国药典: 一部[S]. 2015.
|
| [4] |
徐振军. 厚朴和厚朴习用品、混淆品及伪品的鉴别[J]. 中国中医药现代远程教育, 2008, 6(5): 431-433. DOI:10.3969/j.issn.1672-2779.2008.05.025 |
| [5] |
张朝民. 厚朴常见伪品的鉴别检验[J]. 光明中医, 2016, 31(8): 1183-1184. DOI:10.3969/j.issn.1003-8914.2016.08.066 |
| [6] |
王万贤, 高守泉, 代为苹. 厚朴及其伪品[J]. 中药材, 1986, 6: 26-28. |
| [7] |
樊小容. 紫外光谱法鉴别厚朴及其伪品有求必应[J]. 中草药, 2001, 32(8): 743-744. DOI:10.3321/j.issn:0253-2670.2001.08.038 |
| [8] |
朱晓云. 厚朴及其伪品的鉴别[J]. 福建医药杂志, 2005, 27(5): 151-152. |
| [9] |
刘红亮, 晏仁义, 郭健. 厚朴"发汗"前后药材颜色及气味差异的数值化研究[J]. 中国中药杂志, 2013, 38(1): 45-48. |
| [10] |
黄文华, 郭宝林, 斯金平. 不同种源厚朴酚性成分的HPLC图谱研究[J]. 中国中药杂志, 2005, 30(13): 968-971. DOI:10.3321/j.issn:1001-5302.2005.13.002 |
| [11] |
白仲梅, 苏学秀. 厚朴及其伪品滇藏木兰的鉴别[J]. 现代中药研究与实践, 2007, 21(4): 28-30. |
| [12] |
陈秀杰, 耿冶飞, 段秀君. 厚朴与伪品山玉兰的鉴别[J]. 河南中医, 2013, 33(3): 440-441. |
| [13] |
裴学军, 芦金清, 刘毅, 等. 厚朴药材高效液相指纹谱实验研究[J]. 中药材, 25(9): 631-634. |
| [14] |
中国药典: 四部[S]. 2015.
|
| [15] |
余驰, 姜红, 刘爱萍. 近红外漫反射光谱法建立厚朴药材的定性模型[J]. 药物分析杂志, 2009, 29(4): 656-658. |
| [16] |
王洁, 杨旭, 杨志玲. 不同产区厚朴nrDNA ITS序列分析及亲缘关系鉴定[J]. 广西植物, 2013, 33(1): 35-41. |
| [17] |
李西文, 胡志刚, 林小涵, 等. 基于454FLX高通量技术的厚朴叶绿体全基因组测序及应用研究[J]. 药学学报, 2012, 47(1): 124-130. |
| [18] |
聂映, 姚卫峰, 沈文斌. 厚朴的1H-NMR指纹图谱研究[J]. 江苏中医药, 2008, 40(11): 91-93. DOI:10.3969/j.issn.1672-397X.2008.11.054 |
 2018, Vol. 32
2018, Vol. 32