2. 贵州省遵义市食品药品检验所, 遵义 563002
2. Zunyi Institute for Food and Drug Control, Zunyi 730070, China
菥蓂,现收载于《中国药典》2015年版一部中,为十字花科菥蓂属一年生草本植物菥蓂Thlaspi arvense L.的干燥地上部分[1],又名遏蓝菜、苏败酱(江苏)、南败酱(湖北)、苦芥子、败酱草、爪子草、野榆树、菥目(陕西),分布于全国各地,其全草、嫩苗和种子均可入药。全草清热解毒、消肿排脓;嫩苗和中益气、利肝明目。菥蓂始载于《神农本草经》,列为上品,之后历代本草多有记载[2-3];《中国药典》 1977年版作为正名,别名“苏败酱”,以区别于败酱科败酱草,具有清肝明目、和中、解毒的功效,用于目赤肿痛,消化不良,脘腹胀痛,肝炎,阑尾炎,疮疖痈肿[4]。河南、广西、湖南等地方标准收载了该药材,《卫生部药品标准》中收载了菥蓂子,为该药材的干燥成熟种子[5-9]。菥蓂主要含有黑芥子苷等硫苷类成分,异荭草苷、异牡荆苷等黄酮碳苷类成分[10-12]。菥蓂的指纹图谱和含量测定研究报道较少。陈玉等[13]采用HPLC法测定了菥蓂子中的黑芥子苷含量;庞赛等[14]以异牡荆苷为参照峰建立了菥蓂的HPLC指纹图谱。
异荭草苷具有较好的体内外抗病毒活性,能一定程度上缓解病毒性炎症[15];异牡荆苷具有抗氧化、降血糖、抗炎等活性[16]。针对《中国药典》2015年版一部菥蓂项下缺少含量测定项目,本研究针对市场上抽取的菥蓂药材,采用恒流HPLC法30 min内完成洗脱,建立菥蓂的指纹图谱,并同时测定2种黄酮碳苷异荭草苷和异牡荆苷(结构式见图 1)的含量,为菥蓂药材的质量控制提供科学依据。

|
图 1 结构式 1.异荭草苷;2.异牡荆苷。 |
沃特世2695型高效液相色谱仪,紫外检测器,P120H型超声波清洗器(德国ELMA公司),Milli-Q纯水系统,电子天平(Sartorius公司,SECURA224-1CN型万分之一天平),电子天平(Sartorius公司,MSE125S型十万分之一天平)。Waters HSS T3色谱柱(填料:十八烷基键合硅胶,250 mm×4.6 mm,5 μm;沃特斯仪器公司)。
1.2 试药异荭草苷对照品(中国食品药品检定研究院,批号:111974-201401,纯度94.0%)、异牡荆苷(上海源叶生物技术有限公司,批号:P20N6FC331,纯度99.6%)。甲醇和乙腈为色谱纯(Fisher公司);水为Milli-Q纯化水。
1.3 样品药材均来自2016年国家药品抽验性评价项目的抽验样品,经中国食品药品检定研究院民族药室郑健研究员鉴定。1~13号样品为十字花科菥蓂Thlaspi arvense L.的干燥地上部分。
2 溶液的制备 2.1 混合对照品溶液取异荭草苷和异牡荆苷约10 mg,精密称定,分别置10 mL量瓶中,用甲醇溶解并定容至刻度,即得各对照品储备液。分别取各对照品储备液适量,置同一10 mL量瓶中,加乙腈配制成上述2种成分分别为20、50 μg·mL-1的混合溶液,即得。
2.2 供试品溶液取样品粉末(过四号筛)约1 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,超声处理(功率:250 W,频率:33 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
3 色谱条件Waters HSS T3色谱柱(250 mm×4.6 mm,5 μm);以乙腈-0.5%醋酸水溶液(15:85)为流动相;流速为1.0 mL·min-1;检测波长为350 nm;柱温为30 ℃;进样量为10 μL。
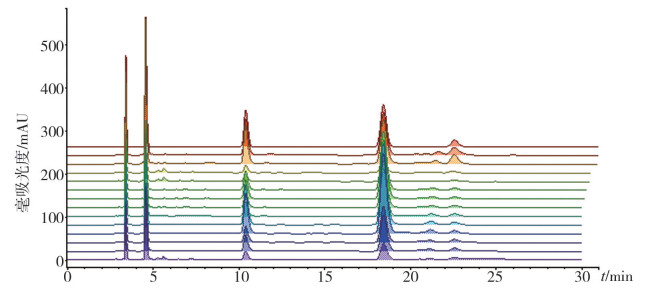
4 指纹图谱 4.1 菥蓂指纹图谱的建立取不同批次的菥蓂(1~13号样品)粉末,按“ 2. 2 ”节方法制备供试品溶液,精密吸取10 μL,进样测定,记录30 min的HPLC色谱图(见图 2)。根据结果,采用Chempattern化学计量学软件进行数据分析处理,设定1号样品的图谱为参照图谱,将其他样品的色谱图与参照图谱进行自动匹配,根据共有峰的平均色谱图生成菥蓂的指纹图谱(图 3)。
|
图 2 13批菥蓂HPLC色谱图 |
|
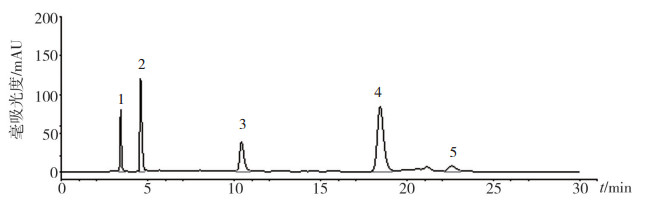
图 3 菥蓂HPLC指纹图谱 1、2、5.未知成分待进一步研究;3.异荭草苷;4.异牡荆苷。 |
根据13批菥蓂的指纹图谱检测结果,共标定5个特征峰。经过与对照品比对,可知3号峰为异荭草苷,4号峰为异牡荆苷。
4.3 方法学考察 4.3.1 精密度试验精密吸取同一菥蓂供试品溶液(样品1)10 μL,按上述色谱条件,连续进样测定6次,记录色谱图。以异牡荆苷为参照峰,计算特征峰的相对保留时间及相对峰面积,结果各特征峰的相对保留时间的RSD<1%,单峰面积占总峰面积大于2%的特征峰的相对峰面积RSD<2%,采用科迈恩(北京)科技有限公司Chempattern化学计量学软件进行评价,相似度(夹角余弦法,下同)为0.99,结果表明仪器精密度良好。
4.3.2 稳定性试验精密吸取同一菥蓂供试品溶液(样品1)10 μL,分别于溶液配制后0、2、4、6、8、12、24 h,按上述色谱条件进样测定,记录色谱图。以异牡荆苷为参照峰,计算特征峰的相对保留时间及相对峰面积,结果各特征峰的相对保留时间的RSD<1%,单峰面积占总峰面积大于2%的特征峰的相对峰面积RSD<2%,采用Chempattern化学计量学软件进行评价,相似度为0.99,表明供试品溶液在24 h内稳定性良好。
4.3.3 重复性试验取同一批菥蓂样品粉末(样品1)6份,精密称定,按“2.2”节方法分别制备供试品溶液,精密吸取供试品溶液10 μL,进样测定,记录色谱图。以异牡荆苷为参照峰,计算特征峰的相对保留时间及相对峰面积,结果各特征峰的相对保留时间的RSD<1%,单峰面积占总峰面积大于2%的特征峰的相对峰面积RSD<2%,采用Chempattern化学计量学软件进行评价,相似度为0.99,结果表明,该方法重复性好。
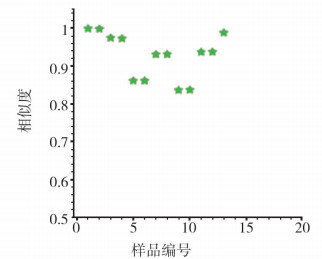
4.4 相似度评价以样品1为参照图谱,生成菥蓂药材的指纹图谱,13批菥蓂药材与指纹图谱的相似度见图 4,相似度分别为1.000、0.999、0.975、0.974、0.862、0.862、0.932、0.932、0.837、0.838、0.938、0.938和0.989,结果表明相似度较好。
|
图 4 菥蓂药材相似度计算结果 |
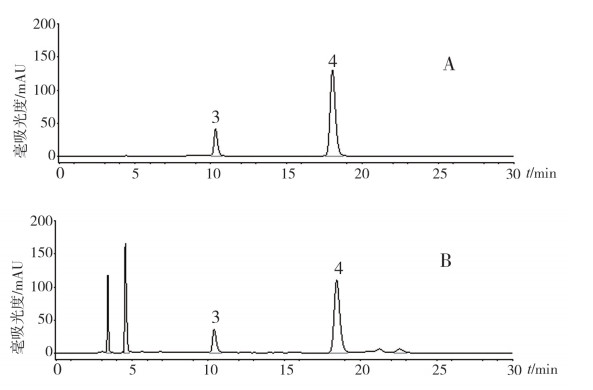
按“3”项下色谱条件进行检测,以异牡荆苷峰计算理论塔板数大于6000,分离度大于1.5。对照品及样品的色谱图见图 5。
|
图 5 菥蓂HPLC含量测定色谱图 A.对照品混合溶液;B.供试品溶液;3.异荭草苷;4.异牡荆苷。 |
精密吸取各对照品储备液0.02、0.1、0.05、0.5、1.0、2.0 mL,分别置于6个10 mL量瓶中,加甲醇定容至刻度,摇匀,即得各系列浓度的混合标准溶液。分别精密吸取各系列浓度的标准溶液及对照品储备液各10 μL,注入液相色谱仪,测定,以各对照品质量浓度(μg·mL-1)为x轴,以峰面积为y轴,进行线性回归,各对照品回归方程和线性范围见表 1。结果表明,2种成分在一定质量浓度范围以内,进样量与峰面积线性关系良好。
|
|
表 1 各被测成分的标准曲线方程、线性范围和相关系数 |
取“2.1”节混合对照品溶液用甲醇逐级稀释后进样测定,以色谱图中信噪比3:1为检测限,信噪比10:1为定量限。结果表明,异荭草苷和异牡荆苷的检测限分别为0.8和1.1 ng;定量限分别为2.1和2.8 ng。
5.4 精密度试验精密吸取“2.1”节对照品混合溶液10 μL,连续进样6次,记录峰面积。结果异荭草苷和异牡荆苷峰面积的RSD分别为0.29%和0.25%(n=6),表明仪器精密度良好。
5.5 重复性试验取样品粉末(样品1)6份,分别按照“2.2”节方法制备供试品溶液,按“3”项下色谱条件测定,记录峰面积,计算含量。结果供试品溶液的异荭草苷和异牡荆苷平均含量分别为0.023%和0.090%,RSD分别为1.57%和1.95%,结果表明重复性良好。
5.6 溶液稳定性试验取同一份供试品溶液(样品1),分别于配制后0、2、4、8、12、24 h进样测定。结果异荭草苷和异牡荆苷峰面积的RSD(n=6)分别为0.72%和0.52%,结果表明供试品溶液在24 h内稳定。
5.7 加样回收率试验分别取异荭草苷和异牡荆苷适量,精密称定,置量瓶中,加甲醇溶解配制成质量浓度分别为0.1089、0.4448 mg·mL-1的对照品溶液。取已知含量的供试品粉末(样品1)6份,每份各约0.5 g,精密称定,分别置具塞锥形瓶中,精密加入上述2种对照品溶液各1.0 mL,按照“2.2”节方法平行制备供试品溶液,进样分析,计算回收率,结果见表 2~表 3,表明该方法加样回收试验结果良好。
|
|
表 2 异荭草苷加样回收率试验结果(n=6) |
|
|
表 3 异牡荆苷加样回收率试验结果(n=6) |
每批样品取2份,分别按“2.2”节方法制备供试品溶液。精密吸取各供试品溶液10 μL,按“3”项下色谱条件进行测定,13批菥蓂样品中异荭草苷和异牡荆苷的含量结果见表 4。
|
|
表 4 13批菥蓂中异荭草苷和异牡荆苷含量测定结果(n=2) |
本研究采用等度洗脱色谱法分离菥蓂药材中2种主要黄酮碳苷类成分,30 min内完成分离,异荭草苷和异牡荆苷分离效果良好,符合含量测定要求。本研究通过二极管阵列检测器考察所测物质紫外吸收,2种待测成分具有相同的结构母核,主要是取代基不同,紫外最大吸收均在350 nm,因此,选择350 nm为检测波长。
6.2 指纹图谱分析13批菥蓂均含有5个特征峰,通过对照品比对法,标定了2种黄酮碳苷类成分,各批次之间HPLC图谱与指纹图谱之间的相似度较好,可用于菥蓂的质量控制。
6.3 含量测定从表 4异荭草苷和异牡荆苷测定结果来看,异荭草苷含量在0.015%~0.094%,平均为0.042%;异牡荆苷含量在0. 0 3 4 % ~ 0. 3 2 3 %,平均为0.152%;二者总含量在0.050%~0.418%,平均为0.195%。异牡荆苷含量均高于异荭草苷含量,二者比值在2.0~5.6倍,平均为3.9倍,该比值具有一定的鉴别意义。
该方法简单方便、准确性高,建议可作为药典含量测定方法。异荭草苷和异牡荆苷二者含量之和作为测定限度较为合理,并可确定异荭草苷和异牡荆苷含量之和不低于0.10%作为指标。按此限度,测定的13批样品,第6和9批次含量较低,低于限度,其余11批符合限度要求。
6.4 小结本试验在同一色谱条件下,建立了菥蓂药材的指纹图谱,并同时测定13批药材中异荭草苷和异牡荆苷的含量,方法简便、快速、准确,具备了定性和定量双重作用,为有效控制菥蓂的质量提供了科学依据。
| [1] |
中国药典: 一部[S]. 2015: 308.
|
| [2] |
青海省藏医药研究所, 青海省药品检验所. 中国藏药[M]. 上海: 上海科学技术出版社, 1996: 337-341.
|
| [3] |
中国药品生物制品检定所, 云南省药品检验所, 内蒙古自治区药品检验所, 等. 中国民族药志:第二卷[M]. 北京: 人民卫生出版社, 1990: 465-469.
|
| [4] |
中国药典: 一部[S]. 1977: 524-525.
|
| [5] |
河南省卫生厅. 河南省中药材标准[S]. 郑州: 中原农民出版社, 1991: 82-83.
|
| [6] |
河南省食品药品监督管理局. 河南省中药饮片炮制规范[S]. 郑州: 河南人民出版社, 2005: 322-323.
|
| [7] |
湖南省食品药品监督管理局. 湖南省中药材标准[S]. 长沙: 湖南科学技术出版社, 2009: 307.
|
| [8] |
广西壮族自治区食品药品监督管理局. 广西壮族自治区壮药质量标准: 第二卷[S]. 2011: 257-258.
|
| [9] |
国家药典委员会. 卫生部药品标准藏药第一册[S]. 1995: 90.
|
| [10] |
潘正, 高运玲, 刘毅, 等. 菥蓂的化学成分研究[J]. 中成药, 2013, 35(5): 995-997. |
| [11] |
丁建海, 张俊芳. 菥蓂的化学成分及药理作用研究[J]. 宁夏师范学院学报:自然科学, 2014, 35(3): 78-81. |
| [12] |
于金英, 王云红, 刘国强, 等. HPLC-ESI-MS/MS分析鉴定菥蓂中黄酮类成分[J]. 中成药, 2015, 37(3): 556-561. |
| [13] |
陈玉, 周旻, 伍丽萍, 等. HPLC测定菥蓂子中的黑芥子苷[J]. 华西药学杂志, 2012, 27(1): 94-95. |
| [14] |
庞赛, 王立升, 史新, 等. 菥蓂药材中异牡荆苷的分离鉴定及指纹图谱研究[J]. 广东农业科学, 2012(1): 105-107. |
| [15] |
朱秀珍, 史文伟, 龚翠莹, 等. 异荭草苷体内外抗呼吸道合胞病毒活性研究[J]. 中山大学学报:医学科学版, 2015, 36(5): 352-359. |
| [16] |
闫冲, 林励, 刘红菊, 等. HPLC研究异牡荆苷在大鼠体内的药代动力学及组织分布[J]. 中国药学:英文版, 2011, 20(4): 376-382. |
 2017, Vol. 31
2017, Vol. 31 
