2. 中国食品药品检定研究院, 北京 100050
2. National Institutes for Food and Drug Control, Beijing 100050, China
红参药材为五加科植物人参(Panax ginseng C.A. Mey)的栽培品经蒸制而成。秋季采挖,洗净,蒸制后,干燥。红参药用历史悠久,自古就有把采集到的野生人参,用煮、蒸、焯等方法进行加工处理,得到熟人参,这种加工方式逐渐演变成以后的红参。红参的使用范围较广,除应用于多种中药成方制剂以外,在中医临床上使用也很普遍,传统医学认为,红参在补虚方面更强于人参,因此也成为日常保健的常用滋补品[1-4]。《中国药典》自1963年版起历版药典中均收载了红参,在1995年版以前,红参作为人参的一种炮制规格,收载于人参项下,自1995年版起,红参开始作为一个独立品种被药典收载。
为科学评价红参药材与饮片的质量状况,2015年国家食品药品监督管理总局在全国范围内对红参药材与饮片进行了专项评价抽验,我们在法定标准检验的基础上,围绕安全性、有效性等方面开展了探索性研究,发现了其主要质量风险,并提出了管控方案,为红参药材与饮片质量标准提高、加强监督管理提供了参考。
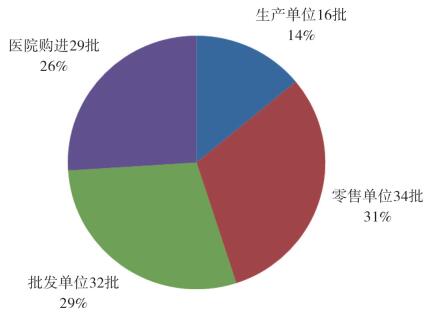
1 抽样情况本次专项抽验共抽取红参样品111批次,包括药材和饮片两个规格,其中药材59批次,饮片52批次。抽样地域覆盖了全国30个省级行政区,只有海南省没有抽到样品。111批次样品中抽自饮片生产单位16批次,零售单位34批次,批发单位32批次、医疗单位29批次。全部样品覆盖了24个省、市、自治区的83家饮片生产企业,另有3批次样品未标示生产单位。见图 1。
|
图 1 红参抽样单位性质分布表 |
红参法定标准为《中国药典》2010年版一部[5],收载有性状、显微鉴别、薄层鉴别、水分以及含量测定等项目,我们选择了性状、薄层鉴别、水分和含量测定进行检验,结果不合格项目主要为性状与含量测定,另有3批次样品薄层鉴别不符合规定。
2.1 性状性状不合格样品主要表现为颜色浅、质地软、味道甜,其原因可能是非法加糖所致。见图 2。

|
图 2 红参药材及饮片性状照片 A、B.合格样品;C、D.不合格样品。 |
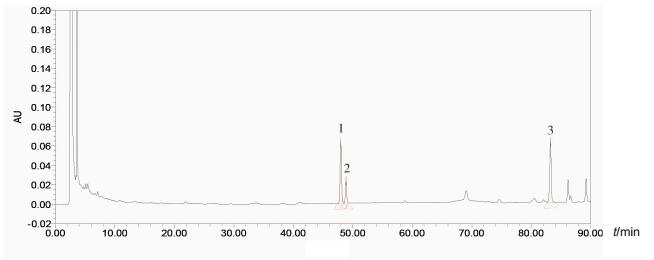
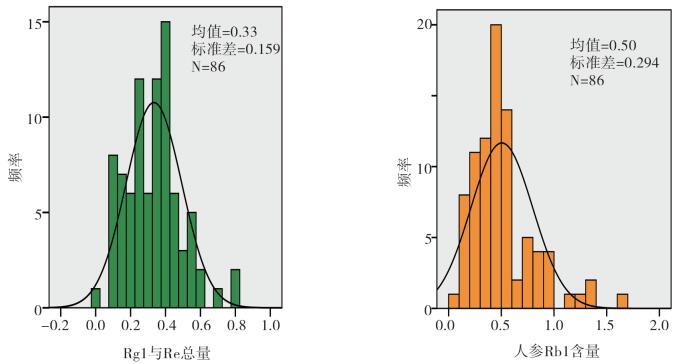
法定标准规定用高效液相色谱法测定人参皂苷Rg1、人参皂苷Re与人参皂苷Rb1的含量,色谱图见图 3。测定结果表明样品含量差异较大,Rg1和Re的总量最高达0.80%,最低不足0.01%,Rb1含量最高达1.32%,最低仅为0.01%,测定结果频数分布详见图 4。含量测定项不合格的样品中,主要为Rg1和Re总量不合格,Rb1含量测定结果不合格较少。
|
图 3 红参含量测定样品色谱图 1.人参皂苷Rg1峰;2.人参皂苷Re峰;3.人参皂苷Rb1峰。 |
|
图 4 红参含量测定频数分布图 |
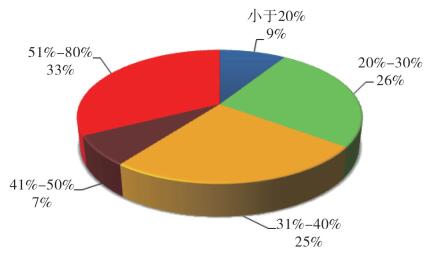
参考《食品中还原糖的测定》[6]等国家标准以及有关文献资料,将样品中所含的糖(包括多糖、寡糖、双糖、单糖等)经酸水解为单糖,与碱性酒石酸铜发生氧化-还原反应来测定样品中总糖含量,制定适当的限度,打击非法掺糖的行为。通过上述方法对全部样品测定含糖量,结果见图 5。正常红参与人参绝大部分样品含糖量小于25%,仅个别批次在25%~30%之间,111批次样品中有39批次含糖量小于30%,占总数的35%,72批大于30%,占总数的65%。
|
图 5 样品含糖量测定结果及分布 |
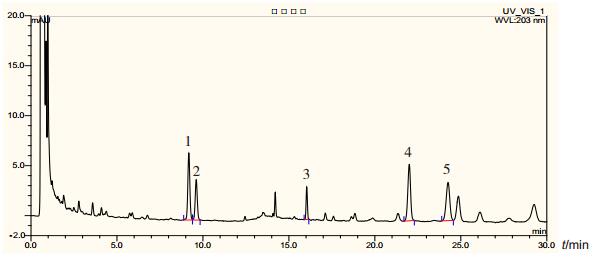
红参的主要有效活性成分为皂苷类成分[7-11],法定标准中测定了3种成分含量,测定时间长达90 min,因此,建立了红参中人参皂苷Rg1、人参皂苷Re、人参皂苷Rf、人参皂苷Rb1及人参皂苷Ro 5种皂苷类成分的UPLC含量测定方法。色谱条件:Thermo Hypersil GOLD C18(2.1 mm× 100 mm,1.9 μm);以乙腈为流动相A,0.05%磷酸为流动相B,梯度洗脱,0~9min,A 18%→20%,9~11 min,20%→28%,11~ 30 min,A保持28%;柱温为40 ℃;检测波长为203 nm;进样量:1 µL。供试品溶液制备:取本品粉末(过4号筛)约1 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇25 mL,密塞,称定重量,加热回流提取1 h,取出,放冷,再称定重量,用80%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。建立的方法简便快速,灵敏度高,5种成分分离度好,见图 6。
|
图 6 红参含量测定色谱图 1.人参皂苷Rg1;2.人参皂苷Re;3.人参皂苷Rf;4.人参皂苷Rb1;5.人参皂苷Ro。 |
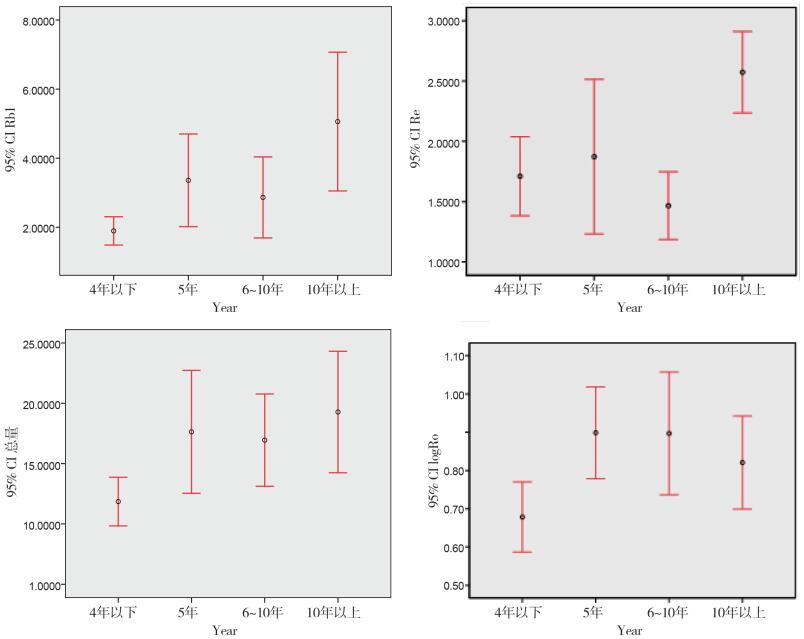
为深入研究红参含量低的原因,我们收集了29批东北产的不同生长年限的人参样品(4年以下9批,5年7批,6~10年7批,10年以上6批),按“3.2”节方法测定含量,采用“SPSS(19.0)”软件,对5种成分的含量及总量数据进行方差分析(ANOVA)。结果,除Rg1、Rf之外,其他P值均小于0.05,说明其余成分在不同年份中有显著性差异。由SNK两两检验和误差条形图可知,10年以上人参中Re、Rb1含量比10年以下的高,Ro含量和总量5年以上区别不大,但都比4年以下的含量高。见图 7。
|
图 7 不同生长年限人参皂苷Rb1、Re、Ro及总量分析图 |
1)人参加工规格较多,除红参外,还有糖参[12]、糖蜜制人参[13]等多种规格,但红参加工过程中不允许加糖,是由鲜人参直接蒸制而成,其自身的总还原糖一般不超过30%[14-17]。此次抽取的111批样品中,约三分之一的样品含糖量超过50%,这严重影响了药材质量,损害了广大群众和用药患者的切身利益,建议严厉打击这种不法行为。
2)红参中主要成分含量较低是其另一个质量问题,经统计分析,可能是使用生长年限较短的人参加工而成,建议加大宣传力度,提倡参农按照传统方式,使用生长年限在5年以上的人参进行加工,保证药材与饮片的质量。
3)经对不同抽样地域、不同地域生产企业、不同被抽样单位性质等进行分析,表明前两者样品质量基本无差异,但抽自生产单位的样品质量较好,抽自经营和使用单位的样品质量相对较差。
4)薄层鉴别不合格的3批样品中有2批检出了西洋参特征成分拟人参皂苷F11,且色谱行为与西洋参相似,提示有西洋参与人参混用现象。
5)在抽验中还发现目前市场上红参名称不规范,如高丽红参、柱参、红柱参、石柱参等,建议对此行为进行统一规范,引导相关单位使用规范名称,便于药品监督管理部门进行统一管理。
| [1] |
孙娜, 徐钢, 徐珊, 等. 人参炮制对其化学成分和药理作用的影响[J]. 中国药房, 2016, 27(6): 857-859. DOI:10.6039/j.issn.1001-0408.2016.06.45 |
| [2] |
赵远, 孙娜, 刘蓬蓬, 等. 生晒参、红参与平性参对气虚大鼠作用的比较研究[J]. 中医药导报, 2014, 20(4): 12-15. |
| [3] |
楚楚, 陈岑, 李行诺, 等. 红参炮制对质量影响的研究进展[J]. 中药材, 2014, 37(5): 901-904. |
| [4] |
赵贤俊, 崔海月, 李性周, 等. 红参虫草胶囊防治早期糖尿病肾病临床观察[J]. 辽宁中医杂志, 2005, 32(7): 667-668. |
| [5] |
中国药典: 一部[S]. 2010: 143.
|
| [6] |
GB/T 5009. 7-2008食品中还原糖的测定[S]. 2008.
|
| [7] |
王越, 孙佳明, 张辉. 人参蒸炖炮制的研究[J]. 长春中医药大学学报, 2015, 31(6): 1130-1131. |
| [8] |
周琪乐, 徐嵬, 杨秀伟. 中国红参化学成分研究[J]. 中国中药杂志, 2016, 41(2): 233-249. |
| [9] |
王海南. 人参皂苷药理研究进展[J]. 中国临床药理学与治疗学, 2006, 11(11): 1201-1206. DOI:10.3969/j.issn.1009-2501.2006.11.001 |
| [10] |
周秋秋, 任谓明, 王艳红, 等. 红参的炮制、化学成分及药理活性研究进展[J]. 上海中医药杂志, 2016, 50(2): 97-99. |
| [11] |
张带荣, 冯丹. 人参皂苷用于肝脏疾病的研究进展[J]. 中国现代应用药学, 2016, 33(5): 671-675. |
| [12] |
GB/T 22539-2008糖参分等质量[S]. 2008.
|
| [13] |
GB/T 22540-2008蜜制人参分等质量[S]. 2008.
|
| [14] |
张浩, 赵景辉, 张瑞, 等. 人参、西洋参制品糖含量特征研究[J]. 人参研究, 2013, 25(2): 6-10. |
| [15] |
齐滨, 刘莉, 赵大庆, 等. 人参、西洋参和红参中糖类含量的比较研究[J]. 中国药房, 2013, 24(7): 616-618. DOI:10.6039/j.issn.1001-0408.2013.07.15 |
| [16] |
陈佳, 刘永利, 崔志海, 等. 红参中总还原糖含量测定及限度值拟定[J]. 中药材, 2016, 39(10): 2247-2250. |
| [17] |
凌益平, 徐兵勇, 刘武, 等. HPLC-ELSD测定红参、麦冬及其制剂中糖的含量[J]. 中国现代应用药学, 2014, 31(11): 1395-1399. |
 2017, Vol. 31
2017, Vol. 31 
