2. 苏州大学, 苏州 215123;
3. 江苏省食品药品监督检验研究院, 南京 210008
2. Soochow University, Suzhou 215123, China;
3. Jiangsu Institute for Food and Drug Control, Nanjing 210008, China
西洋参为五加科植物西洋参Panax quinquefolium L.的干燥根,又名花旗参。其味甘、苦,性凉,归心、肺、肾经,具有补气养阴、清热生津之功效,现代研究表明西洋参具有免疫调节、抗肿瘤、抗氧化、降血糖等作用[1-2],是人们保健补益之佳品。近年来,在中药材的仓储和流通过程中,出现硫磺熏蒸西洋参现象。硫熏后的西洋参饮片色泽白晰,外观水润,其外观优于未经硫磺熏蒸的西洋参,且能够防虫,防霉,延长保质期。但硫熏过程产生的二氧化硫,为活泼的氧化还原剂,对药材的化学成分均有不同程度的影响[3-4]。《中国药典》2010年版第二增补本规定,对药典收载的山药、牛膝、粉葛、甘遂、天冬、天麻、天花粉、白及、白芍、白术、党参等11味药材及其饮片品种限度规定为“二氧化硫残留量不得超过400 mg·kg-1”;对其他中药材及饮片,规定“二氧化硫残留量不得超过150 mg·kg-1” [5]。根据此规定,西洋参二氧化硫残留量不得过150 mg·kg-1。
考虑西洋参饮片较原药材更容易吸附二氧化硫,易受硫磺熏蒸的影响,本文以西洋参饮片为研究对象,模拟库房熏蒸法,对西洋参饮片进行硫磺熏蒸,将二氧化硫残留量分别控制在150 mg·kg-1及其以下(药典规定的合格限度之内)和400 mg·kg-1以上(模拟过度熏蒸),以人参皂苷Rg1、Re、Rb1为指标,考察硫磺熏蒸对其主要活性成分皂苷类成分的影响。
1 仪器与材料美国Waters UPLC超高效液相色谱仪,工作站:Empower 3;梅特勒-托利多XS205DU电子天平;Millipore Milli-Q Reference纯水仪;大德牌DFY-400粉碎机;上海跃进HH.S21-6S电热恒温水浴锅。
人参皂苷Rg1(批号:110703-201128,含量为93.4%)、人参皂苷Re(批号:110754-201123,含量为89.1%)、人参皂苷Rb1(批号:110704-201223,含量为95.9%),均购自中国食品药品检定研究院;供试品由苏州天灵中药饮片有限公司提供,经江苏省食品药品监督检验研究院狄恒建老师鉴定为五加科植物西洋参Panax quinquefolium L.饮片。
2 方法与结果 2.1 西洋参饮片的硫磺熏蒸方法取西洋参饮片供试品,模拟库房熏蒸法对其进行硫磺熏蒸,将二氧化硫残留量分别控制在150 mg·kg-1以下、150 mg·kg-1、400 mg·kg-1以上三级级别。将熏蒸饮片按《中国药典》2010年版第一增补本附录Ⅸ U二氧化硫残留量测定法测定二氧化硫残留量[6]。
二氧化硫残留量测定方法:取西洋参饮片,打粉,过五号筛,取过筛粉末10 g,精密称定,置《中国药典》规定用二氧化硫测定用圆底烧瓶中,加水400 mL,取6 mol·L-1盐酸溶液10 mL加入带刻度分液漏斗中,待回流开始加入烧瓶内。另准备一锥形瓶,加入125 mL水和淀粉指示液1 mL作为吸收液,置于磁力搅拌器上不断搅拌。开通氮气,调整氮气流速为0.2 mL·min-1,至上述锥形瓶内有气泡均匀排出。打开上述分液漏斗活塞,使盐酸溶液流入烧瓶中,摇匀,加热烧瓶内的溶液至沸,并保持微沸3 min,立即用碘滴定液(0.01 mol·L-1)滴定锥形瓶内二氧化硫吸收液,至吸收液显蓝色或蓝紫色持续30 s不完全消退,并将滴定结果用空白试验校正。每1 mL的碘滴定液(0.01 mol·L-1)相当于0.6406 mg的SO2。
2.2 UPLC法测定硫熏西洋参与非硫熏西洋参中人参皂苷Rg1、Re、Rb1的含量 2.2.1 溶液的制备1)对照品储备液的制备:分别取人参皂苷Rg1、Re、Rb1适量,精密称定,置同一10 mL容量瓶中,用甲醇溶解并稀释至刻度,摇匀,使成终浓度分别为241.91、749.33、1583.31μg·mL-1的混合对照品储备液。
2)供试品溶液的制备:将西洋参供试品于60℃干燥2 h,粉碎成中粉,取约0.5 g,精密称定,置250 mL三角锥形瓶内,精密加甲醇50 mL,称定重量,水浴回流1.5 h,放冷,称定重量,用甲醇补足减失重量,摇匀,用0.22 μm微孔滤膜滤过,取续滤液,备用。
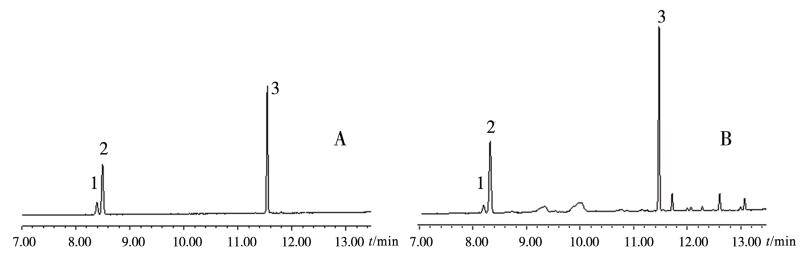
2.2.2 色谱条件及系统适应性试验色谱柱:Acquity BEH C18柱(2.1 mm×100 mm,1.7μm);柱温:40℃;检测波长:203 nm;流速:0.5 mL·min-1;进样量:2μL[7]。采用二元梯度洗脱,洗脱程序见表 1。其中流动相A为乙腈,流动相B为水相。人参皂苷Rg1和人参皂苷Re分离度大于1.5,人参皂苷Rg1、Re、Rb1峰理论板数均超过250000,结果见图 1。
|
|
表 1 西洋参人参皂苷Rg1、Re、Rb1含量测定梯度洗脱程序 |
|
图 1 混合对照品和西洋参供试品的UPLC色谱图 A.混合对照品; B.西洋参供试品; 1.人参皂苷Rg1; 2.人参皂苷Re; 3.人参皂苷Rb1。 |
取“2.2.1”节人参皂苷Rg1、Re、Rb1混合对照品储备液,用甲醇逐步稀释,使人参皂苷Rg1的系列浓度分别为12.10、24.19、72.57、120.95、241.91 μg·mL-1;人参皂苷Re的系列浓度分别为37.47、74.93、224.80、374.67、749.33 μg·mL-1;人参皂苷Rb1的系列浓度分别为79.17、158.33、474.99、791.65、1583.31 μg·mL-1。进样2μL,以对照品浓度为横坐标,峰面积为纵坐标进行线性回归,得回归方程,结果见表 2。
|
|
表 2 人参皂苷Rg1、Re、Rb1标准曲线和线性范围 |
取人参皂苷Rg1、Re、Rb1混合对照品溶液(浓度分别为24.19、74.93、158.33 μg·mL-1),重复进样6次,测定峰面积值,RSD分别为1.0%、0.2%、0.3%,精密度良好。
2.2.5 稳定性试验称取西洋参供试品(苏州天灵,批号:130427-3),按“2.2.1”节方法制备西洋参供试品溶液,分别于0、2、4、8、12、24 h进样,测定人参皂苷Rg1、Re、Rb1峰面积值,RSD分别为2.8%、2.0%、2.6%,表明西洋参供试品在24 h内稳定性良好。
2.2.6 重复性试验称取西洋参供试品(苏州天灵,批号:130427-3),每份约0.5 g,精密称定,共6份,按照“2.2.1”节方法制备供试品溶液,测定峰面积,计算样品中人参皂苷Rg1、Re、Rb1质量分数的平均值分别为0.17%、1.37%、2.98%,RSD分别为2.4%、1.9%、2.6%。
2.2.7 加样回收试验称取西洋参供试品(苏州天灵,批号:130427-3),每份约0.25 g,精密称定,共6份,精密加入人参皂苷Rg1、Re、Rb1混合对照品溶液50 mL,其中,人参皂苷Rg1对照品的加入量为436.03μg,人参皂苷Re对照品的加入量为1554μg,人参皂苷Rb1对照品的加入量为5249.57μg,按照“2.2.1”节方法制备供试品溶液并测定。计算得到人参皂苷Rg1的平均加样回收率为98.8%,RSD为3.2%;人参皂苷Re的平均加样回收率为98.3%,RSD为2.9%;人参皂苷Rb1的平均加样回收率为98.1%,RSD为2.4%,结果见表 3。
|
|
表 3 西洋参中人参皂苷Rg1、Re、Rb1的加样回收率结果(n=6) |
取3批未经硫磺熏蒸的西洋参饮片和其对应的经过硫磺熏蒸的西洋参饮片粉末,每份取约0.5 g,精密称定,平行制备2份供试品溶液并进行含量测定,结果见表 4。
|
|
表 4 西洋参供试品中人参皂苷Rg1、Re、Rb1的含量测定(n=2) |
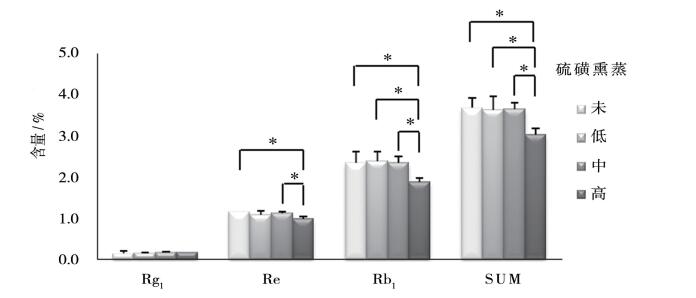
根据表 4中的测定结果,采用方差分析法分别比较硫磺熏蒸前后西洋参中人参皂苷Rg1、Re、Rb1的含量及三者总含量,结果如图 2所示。
|
图 2 硫磺熏蒸组西洋参与未熏蒸组西洋参中人参皂苷Rg1、Re和Rb1的比较 低剂量组SO2残留量<150 mg·kg-1;中剂量组SO2残留量约为150 mg·kg-1;高剂量组SO2残留量>400 mg·kg-1。 |
方差分析结果表明:1)硫磺熏蒸前后,西洋参中人参皂苷Rg1含量无显著性差异,说明硫磺熏蒸对西洋参中人参皂苷Rg1的含量无显著性影响。2)经过高剂量硫磺熏蒸的西洋参组与未熏蒸组相比较,人参皂苷Re含量存在显著性差异,说明硫磺熏蒸至西洋参中二氧化硫残留量>400 mg·kg-1时,会引起西洋参中人参皂苷Re含量的显著性降低;硫磺熏蒸中剂量组与高剂量组西洋参人参皂苷Re存在显著性差异,且低、中剂量组与未熏蒸组西洋参相比,人参皂苷Re不存在显著性差异,说明硫磺熏蒸至西洋参中二氧化硫残留量至150 mg·kg-1时,成为一个分水岭。本试验表明二氧化硫残留量在150 mg·kg-1及以下,西洋参中的人参皂苷Re含量不受显著性影响。3)经过高剂量硫磺熏蒸的西洋参组与未熏蒸组、低剂量组、中剂量组西洋参相比较,人参皂苷Rb1含量均存在显著性差异,说明硫磺熏蒸至西洋参二氧化硫残留量>400 mg·kg-1时,会引起西洋参中人参皂苷Rb1含量的显著性降低;未熏蒸组与低、中剂量组西洋参人参皂苷Rb1不存在显著性差异,说明二氧化硫残留量在150 mg·kg-1及以下,西洋参中的人参皂苷Rb1含量不受显著性影响。4)硫磺熏蒸高剂量组与未熏蒸组、低剂量组、中剂量组西洋参相比较,人参皂苷Rg1、Re和Rb1三者总量均存在显著性差异,说明硫磺熏蒸至西洋参二氧化硫残留量>400 mg·kg-1时,会引起西洋参中人参皂苷Rg1、Re和Rb1三者总量的显著性降低;但未熏蒸组与低、中剂量组相比,人参皂苷Rg1、Re和Rb1三者总量不存在显著性差异,说明二氧化硫残留量在150 mg·kg-1及以下时,西洋参中人参皂苷Rg1、Re和Rb1三者总量不受显著性影响。
3 讨论1)人参皂苷Rg1、Re和Rb1是西洋参中含量较高的3个特征性皂苷成分,也是《中国药典》[8]西洋参含量测定项下的指标成分,本文通过测定三者含量来考察硫磺熏蒸对其产生的影响。结果表明,硫磺熏蒸后人参皂苷Rg1、Re和Rb1总量均符合《中国药典》规定,总量不少于2.0%;但当硫磺熏蒸西洋参导致二氧化硫残留量大于400 mg·kg-1时,能够引起人参皂苷Re、Rb1含量及人参皂苷Rg1、Re和Rb1三者总量的显著性降低。当二氧化硫残留量小于等于150 mg·kg-1时,人参皂苷Rg1、Re和Rb1的含量和总量基本不受影响。本文选取3批次西洋参饮片,经过控制硫磺熏蒸程度,使其二氧化硫残留量分别控制在150 mg·kg-1以内、400 mg·kg-1以上,基本能够证明药典规定的西洋参二氧化硫残留量不得大于150 mg·kg-1有其科学合理性。但对150~400 mg·kg-1二氧化硫残留量的样本尚缺少考察,有待进一步的试验。
2)硫磺熏蒸产生的二氧化硫气体遇水能够生成亚硫酸,再遇空气能够氧化生成硫酸,可与人参皂苷母核或糖基上的羟基发生磺酸化反应。有文献报道[9-10],人参经过硫熏后生成磺酸化人参皂苷Re和磺酸化人参皂苷Rb1,推测西洋参硫熏后可能也容易使人参皂苷Re、Rb1发生磺化反应,从而引起含量的降低。
3)《中国药典》西洋参项下人参皂苷Rg1、Re和Rb1含量测定采用水饱和的正丁醇水浴回流提取,经过比较,发现用甲醇水浴回流提取,加样回收率也较好,因此采用甲醇提取,该方法较药典方法简单。且《中国药典》采用HPLC检测,分析时间长达2 h左右,本文采用UPLC法进行测定,可对人参皂苷Rg1、Re、Rb1进行快速高效的含量测定。
4)试验结果表明,过度的硫磺熏蒸西洋参能显著降低其皂苷类成分的含量,影响西洋参品质,且西洋参饮片质地泡松,表面积大,容易吸附二氧化硫,造成二氧化硫超标,为了公众健康,并不提倡硫磺熏蒸西洋参。建议采用更为科学合理的存贮方法来延长西洋参的保质期和保持其品质。
| [1] |
王艳红, 刘中申, 关枫, 等. 西洋参及其制剂的免疫调节作用研究[J]. 中医药学刊, 2004, 22(3): 566-567. |
| [2] |
张酉珍, 苏光悦, 夏晓艳, 等. 天然达玛烷型皂苷降血糖作用的研究进展[J]. 中草药, 2016, 47(8): 2758-2763. |
| [3] |
孙艳菲, 牛韬, 刘静静, 等. 硫磺熏蒸中药材现状及解决措施[J]. 辽宁中医药大学学报, 2015, 17(1): 125-127. |
| [4] |
Ma Xiao-qing, Kai Man Leung Alexander, Chan Chi Leung, et al. UHPLC UHD Q-TOF MS/MS Analysis of the Impact of Sulfur Fumigation on the Chemical Profile of Codonopsis Radix(Dangshen)[J]. Analyst, 2014, 139: 505-516. DOI:10.1039/C3AN01561K |
| [5] |
中国药典: 第二增补本[S]. 2010: 180.
|
| [6] |
中国药典: 第一增补本[S]. 2010: 262.
|
| [7] |
吴银生, 闵春艳. 不同参类中人参皂苷Rg1、Re、Rb1的质量测定[J]. 抗感染药学, 2011, 8(2): 106-108. |
| [8] |
中国药典: 一部[S]. 2015: 132.
|
| [9] |
周珊珊, 徐金娣, 沈红, 等. UPLC-Q-TOF-MS/MS结合对照药材法快速筛查硫磺熏蒸商品人参[J]. 中国中药杂志, 2014, 39(15): 2807-2813. |
| [10] |
Jin Xin, Zhu Lingying, Shen Hong, et al. Influence of Sulphur-fumigation on the Quality of White Ginseng:A Quantitative Evaluation of Major Ginsengsides by High Performance Liquid Chromatography[J]. Food Chemistry, 2012, 135: 1141-1147. DOI:10.1016/j.foodchem.2012.05.116 |
 2017, Vol. 31
2017, Vol. 31 
