2. 中国食品药品检定研究院, 北京 102600
2. National Institutes for Food and Drug Control, Beijing 102600, China
纠正和预防措施系统[1](Corrective Action and Preventive Action System,CAPAs)是以风险管理为依据,通过施行一些程序,识别、预防和消除潜在的或已经发生不合格的文件的集合。CAPAs是质量管理过程中一个非常重要的环节,被形象地描述为质量体系的“免疫系统”,是持续改进产品质量和保证质量管理体系运行的关键工具之一。CAPAs一般通过收集问题、分析原因、采取措施、有效性追踪等程序,解决已经发生的问题,同时达到防止问题再次发生的目的。
医疗器械技术审评事关公众用械安全,建立可持续改进的医疗器械质量评价体系对于公众健康意义重大,CAPAs做为质量管理的有效手段,未见其在该领域应用的相关报道。由此,本文就医疗器械技术审评过程中CAPAs的构建进行了简要介绍,并对其中涉及到的问题进行了初步探讨,以期能为相关研究者提供借鉴。
1 相关背景CAPAs的应用由来已久,尤其是在医药行业[2],应用更加广泛,并且取得了较好的效果。世界卫生组织的《药品生产质量管理规范》(GMP)第二章规定“出现的任何重大偏差都应完全记录下来并进行调查,分析上市产品的用户投诉,调查质量缺陷的原因,提出改进缺陷的措施和防止再发生缺陷的预防措施。”讲的就是要在生产过程中建立CAPAs。人用药品注册技术要求国际协调会议ICH Q10药品质量体系模型中明确指出:CAPAs、工艺性能和产品质量监测系统、变更管理系统、管理评审组成了药品质量体系的四要素[3]。
美国FDA也很重视CAPAs,在美国联邦法规第21章820部分中,明确了对质量管理体系建立CAPAs的要求,即CAPAs运行的七步法:识别、调查、制定措施、评估措施、实施措施、有效性验证、文件归档[4-6]。CAPAs是FDA质量体系审核的重要关注点之一,历年FDA开出的不符合项中,CAPAs问题排名居前二位。
我国颁布的《药品生产质量管理规范(2010年修订)》,在“质量控制与质量保证”章节中新设了“纠正措施和预防措施”一节,明确企业应建立CAPAs[5]。我国《医疗器械生产质量管理规范》第七十四条规定,企业应当建立纠正措施程序,确定产生问题的原因,采取有效措施,防止相关问题再次发生[7]。所以,对于医药产业而言,CAPAs是质量体系的关键要素之一,是企业产品质量控制不可或缺的重要组成部分[8]。
2 医疗器械技术审评CAPAs的构建CAPAs的主要目的不仅仅是纠正某一项或几项缺陷,而是要查找根本原因,采取相应的纠正或预防措施,防止问题的重复发生[9]。CAPAs的实施过程一般包括七个步骤:问题识别、原因分析、措施制定、措施评估、措施执行、有效性追踪、归档留存。基于医疗器械技术审评的特殊性,其CAPAs的构建在上述步骤的基础上,又有进一步的细化和调整,具体如下。
2.1 CAPAs框架结构技术审评CAPAs文件架构共分为三个层次,第一层次是程序性文件,包括CAPA大流程及七个环节的程序文件;第二个层次是操作规范,涵盖了11类常见的技术审评问题;第三个层次是各种记录文件及表单。
程序文件是规定各项活动程序的文件,是CAPAs的核心,是各项操作规范的编制依据,共包括《医疗器械技术审评CAPA总流程》《问题识别程序》《调查分析程序》等7个CAPAs程序文件,对于CAPA的发起、运行、流向及各环节分工都进行了明确的界定。
操作规范是程序文件的细化,具体规定各种工作的规则和要求。对于技术审评中遇到的问题,CAPAs建立了针对性的操作规范,如受理错误、审评错误、超时限、设备损毁等。对于导致错误的可能原因,规范进行了汇总,并提供了相应的纠正或预防措施供参考。譬如审评错误,可能涉及到的原因如审评流程有缺漏、技术依据和要求不全面、培训不到位等。相应的纠正措施包括完善审评流程、加强培训、制定更加全面的技术审评依据等。
记录文件是各种活动和活动结果的客观描述,是判定体系是否正常运行的证明性材料。记录和表单一般有原始记录、统计报表和分析报告三种形式。为确保CAPAs符合要求且可追溯,执行过程需填写程序和规范要求的各项记录,这也是质量体系的要求[10]。CAPAs从启动到关闭,各程序执行过程中所有的记录和表单均需归档留存。
2.2 CAPAs流程CAPAs的启动来源于技术审评的各个方面,如投诉抱怨、内部审核、定期质量数据分析等,但并不是所有的不符合项都需要启动CAPAs,要按照风险程度进行判定。若通过识别发现无需启动CAPAs,则需形成分析报告上报质量管理负责人批准即可。若不符合项发生情况比较紧急,为防止不利影响的恶化,需立即实施紧急补救措施进行纠正,该补救措施由发生问题的部门负责人最终确定[11]。
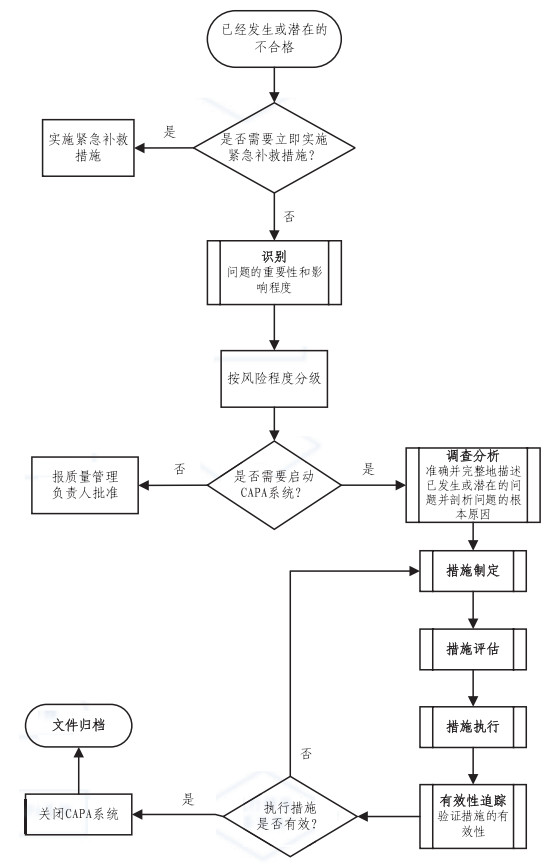
当确定启动CAPAs,则进入调查分析程序,针对调查目标制定完整的问题调查计划,确保所有关键因素均在调查范围内,通过收集可能导致问题的数据,剖析可能的根本原因;根据问题严重程度级别,制定措施计划,经相关审核部门评估后实施;措施执行过程中,需确保所有在措施计划中列出和描述的任务,都要被发起、完成,通过有效性跟踪,对措施实施后结果和执行方法的有效性进行评估和认定,完成一系列验证,最终判定是否关闭CAPAs。上述活动均应有效记录,形成文件并归档。具体流程见图 1。
|
图 1 医疗器械技术审评CAPAs运行流程 |
CAPAs数据库是质量体系的重要组成部分,也是管理评审的重要输入,可为质量体系的改进提供有效依据[12]。数据的汇总应贯穿于CAPAs的全过程,以确保完整性和有效性。数据的记录应翔实,至少包括发现日期、发现部门和人员、基本情况、采取措施、效果及验证等。为保证数据的有效性,还需对数据进行分析处理,定期形成相应的汇总分析报告,并按一定规则进行编号,如风险级别、CAPAs质量问题类型、发生年份等。
数据汇总和分析对于审评质量的提高和审评尺度的统一有重要意义,也是风险判定的主要依据[13]。通过对历史数据的分析,可以判断是否需要启动CAPAs,还是仅完成纠正即可。定期对数据记录进行回顾和统计分析,可判断所采取的纠正和预防措施的有效性,并可对不符合项趋势进行分析预判,为组织决策提供参考,以确保技术审评质量的不断提高[14-16]。
3 讨论 3.1 CAPAs应贯穿于技术审评全生命周期技术审评是一个系统的工程,每一个环节出现问题,都会对最终的审评结果带来一定的影响[17]。从申报资料受理到分配、审评、复核、签发,都需要在质量管理体系框架内建立职责明确、程序清晰、操作规范的CAPAs,确保每一环节操作的规范性。
CAPAs的启动应涵盖技术审评的全生命周期,如问卷调查、投诉、数据分析、案卷评查、内审、管理评审、审计等[18]。另外,对于发生的不合格问题,其原因也会涉及技术审评的各个方面,譬如发生审评错误,可能需要从职员培训是否到位、已有的审评要点是否涵盖该产品、审评流程是否合规、制度机制有无缺陷、审评资料是否齐全、是否按照标准操作规程(SOP)进行审评、审评有无外界干扰、是否曾经发生过类似问题及原因和采取的措施等多个方面进行分析。
3.2 CAPAs应权责明确在CAPAs每个程序中都应明确责任人和辅助人员的职责,如信息收集、调查取证、审查、实施、配合、监督等,只要做到分工明确,权责清晰,才能确保CAPAs的顺利推进。
CAPAs每个岗位的人员构成和职责都应明确,如调查小组由不符合项关联性较弱部门相关人员组成,根据不符合情况制定相应调查计划,以确保所有关键因素均被识别、调查,为进一步识别根本原因打好基础;CAPA审核小组由中心领导和各处室负责人组成,对高风险CAPAs进行审核,并对实施过程进行审核监督;纠正/预防措施负责人的职责是组织调查及原因分析,并根据调查结果要求责任部门确定和实施改进措施。
3.3 CAPAs应建立分级管理机制基于医疗器械的特殊性,对于在审评中发现的问题,应按照风险进行分级评估,并采用不同的处理方式,一方面可以提高效率,另一方面对于可预见的风险,做到提前控制,最大程度地避免风险的扩大,以确保风险的可控性[19]。
CAPAs的分级与风险管理密不可分[20],其风险等级的建立一般通过科学的统计工具,对既往不符合项发生的概率和危害程度进行综合评估,依据评估结果和审评实际确定等级评定标准。
风险等级与危害的大小和发生的频率两个因素密切相关。对于危害大的问题,一般都会得到重视优先处理,对于一些危害小但发生频率却很高的问题,很有可能被忽视。如审评报告书写错误、行政相对人的抱怨等。对于这些危害不大,发生频率较高的问题,发生应当引起足够的重视,认真分析根本原因和不良趋势,及时采取相应的措施。
| [1] |
ISO 9001: 2008 Quality Management SystemsRequirements[S]. 2008.
|
| [2] |
ICH. Q10 Pharmaceutical Quality System[S]. 2009.
|
| [3] |
FDA. FDA 21 CFR Part 820 Quality System Regulation[S]. 2017.
|
| [4] |
FDA. FDA21 CFR 820.100 Quality System Regulation: Corrective and Preventive Action[S]. 2017.
|
| [5] |
卫生部令第79号药品生产质量管理规范[S]. 2011.
|
| [6] |
国家食品药品监督管理总局公告2014年第64号医疗器械生产质量管理规范[S]. 2015.
|
| [7] |
刘祝东. 探讨新版GMP中偏差处理、纠错和预防措施、变更控制在质量管理活动中的运用[J]. 中国药事, 2012, 26(6): 646-649. DOI:10.3969/j.issn.1002-7777.2012.06.031 |
| [8] |
戴锦玲. 探析制药企业纠正和预防措施体系的管理[J]. 化工管理, 2016, 12: 113. |
| [9] |
丁晓玥, 梁毅. 制药企业质量管理体系中纠正与预防措施(CAPA)的实施[J]. 中国制药装备, 2011, 2(2): 16-19. |
| [10] |
马汝孟, 荣晓阳. CAPA-药品生产质量持续改进的利器[J]. 沈阳药科大学学报, 2014, 5(31): 411-415. |
| [11] |
迈克尔·拉帕波特. 质量管理系统和业务管理系统的融合[J]. 质量译丛, 2014, 5: 27-29. |
| [12] |
郑士辉, 娄玲珠. 制药企业纠正和预防措施(CAPA)体系的建立[J]. 中国现代药物应用, 2011, 5(5): 10. DOI:10.3969/j.issn.1673-9523.2011.05.006 |
| [13] |
吕宏光, 张虎. 医疗器械企业如何有效实施纠正和预防措施[J]. 中国医疗器械信息, 2013(7): 27-31. DOI:10.3969/j.issn.1006-6586.2013.07.007 |
| [14] |
裴欢, 孙玉凤, 邓翀. 药品生产质量管理中偏差的纠正预防措施效果评估[J]. 首都食品与医药, 2015(7): 10-12. |
| [15] |
于庆华, 张璇. 药品生产的偏差处理[J]. 上海医药, 2016, 37(11): 74-77. |
| [16] |
张利英, 郑强. 我国药企纠正和预防措施管理研究分析[J]. 中国新药杂志, 2015, 24(17): 1968-1974. |
| [17] |
李丽莉, 卢大伟, 白东亭, 等. 医疗器械产业发展机遇的探讨[J]. 中国药事, 2017, 31(6): 622-625. |
| [18] |
刘清峰, 刘洋, 蒋海洪, 等. 基于监管科学的医疗器械监管人才培养探索设计[J]. 中国药事, 2018, 32(11): 1500-1504. |
| [19] |
吴丹. 基于PDCA循环模式优化医疗器械技术审评质量的设想[J]. 中国药事, 2018, 32(6): 715-718. |
| [20] |
孙健, 朴惠顺, 李英姬. 对药品GMP质量管理体系中变更控制、偏差管理、质量风险管理的探讨[J]. 中国药事, 2018, 32(1): 88-91. |
 2019, Vol. 33
2019, Vol. 33 
