2. 株洲千金药业股份有限公司, 株洲 412003
2. Zhuzhou Qianjin Pharmaceutical Co., Ltd., Zhuzhou 412003, China
鸡血藤为豆科植物密花豆Spatholobus suberectus Dunn的干燥藤茎。秋、冬二季采收,除去枝叶,切片,晒干。具有活血补血、调经止痛、舒筋活络之功效,用于月经不调,痛经,经闭,风湿痹痛,麻木瘫痪,血虚萎黄[1]。鸡血藤化学成分复杂,药理活性多样,作为一种传统的活血补血中药,药用历史久远,大量应用于中成药处方,是一味临床利用率较高的活血补血中药[2-5]。自《中华人民共和国药典》(以下简称《中国药典》)1977年版首次收载鸡血藤,历版均沿用收载,且基原相同[2]。鸡血藤现行标准收载于《中国药典》2015年版,检验项目包括【性状】【鉴别】【检查】等[1],尚缺少化学成分信息相关的质量控制项,存在进一步提高与完善的空间。本研究在对15批鸡血藤饮片进行现行标准质量控制项目检测的基础上,进一步优化了薄层鉴别方法,同时建立了能够充分体现本品化学成分信息的HPLC指纹图谱,及其主要成分儿茶素和表儿茶素的含量测定方法,为全面、有效地控制本品质量提供了科学依据。
1 仪器与试药Waters 2690高效液相色谱系统(包括Waters 2690液相色谱仪、PDA紫外检测器,美国Waters公司)。METTLER XS105型电子分析天平(瑞士Mettler公司);Milli-Q超纯水处理系统(美国Millipore公司);KQ-300DA型数控超声波清洗仪(中国昆山市超声仪器有限公司)。
儿茶素、表儿茶素、原儿茶酸、没食子酸、原儿茶醛、大豆苷、染料木苷、大豆苷元、染料木素、芒柄花素对照品(批号分别为110877- 201604、110878-201703、111809-201205、110831-201605、110810-201608、111738- 201603、111709-201702、111502-200402、111704-201703、111703-201504,中国食品药品检定研究院);乙腈、甲酸(色谱纯,Fischer公司),甲醇、乙酸乙酯(分析纯,国药化学试剂有限公司)。
15批鸡血藤样品(批号分别为20160901、20160902、20161001、20161002、20161003、1611001、1612001、1612002、1612003、1701001、1701002、1701003、1702001、1702002、1702003,编号分别为1~15)以及市场收集鸡血藤样品2份(编号为16~17)、鸡血藤伪品3批(分别为大血藤、雷公藤、过岗龙,编号为18~20)均由株洲千金药业股份有限公司提供,并经中国食品药品检定研究院张南平主任药师、康帅副研究员鉴定,鸡血藤来源于豆科植物密花豆Spatholobus suberectus Dunn,大血藤来源于木通科植物大血藤Sargentodoxa cuneata(Oliv.)Rehd. Et Wils.,雷公藤来源于卫矛科植物雷公藤Tripterygium wilfordii J.D. Hooker,过岗龙来源于豆科植物榼藤Entada phaseoloides(Linnaeus)Merrill。
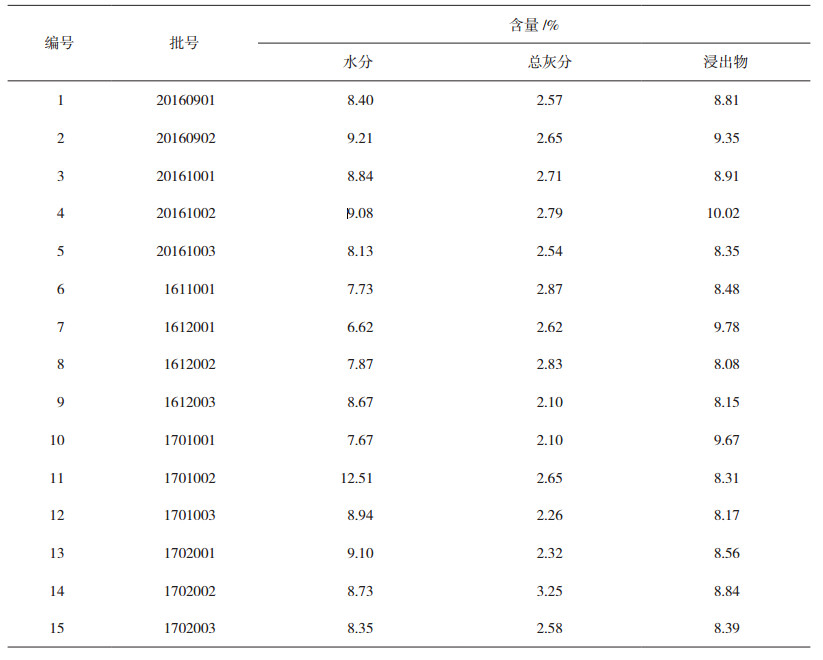
2 标准检测取鸡血藤样品粉末适量,分别按照《中国药典》2015年版一部鸡血藤项下规定的水分、总灰分和浸出物测定方法对15批鸡血藤饮片进行检测,结果均符合标准规定,测定结果见表 1。
|
|
表 1 测定结果 |
取芒柄花素对照品适量,精密称定,用甲醇溶解,制成每1 mL中约含0.1 mg的对照溶液。
取对照药材粉末1 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,密塞,称定重量,超声处理(功率300 W,频率50 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,滤过,精密量取续滤液10 mL,蒸干,残渣加水10 mL使溶解,用乙酸乙酯10 mL萃取2次,合并乙酸乙酯萃取液,蒸干,残渣加甲醇溶解于2 mL量瓶,甲醇稀释至刻度,0.45 μm微孔滤膜滤过,即得。
3.1.2 供试品溶液制备取鸡血藤样品适量,粉碎,取粉末1 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,密塞,称定重量,超声处理(功率300 W,频率50 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,滤过,精密量取续滤液10 mL,蒸干,残渣加水10 mL使溶解,用乙酸乙酯10 mL萃取2次,合并乙酸乙酯萃取液,蒸干,残渣加甲醇溶解于2 mL量瓶,甲醇稀释至刻度,0.45 μm微孔滤膜滤过,即得。
3.1.3 展开与检视照薄层色谱法(通则0502)试验,分别吸取供试品溶液、对照药材、对照品溶液各5 μL,点于同一硅胶G薄层板上,以三氯甲烷-甲醇(20:1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材、对照品色谱相应的位置上,显相同颜色的斑点。
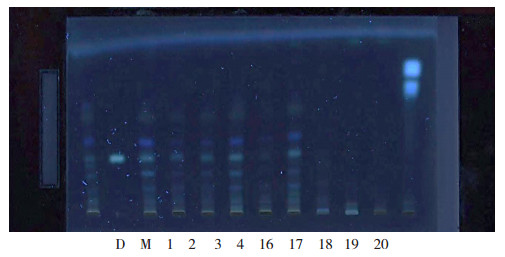
3.1.4 样品检测按“3.1.3”节下展开与检视条件对15批饮片及市场收集正伪品进行薄层色谱鉴别,代表性TLC图见图 1。在此条件下斑点分离较好,显色清晰,且15批饮片的薄层鉴别结果一致性较好,能区分正伪品。
|
D.对照药材;M.芒柄花素;1 ~ 4及16 ~ 17.样品;18 ~ 20.伪品。 图 1 鸡血藤饮片及伪品薄层色谱图 |
取原儿茶酸对照品适量,用甲醇溶解,制成每1 mL中约含0.1 mg的混合对照溶液,0.45 μm微孔滤膜滤过,即得。
3.2.2 供试品溶液制备同薄层色谱鉴别“3.1.2”节方法。
3.2.3 色谱条件色谱柱:Agilent Zobarx SB C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)和0.1%甲酸(B)梯度洗脱(0~5 min,3%A~8%A;5~20 min,8%A~10%A;20~45 min,10%A~20%A;45~100 min,20%A~43%A;100~105 min,43%A~85%A);检测波长:260 nm;进样体积:10 μL;流速:1 mL· min-1。
3.2.4 方法学考察 3.2.4.1 精密度取同一供试品溶液(批号1702002),按“3.2.3”节下色谱条件重复进样6次,记录色谱图。以原儿茶酸为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明,各特征峰的相对保留时间和相对峰面积的RSD分别为0.1%~0.4%、0.2%~1.3%,表明仪器精密度良好。
3.2.4.2 重复性取同一批次鸡血藤样品(批号1702002),按“3.2.2”节下方法制备6份供试品溶液,按“3.2.3”节下色谱条件进样测定,记录色谱图。以原儿茶酸为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明,各特征峰的相对保留时间和相对峰面积的RSD分别为0.1%~0.5%、0.7%~5.3%,表明方法重复性良好。
3.2.4.3 稳定性取同一供试品溶液(批号1702002),分别于0、6、12、18、24 h,按“3.2.3”节下色谱条件进样测定,记录色谱图。以原儿茶酸为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明,各特征峰的相对保留时间和相对峰面积的RSD分别为0.1%~0.4%、0.3%~3.5%,表明供试品溶液在24 h内稳定。
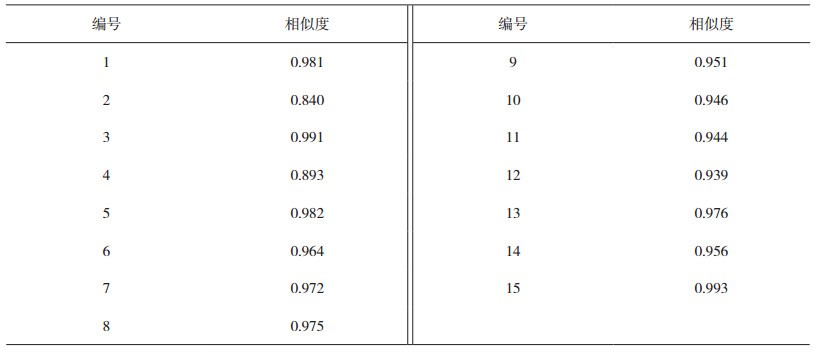
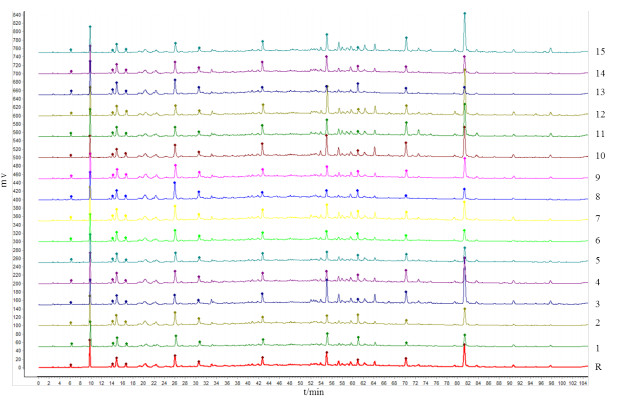
3.2.5 指纹图谱的建立与分析取15批鸡血藤饮片样品,按“3.2.2”节下方法制备供试品溶液,按“3.2.3”节下色谱条件进样测定,记录色谱图。结果导入国家药典委员会开发的《中药色谱指纹图谱相似度评价系统研究版》(2012年版),对15批鸡血藤样品进行数据处理,建立了指纹图谱(见图 2),相似度计算结果见表 2。结果显示,所有样品指纹图谱相似度均高于0.8,其中13批样品相似度高于0.9。
|
R.对照指纹图谱;1~15.样品。 图 2 鸡血藤饮片HPLC指纹图谱 |
|
|
表 2 相似度计算结果 |
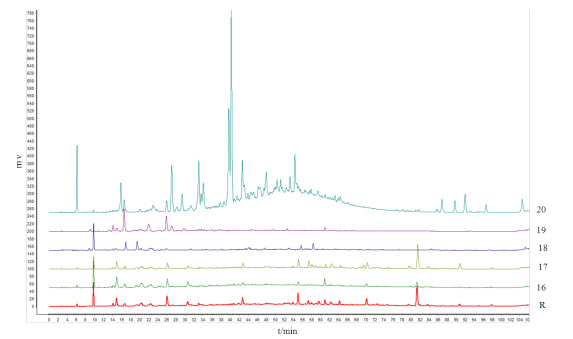
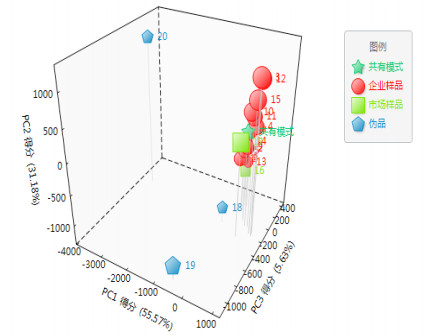
研究同时发现,上述指纹图谱可有效区分市场收集的鸡血藤正品与伪品,如图 3所示。其中鸡血藤样品16、17相似度计算结果分别为0.807、0.945,而伪品大血藤(18)、雷公藤(19)和过岗龙(20)的相似度计算结果分别为0.377、0.272、0.051,且其图谱与鸡血藤对照指纹图谱明显不同。另外,将所有样品谱图导入ChemPattern软件进行主成分分析,PCA得分图(见图 4)可区分鸡血藤样品与伪品。
|
R.对照指纹图谱;16~17.鸡血藤正品;18~20.鸡血藤伪品。 图 3 鸡血藤正伪品HPLC谱图 |
|
图 4 鸡血藤正伪品主成分分析得分图 |
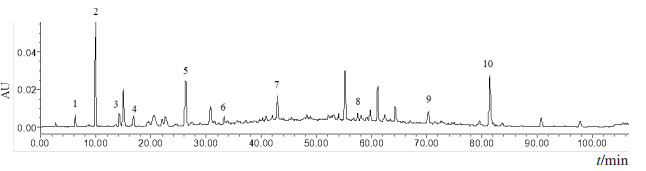
此外,通过与对照品比较,经保留时间与紫外吸收光谱比对,指认样品中10个共有色谱峰(见图 5),编号1~10分别标记为没食子酸(6.3 min)、原儿茶酸(9.9 min)、原儿茶醛(14.2 min)、儿茶素(16.8 min)、表儿茶素(26.2 min)、大豆苷(33.2 min)、染料木苷(42.9 min)、大豆苷元(57.5 min)、染料木素(70.3 min)、芒柄花素(81.4 min)。
|
1.没食子酸;2.原儿茶酸;3.原儿茶醛;4.儿茶素;5.表儿茶素;6.大豆苷;7.染料木苷;8.大豆苷元;9.染料木素;10.芒柄花素。 图 5 鸡血藤饮片HPLC指纹谱图 |
取儿茶素、表儿茶素对照品适量,用甲醇溶解,分别制成每1 mL中约含0.1 mg、1 mg的对照溶液,0.45 μm微孔滤膜滤过,作为混合对照品储备溶液。
3.3.2 供试品溶液制备取鸡血藤样品适量,粉碎,取粉末1 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,密塞,称定重量,超声处理(功率300 W,频率50 kHz)30 min,放冷,用甲醇补足减失的重量,滤过,取续滤液用0.45 μm微孔滤膜滤过,即得。
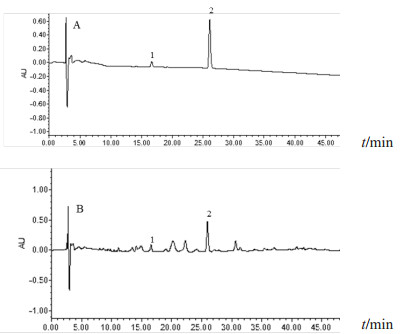
3.3.3 色谱条件色谱柱:Agilent Zobarx SB C18柱(250 mm×4.6 mm, 5 μm);流动相:乙腈(A)和0.1%甲酸(B)梯度洗脱(0~5 min,3%A~8%A;5~20 min,8%A~10%A;20~45 min,10%A~20%A;45~55 min,20%A~85%A;55~60 min,85%A);检测波长:202 nm;进样体积:10 μL;流速:1 mL· min-1。色谱图如图 6所示:
|
A.对照品;B. 样品(1. 儿茶素;2. 表儿茶素)。 图 6 鸡血藤饮片 HPLC 含量测定谱图 |
取“3.3.1”节下混合对照品溶液分别用甲醇稀释成系列浓度,按“3.3.3”节下色谱条件分别进样,以质量为横坐标X,峰面积为纵坐标Y,绘制标准曲线并进行线性回归。结果儿茶素、表儿茶素分别在0.00999~0.499 μg、0.0503~2.014 μg范围内线性关系良好,其线性范围、回归方程、相关系数见表 3。
|
|
表 3 儿茶素、表儿茶素的线性、检出限、定量限 |
将对照品溶液稀释至不同浓度,进样测定,以信噪比3:1为检出限、10:1为定量限,测定结果见表 3。
3.3.4.3 精密度取同一供试品溶液(批号1 7 0 2 0 0 2),按“3.3.3”节下色谱条件重复进样6次,记录色谱图。儿茶素与表儿茶素的峰面积RSD分别为2.9%、0.6%,表明方法精密度良好。
3.3.4.4 重复性分别取同一批鸡血藤样品(批号1702002)6份,精密称定,按“3.3.2”节下方法制备供试品溶液,按“3.3.3”节下色谱条件进样测定。以干燥品计,结果测得儿茶素的含量分别为0.044%、0.041%、0.045%、0.045%、0.045%、0.045%,RSD为3.6%;表儿茶素的含量分别为0.17%、0.16%、0.17%、0.17%、0.17%、0.17%,RSD为1.6%。表明方法重复性良好。
3.3.4.5 稳定性取同一供试品溶液(批号1702002),分别于0、6、12、18、24 h,按“3.3.3”节下色谱条件进样测定,记录色谱图。儿茶素与表儿茶素的峰面积RSD分别为3.2%、0.7%,表明供试品溶液在24 h内稳定性良好。
3.3.4.6 加样回收率精密称取已测知儿茶素、表儿茶素含量的鸡血藤样品0.5 g,共6份,分别置具塞锥形瓶中,精密加入儿茶素、表儿茶素质量浓度分别为0.0858、0.3588 mg·mL-1的对照品溶液2 mL,精密加入甲醇18 mL,密塞,称量,超声(功率300 W,频率50 kHz)处理30 min,放冷,用甲醇补足减失的量,滤过,取续滤液用0.45 μm微孔滤膜滤过,即得供试溶液。进样测定,结果儿茶素与表儿茶素的平均回收率分别为107.0%、105.8%,RSD分别为3.4%、2.9%。
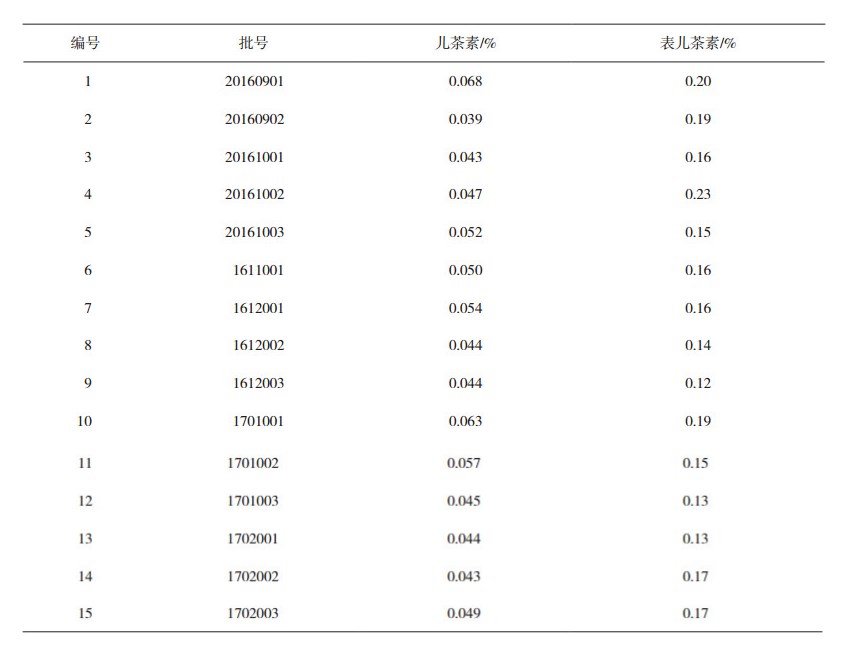
3.3.5 样品测定15批样品按“3.3.2”节制备供试品溶液,按“ 3. 3. 3 ”节下色谱条件进样测定。以干燥品计,样品中儿茶素与表儿茶素含量分别为0.039%~0.068%、0.12%~0.23%,详见表 4。
|
|
表 4 含量测定结果 |
由于鸡血藤含有较多鞣质成分,易对其他化学成分分析造成干扰[6-9]。因此,试验过程中考察药材粉末甲醇、乙醇、60%甲醇直接超声提取以及提取后乙酸乙酯、正丁醇分别萃取等前处理方式,结果表明,采用甲醇超声提取后乙酸乙酯萃取可较大程度地减少样品中所含鞣质类成分引起的干扰。
4.2 色谱条件考察了Agilent Zobarx SB C18、Agilent TC C18、Phenomix Gemini C18、Waters Symmetry shield C18等不同型号色谱柱,以及乙腈-0.1%甲酸、乙腈-0.1%磷酸溶液、乙腈-水等不同流动相体系。结果显示,采用Agilent Zobarx SB C18柱、乙腈-0.1%甲酸梯度洗脱能够较好分离样品中色谱峰。指纹图谱分析考察发现UV 260 nm波长下样品中色谱峰信息丰富,背景噪音低。含量测定考察发现UV 202 nm波长下,检测成分色谱峰分离较好,尽管甲酸在末端波长有吸收,但并未干扰指标成分分析,且方法学考察符合含量测定有关要求。
4.3 薄层色谱鉴别试验首先参照《中国药典》2015年版一部鸡血藤薄层鉴别项下展开系统与检视条件,结果发现该条件下正伪品呈现斑点较为相似,难以有效区分,因而进一步通过条件摸索发现三氯甲烷-甲醇(20:1)展开,紫外光灯(365 nm)检视样品斑点清晰,而伪品则无相应斑点出现。
4.4 指纹图谱鸡血藤饮片中所含化学成分极性差异较大,本研究所建立指纹图谱能够较为全面地反映不同极性的化学成分信息。从相似度计算结果来看,鸡血藤饮片相似度均高于0.8,分析显示不同批次样品所含主要色谱峰基本一致,主要差别在于部分色谱峰峰面积存在一定差异。此外,所建立指纹图谱能够明显区分大血藤、雷公藤和过岗龙等鸡血藤伪品。
4.5 含量测定试验过程中发现,鸡血藤中含量较高的成分主要集中于极性相对较大的水溶性成分,结合文献报道[10-16],研究建立了本品儿茶素和表儿茶素的含量测定方法。从测定结果来看,儿茶素含量整体较低,表儿茶素含量较高,可选择表儿茶素作为本品含量测定指标成分。
综上所述,本研究针对鸡血藤所含化学成分特点,优化并研究建立了薄层色谱鉴别、指纹图谱及含量测定的多维质量控制方法,为更全面、有效地控制与评价产品质量,以及本品质量标准的进一步提高与完善提供了科学依据。
| [1] |
中国药典: 一部[S]. 2015: 194.
|
| [2] |
秦双双, 朱艳霞, 韦坤华, 等. 鸡血藤的本草沿革与黄酮类成分及其药理学研究进展[J]. 中国中药杂志, 2018, 43(11): 2216-2223. |
| [3] |
余弯弯, 双鹏程, 张凌. 鸡血藤化学成分及药理作用研究概况[J]. 江西中医药大学学报, 2014, 26(4): 89-92. |
| [4] |
滕婧, 梁敬钰, 陈莉. 鸡血藤的研究进展[J]. 海峡药学, 2015, 27(3): 1-6. DOI:10.3969/j.issn.1006-3765.2015.03.001 |
| [5] |
符影, 程悦, 陈建萍, 等. 鸡血藤化学成分及药理作用研究进展[J]. 中草药, 2011, 42(6): 1229-1234. |
| [6] |
林惠贞, 刘浩文, 韦玮, 等. 鸡血藤药材及其不同部位缩合鞣质的含量测定[J]. 中国实验方剂学杂志, 2013, 19(24): 70-74. |
| [7] |
陈红英, 严萍, 张敏, 等. 不同产地鸡血藤药材高效液相色谱指纹图谱及芒柄花素含量分析[J]. 广州中医药大学学报, 2015, 32(5): 923-928, 936. |
| [8] |
李小莹, 周龙颖珍, 赖丽嫦, 等. 鸡血藤干、鲜品黄酮部位的高效液相指纹图谱比较[J]. 中国实验方剂学杂志, 2015, 21(20): 72-75. |
| [9] |
杨冉冉, 姬蕾, 李二文, 等. 鸡血藤的HPLC指纹图谱及模式识别研究[J]. 中草药, 2017, 48(21): 4530-4536. DOI:10.7501/j.issn.0253-2670.2017.21.026 |
| [10] |
杨冉冉, 索亚然, 乔艺涵, 等. HPLC同时测定鸡血藤中芒柄花素和美迪紫檀素等6个黄酮类成分[J]. 药物分析杂志, 2017, 37(12): 2139-2144. |
| [11] |
杜憬生, 吴立群, 马鸿雁. 一测多评法测定鸡血藤中4种黄酮成分含量[J]. 中药材, 2017, 40(4): 881-883. |
| [12] |
张敏, 刘翠婷, 严萍, 等. 快速液相法同时测定鸡血藤原儿茶酸、儿茶素和表儿茶素的含量[J]. 广州中医药大学学报, 2014, 31(3): 439-442, 447. |
| [13] |
谭潇, 董宪喆, 郭代红, 等. 鸡血藤醇提物及其活性成分儿茶素抗辐射作用及机制研究[J]. 中国中药杂志, 2016, 41(9): 1718-1724. |
| [14] |
董攀, 罗泽欣, 王冬梅. 鸡血藤原花青素的提取工艺和体外抗氧化活性[J]. 中山大学学报(自然科学版), 2017, 56(1): 8-13. |
| [15] |
Zhang Yu, Guo Long, Duan Li, et al. Simultaneous Determination of 16 Phenolic Constituents in Spatholobus Caulis by High Performance Liquid Chromatography/Electrospray Ionization Triple Quadrupole Mass Spectrometry[J]. J. Pharm. Biomed. Anal, 2015, 102: 110-1118. DOI:10.1016/j.jpba.2014.09.006 |
| [16] |
香港中药材标准第五期[S]. 2015: 381.
|
 2019, Vol. 33
2019, Vol. 33