2. 中国食品药品检定研究院, 北京 100050
2. National Institutes for Food and Drug Control, Beijing 100050, China
通滞苏润江是一种维吾尔药制剂, 由番泻叶、秋水仙、诃子肉、盒果藤、巴旦仁、西红花、司卡摩尼亚脂七味药材粉碎制成。现有胶囊剂和片剂两种剂型, 全国共有生产企业7家, 批准文号8个。现行标准既有收载于《卫生部药品标准》维吾尔药分册1998年版, 又有原国家食品药品监督管理总局批准的试行标准或单行标准。
本次国家药品抽验工作共抽取55批次样品, 涉及6家生产企业, 7个批准文号。首先, 进行了标准检验; 然后, 基于标准检验, 以原料药材和制剂的质量问题为导向, 结合本品处方含贵细药、毒性药等特点, 在参考相关文献[1-11]的基础上, 围绕药品安全性、有效性、整体质量控制等方面开展了13项探索性研究和评价, 查找潜在质量隐患, 探索新的质控技术与方法。通过分析标准检验和探索性研究结果, 对该制剂的整体质量进行评价, 以期为该制剂的监督管理和质量标准提高提供参考, 同时, 希望相关企业对自身产品质量状况有更全面的认识和了解, 持续地改进和提高产品质量。
1 仪器与试药Waters 2695高效液相色谱仪(2998PDA检测器); Agilent1100高效液相色谱仪(MWD检测器); LC-2010AHT型高效液相色谱仪(UV-Vis检测器); Waters 2695高效液相色谱仪(2475荧光检测器); 光化学衍生器(北京华安麦科生物技术有限公司); 黄曲霉毒素(B1/B2/G1/G2)免疫亲和柱(北京华安麦科生物技术有限公司, 规格为3 mL); 岛津GC-MS气相色谱质谱联用仪(带ECD检测器); 岛津AA7000原子吸收分光光度仪; EHD-36plus型湿法消解仪; AFS-830型原子荧光光度仪(北京吉天仪器有限公司); SURRC脉冲光激发光(PPSL)辐照食品检测仪(英国苏格兰大学研究和反应堆中心研制); ChemPattern先进化学计量学系统解决方案软件[科迈恩(北京)科技有限公司]; Milli-Q超纯水处理系统; Agilent Zorbax SB C18色谱柱, Venusil MP C18色谱柱, Waters Sunfire C18色谱柱, Kromasil C18色谱柱, Kromasil Eternity-5-C18色谱柱, 上述色谱柱规格均为(250 mm×4.6 mm×5µm); Rtx-5MS (30 mm×0.25 mm×0.25µm)。
乙腈、甲醇、四氢呋喃(色谱纯, Fisher公司); 甲醇、氯化钠、乙醇、甲酸、磷酸(分析纯, 北京化学试剂厂), 吐温20购自Sigmaaldrich; 西红花苷-Ⅰ(批号111588-201303)、西红花苷-Ⅱ(批号111589-201304)、番泻苷B (批号110825-201301)、番泻苷A (批号110824- 201301)、没食子酸(批号110831-201204)、秋水仙碱(批号101176-201202)和黄曲霉毒素混合对照品(B1/B2/G1/G2)均购于中国食品药品检定研究院; 诃子酸(CAS号23094-71-5)对照品购自成都普瑞法科技开发有限公司。
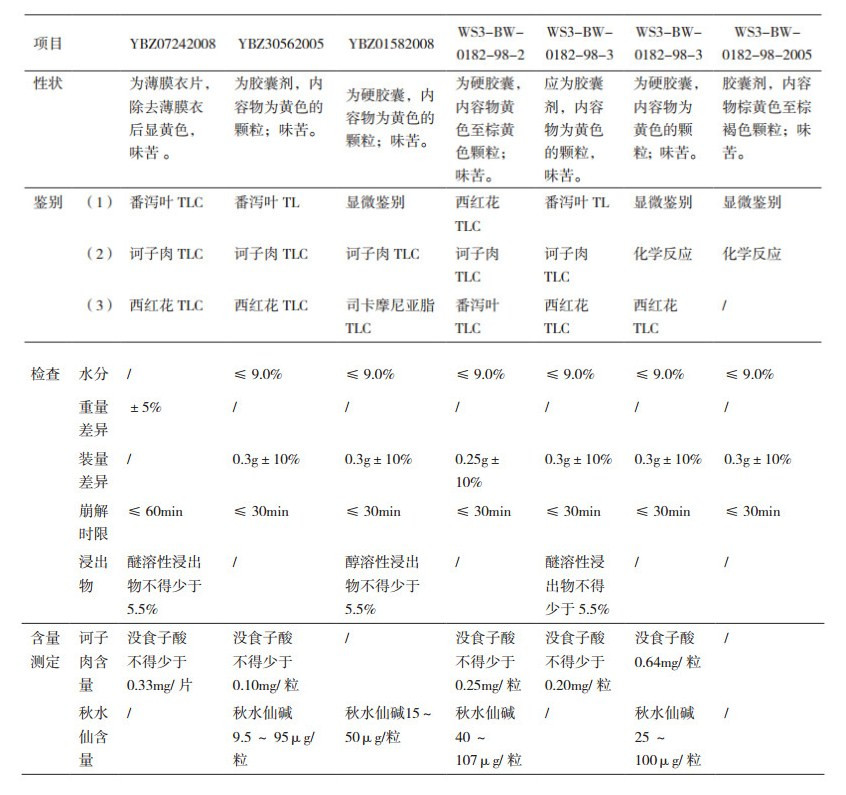
2 标准检验 2.1 检验标准通滞苏润江胶囊和通滞苏润江片的执行标准共8个, 此次检验涉及到7个, 执行标准各不相同, 详见表 1。
|
|
表 1 通滞苏润江制剂的质量标准 |
55批次样品按质量标准检验, 结果均符合规定, 合格率100%, 但各厂家样品的测定结果不尽一致。以诃子肉为例, 在各厂家处方中的量相同, 但没食子酸的含量测定限度和结果差异较大, 厂家A规定不得少于0.25 mg/粒, 平均含量为0.37 mg/粒; 厂家B规定应不得少于0.10 mg/粒, 平均含量为0.20 mg/粒; 厂家D规定应不得少于0.20 mg/粒, 平均含量为0.36 mg/粒; 厂家E规定不得少于0.64 mg/粒, 平均含量为7.04 mg/粒。建议同种成分的含量测定项的测定方法及限度统一。
2.3 标准评价对检验结果进行分析, 表明现行标准设置过于简单、不够全面; 存在着检验项目缺失的情况, 如各厂家均未对番泻叶和西红花药材设定含量测定项, 并非所有厂家均对秋水仙药材进行了控制。此外, 本品为生药原粉的制剂, 原料药材存在硫磺熏蒸、农药残留、黄曲霉污染、化工染料染色等安全隐患, 质量风险可能向制剂转移, 但各厂家均未对安全性进行控制。
3 探索性研究 3.1 安全性相关研究 3.1.1 色素检测制剂处方中含有的西红花药材, 存在非法染色的可能, 因此, 参照西红花药材中金胺O、新品红、柠檬黄、胭脂红的补充检验方法进行了检测。结果55批次样品均未检出相应的色素, 合格率为100.0%。
3.1.2 黄曲霉毒素检测制剂处方中含有的巴旦仁药材, 存在黄曲霉毒素污染的可能, 故采用HPLC-光化学衍生-荧光检测的方法进行了分析。目前, 国内尚无制剂中黄曲霉毒素的限量标准, 笔者采用文献[1]中的建议限量, 即黄曲霉毒素B1不得过5µg·kg-1, 总量不得过10µg·kg-1。结果49批次样品检出率为100%, 合格率为89.8%, 厂家A和厂家F均有不合格的批次, 存在一定的风险。
3.1.3 二氧化硫检测制剂为原粉入药, 若原料药经过硫磺熏蒸, 存在将毒性物质引入制剂的风险, 故采用《中国药典》(2010年版一部)附录Ⅸ U二氧化硫残留量中的滴定法进行了测定。参照《中国药典》(2010年版一部)第二增补本规定的中药材及饮片二氧化硫残留量不得超过150µg·kg-1为限量, 则55批次样品合格率为100%。
3.1.4 有机氯农药残留检测制剂为原粉入药, 不涉及提取等步骤, 那么成药中可能会引入原药材中含有的农药残留, 因此, 采用《中国药典》(2010年版一部)附录的农药残留量测定法(GC-ECD法)进行了有机氯农药的分析。结果均未检出相应的农药, 55批次样品合格率为100.0%。
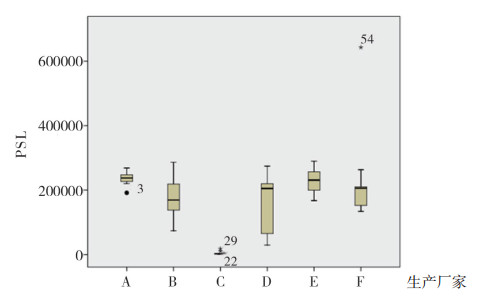
3.1.5 辐照情况考察辐照杀菌[2]在农业、工业、医药以及医疗器械等领域均有应用。本制剂为全粉入药, 存在辐照的可能, 因此, 采用光释光法进行了检测。以PSL值大于5000作为辐照的判定依据。结果55批次样品PSL值在1019~643074, 大部分批次PSL值远大于判定值, 可初步推测这些样品均经过不同程度的辐照灭菌处理, 辐照率为87.3%, 如图 1所示。个别厂家的辐照剂量明显大于其他企业, 其中厂家A的样品辐照率为100%。上述结果表明本制剂可能存在安全风险。
|
图 1 辐照结果箱式图 |
重金属是目前公认对人体有害的微量元素, 重金属含量超标造成的中药材的安全隐患日益受到重视, 故采用《中国药典》(2015年版四部)附录2321方法测定了铅、镉、砷、汞、铜等有害元素的含量。参照《中国药典》(2015年版一部)中药材的限量, 55批次样品合格率为100.0%。
3.1.7 松香酸检测乳香等树脂类药材存在非法添加松香的情况, 已造成了药害事件的发生。本制剂处方中的司卡摩尼亚脂亦为树脂类药材, 因此, 采用HPLC法检查是否添加了松香。结果55批样品均未检出松香酸, 合格率为100%。
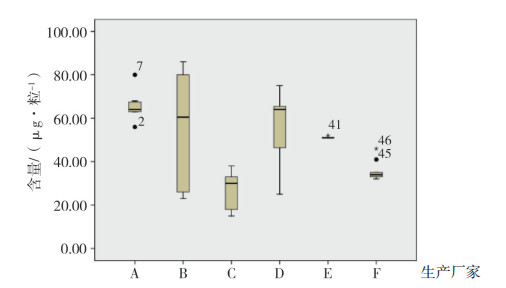
3.2 有效性相关研究 3.2.1 秋水仙中秋水仙碱的含量测定[3]此次被抽样的6个厂家中, 仅有A、B、E、F 4个厂家的标准设置了秋水仙碱含量测定项, 已设置含量测定项的4个标准提取方法各异, 规定限度差异也较大, 因此, 建立了统一的秋水仙碱的含量测定方法, 并设置了统一的限度。秋水仙收载于《卫生部药品标准》维吾尔药分册, 但该药材的质量标准中无秋水仙碱含量测定项, 因为无法参照药材标准折算本制剂中秋水仙碱的含量限度。笔者汇总了各厂家标准中秋水仙碱的含量限度, 最大差值为9.5~107µg/粒; 最小差值为40~50µg/粒。同时, 按拟定的含量测定方法测定了55批次样品中秋水仙碱的含量, 均值为50µg/粒, 上下浮动20%为40~60µg/粒; 上下浮动30%为35~65µg/粒; 上下浮动40%为30~70µg/粒。综合各企业标准对秋水仙碱的含量测定限度, 并参考实际检测数值均值, 暂定秋水仙碱的限度为40~95µg/粒(胶囊剂)、67~158µg/片(片剂)。55批样品测定结果在16~80µg/粒, 合格率为50.9%, 存在较大的安全风险。由箱式图 2可见, 6个厂家样品之间的差异较大, 而厂家B的样品批间差异很大, 可能都是秋水仙药材差异大所致。
|
图 2 秋水仙含量测定结果箱式图 |
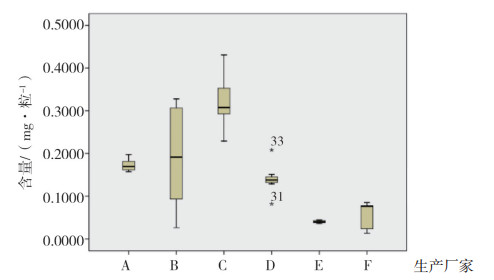
处方中西红花为贵细药材, 6个厂家的标准均未设置相应的含量测定项, 为保证制剂的质量, 增加了西红花的HPLC含量测定法。根据《中国药典》(2015年版一部)规定, 药材含西红花苷Ⅰ和西红花苷Ⅱ的总量不得少于10.0%。此方为全粉入药, 转移率按90%计, 暂定胶囊每粒含西红花以西红花苷Ⅰ和西红花苷Ⅱ的总量不得少于0.27 mg, 每片不得少于0.45 mg/片。55批样品测定结果在0.013~0.431mg/粒, 合格率为23.6%。由结果箱式图 3可见, 6个厂家之间的差异较大, 其中厂家B的样品批间差异很大, 分析为西红花药材批间差异大所致, 部分厂家还存在着少投料或者投劣药的可能。
|
图 3 西红花含量测定结果箱式图 |
此次被抽样的6个厂家的质量标准均未制定番泻叶的含量测定项, 为提高本制剂的质量控制水平, 建立了番泻叶的HPLC含量测定方法。根据《中国药典》(2015年版一部)规定, 药材含番泻苷A和B的总量不得低于1.1%, 转移率按90%计, 暂定胶囊剂的限度为不低于0.42 mg/粒; 片剂为不低于0.70 mg/片。结果表明, 55批次的样品的合格率为72.7%。由箱式图 4可见, 厂家A、B、D、E和F的样品含量均值均较接近, 同一厂家不同批次间的含量差异也不大, 仅厂家C的样品中未检出番泻皂苷A和B, 推测其投料的原药材或制剂工艺可能存在问题。

|
图 4 番泻叶含量测定结果箱式图 |
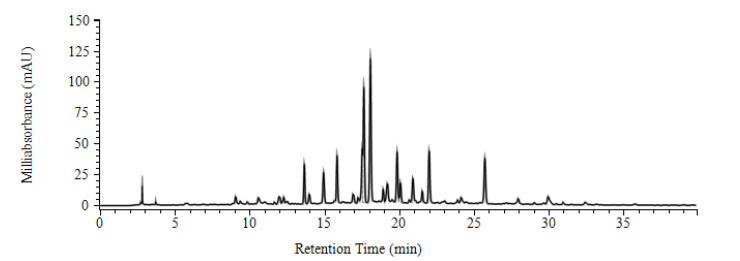
前文中建立的秋水仙、西红花和番泻叶三味药材的含量测定方法的前处理方法和色谱条件均不一致, 为提高分析效率, 探索新技术的可行性, 研究建立了可同时分析上述三种药材及诃子肉中7种成分的HPLC多指标含量测定法, 典型色谱图见图 5。
|
图 5 多指标含量测定350nm的HPLC色谱图(厂家A样品) |
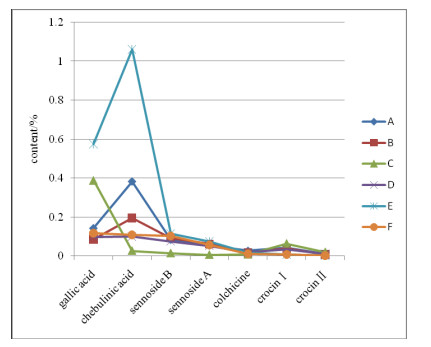
为了更清晰地显示各厂家样品的含量特征, 绘制了对应的平均样品折线图, 见图 6。厂家A的样品综合质量最佳, 这与其质量标准较为完备有直接关系, 但也存在西红花苷类含量不足的问题; 厂家B的样品轮廓与厂家A较接近, 两者主要差异在于诃子酸含量的高低; 厂家C的样品质量不佳, 表现在没食子酸含量偏高, 但诃子酸含量极低, 同时番泻苷A、B和秋水仙碱的含量也极低, 这与其质量标准最为简单有关; 厂家D的样品轮廓与厂家B较为接近, 差异在于诃子酸的含量更低; 厂家E的样品轮廓最为特别, 即没食子酸和诃子酸含量奇高, 但其余成分含量都较低, 特别是西红花苷类成分含量很低; 厂家F的样品轮廓与厂家D的样品也较为相似, 主要差别在于西红花苷类成分特别低。
|
图 6 各厂家样品含量结果图(平均值) |
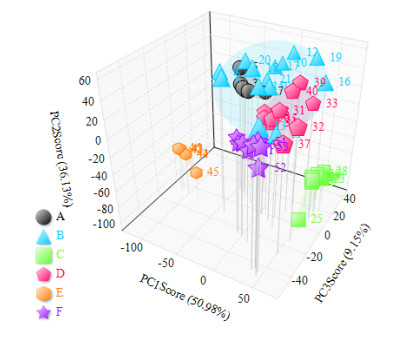
采用与多指标含量测定相同的前处理及色谱条件, 进一步拓展建立了可以分析5种药材(增加了司卡摩尼亚脂)中18个成分的指纹图谱分析法, 并采用相似度分析、聚类分析和主成分分析多种化学计量学方法进行数据分析。3种方法的分析结果较一致, 本文简述PCA结果(见图 7):不同厂家的样品分布在不同的主成分空间位置, 相互之间可以较好地区分; 其中厂家A和厂家B的样品空间位置较接近, 表明整体成分的种类和量较相近; 厂家A、厂家C和厂家F的样品更为集中, 表明批间差异小, 其余3家的样品较为分散, 表明不同批次存在一定的差异。
|
图 7 各厂家样品主成分分析结果图 |
多指标含量测定和化学计量学分析可以极大地提高分析效率, 考察制剂的一致性以及从整体上分析样品的质量和异同, 具有高效和全面的优势。
4 问题与建议 4.1 主要问题根据对药品安全性、真实性、有效性、均一性等影响程度的不同, 我们将标准检验及探索性研究中发现的问题归纳如下。主要问题:(1)标准繁多, 设置不全面, 项目不一致; (2)检出黄曲霉毒素; (3)西红花和番泻叶成分含量低; (4)毒性药秋水仙含量差异较大。次要问题:(1)存在辐照问题; (2)诃子肉药材或存在一定差异; (3)各企业间样品整体的一致性不佳; (4)同一企业不同批次样品存在差异。
4.2 相关建议1) 完善质量标准, 增加番泻叶、西红花含量测定项; 统一诃子肉和秋水仙的含量测定项; 增加黄曲霉毒素检查项; 加强整体质量控制法研究。
2) 加强生产监管, 企业加强对原料药材及制剂质量的自检。
3) 开展专项研究, 开展辐照对本制剂安全性和有效性的影响研究, 为允许辐照或禁止辐照提供依据。
| [1] |
刘丽娜, 金红宇, 孙磊, 等. 中药材及部分制剂中黄曲霉毒素残留筛查报告及初步风险评估[J]. 中国药学杂志, 2015, 50(17): 1541-1546. |
| [2] |
陈佳, 金红宇, 田金改, 等. ~(60)Co-γ射线灭菌后中药材中的辐照残留考察[J]. 药物分析杂志, 2012(9): 1694-1696. |
| [3] |
刘桂花, 何承辉, 邢建国, 等. HPLC法同时测定复方苏润江滴丸中秋水仙碱、芦荟苷及芦荟大黄素的含量[J]. 药物分析杂志, 2013(3): 409-413. |
| [4] |
何常明, 谢晓梅, 何美莲, 等. 西红花中西红花苷-1和西红花苷-2含量测定方法的建立[J]. 药物分析杂志, 2006(9): 1270-1273. |
| [5] |
Koulakiotis N S, Gikas E, Iatrou G, et al. Quantitation of Crocins and Picrocrocin in Saffron by HPLC:Application to Quality Control and Phytochemical Differentiation from Other Crocus Taxa[J]. Planta Medica, 2015, 81: 606-612. DOI:10.1055/s-00000058 |
| [6] |
Lech K, Witowska-Jarosz J, Jarosz M. Saffron Yellow:Characterization of Carotenoids by High Performance Liquid Chromatography with Electrospray Mass Spectrometric Detection[J]. Journal of Mass Spectrometry, 2009, 44(12): 1661-1667. |
| [7] |
邵怡, 张水寒, 蔡光先, 等. 番泻叶超微粉体HPLC指纹图谱的研究[J]. 中成药, 2012, 34(3): 397-400. DOI:10.3969/j.issn.1001-1528.2012.03.003 |
| [8] |
尹春梅, 韩世柳, 田成旺, 等. 诃子HPLC指纹图谱及模式识别研究[J]. 中草药, 2010, 41(9): 1467-1469. |
| [9] |
颜玉贞, 卢平华, 谢培山. 西青果与诃子的HPLC指纹图谱鉴别研究[J]. 中药新药与临床药理, 2001, 12(3): 173-178. |
| [10] |
逄瑜, 孙磊, 金红宇, 等. 指纹图谱结合化学计量学分析用于多种大黄的鉴别及质量评价[J]. 中国药学杂志, 2014(4): 287-293. |
| [11] |
Zhang C, Sun L, Run-tao Tian, et al. Combination of Quantitative Analysis and Chemometric Analysis for the Quality Evaluation of Three Different Frankincenses by Ultra High Performance Liquid Chromatography and Quadrupole Time of Flight Mass Spectrometry[J]. Journal of Separation Science, 2015, 38(19): 3324-3330. DOI:10.1002/jssc.201500326 |
 2019, Vol. 33
2019, Vol. 33