中药依靠其独特的疗效、较低的毒副作用在临床上得到广泛应用。但近年来, 部分中药材不法商贩使用合成染料将药材染色后出售, 谋取暴利[1-2]。这些合成染料大都具有一定的毒性, 在食品领域被禁止使用或严格控制用量[3-4], 染色行为对中药的用药安全构成了极大威胁。这些染色过的中药材也可能作为原料用于中成药的生产中, 污染中成药[5-6]。此外, 合成色素也可能用于制剂生产过程中, 以改善制剂外观。如使用了没有药品辅料标准的色素, 或该生产工艺未向药品监督管理部门申报, 上述行为就违反了药品生产GMP规定。因此, 中成药合成色素的测定方法也越来越受到关注。国家药品监督管理部门对此高度重视, 审核并通过了多个中药中合成染料的补充检验方法[7], 有力地打击了中药中使用合成染料的违法行为。
已报道的中药中合成染料检测方法主要有薄层色谱法[2]、液相色谱法[1-2, 8]、液相色谱与质谱联用[1-2, 5-6, 9-10]、薄层色谱与质谱联用[11]以及离子迁移谱[12]等, 其中液相色谱与质谱联用是最常用的检测方法, 质谱谱库也已广泛应用于染色物质筛查中[13-15]。可能被染色的药材主要有西红花、红花、乌梅、蒲黄、栀子、延胡索、石斛、黄连、黄芩、黄柏、红花、丹参、朱砂、血竭等, 可能含有染色药材的中成药主要有少腹逐瘀丸、冠脉宁片等。
女金丸为妇科常用药物, 由当归、白芍、川芎等23味药制成, 功能益气养血、理气活血、止痛, 临床用于气血两虚、气滞血瘀所致的月经不调等症的治疗[16]。笔者实验室得到8批疑似含有苋菜红(amaranth)、亮蓝(brilliant blue)、日落黄(sunset yellow)等合成染料的女金丸样品, 对其中的染色情况进行了分析测定。
1 仪器与试药Agilent 1260-6410B液相色谱-质谱联用系统, 配有二极管阵列检测器及三重四级杆质谱检测器, 安捷伦Mass Hunter化学工作站; Mettler XS105DU电子天平; KQ-300DA型数控超声波清洗仪(昆山市超声仪器有限公司; 超声功率300 W; 频率40 kHz); 苋菜红(批号20121215)、日落黄(批号20130618)由天津市光复精细化工研究所提供; 亮蓝由中国计量科学研究院提供[批号: GBW (E)100005a-08002]。乙腈为色谱纯, 醋酸铵、乙醇、冰醋酸为分析纯, 试验用水为Milli-Q系统制备。
样品共计8批次, 均标示为同一生产厂家生产。阴性样品为市售另一厂家女金丸样品。
2 方法与结果 2.1 制剂染色情况观察将丸剂切开, 观察丸剂外层和内层的色差, 结果见图 1。从图 1可以看到, 该丸剂表层较内层颜色明显偏深, 有可能存在外层色素染色情况。用棉花蘸取70%乙醇, 轻轻擦拭丸剂外侧, 棉花被染为蓝黑色, 见图 2。提示丸剂表层含有色素。

|
图 1 丸剂外层和内层的颜色差异 |

|
图 2 棉花擦拭丸剂外侧结果 |
为确认制剂中是否含有合成色素以及所含色素种类, 参考本实验室已建立的方法[15], 使用HPLC-DAD-MS对样品进行测定。
2.2.1 对照品溶液制备取苋菜红、亮蓝、日落黄对照品适量, 用甲醇溶解, 制成每1 mL中约含0.1 mg的混合对照品溶液, 用0.45 µm微孔滤膜滤过, 取续滤液, 即得。
2.2.2 供试品溶液制备取丸剂1包(水蜜丸, 5 g), 加70%乙醇溶液15 mL, 振摇5 min, 分取乙醇液蒸干, 加1.5 mL甲醇溶解, 再用0.45 µm微孔滤膜滤过, 取续滤液, 作为供试品溶液。
2.2.3 阴性样品溶液制备取阴性样品丸剂5 g (水蜜丸), 同"2.2.2节下方法制备阴性样品溶液。
2.3 色谱条件[15]采用Phenomenon Luna C18(250 mm×4.6 mm, 5 µm)色谱柱, 以乙腈为流动相A, 0.05 mol·L-1醋酸铵(冰醋酸调pH 4.5)为流动相B, 线性梯度洗脱, 在30 min内, 流动相A的比例由2%升至70%;流速:1 mL·min-1;柱温:25℃; DAD检测器检测波长范围:400~700 nm, 各化合物检测波长见表 1最大吸收波长; 进样量10 µL。
|
|
表 1 各化合物色谱及质谱测定参数 |
流动相分流比约4:1;采用电喷雾离子源(electronic spray ionization, ESI), 二级质谱全扫描模式(product ion scan); 干燥气温度350℃; 干燥气流速10 L·min-1;雾化气压力35 psi; 源电压4 kV; 各化合物离子源、母离子、裂解电压及碰撞能量等质谱参数见表 1。
2.5 样品测定取对照品及供试品溶液各10 µL, 分别注入高效液相色谱仪, 记录色谱、可见光光谱及质谱图, 结果见图 3~5。从图中可以看到, 在样品中可检测到与苋菜红、日落黄和亮蓝保留时间一致的色谱峰, 并且上述色谱峰的二级质谱谱图与对照品基本一致。8个批次样品均可检出苋菜红、日落黄和亮蓝。

|
1.苋菜红; 2.日落黄; 3.亮蓝。 图 3 对照品(A)、样品(B)和阴性样品(C) HPLC-DAD色谱图(400~700 nm) |

|
图 4 苋菜红、日落黄及亮蓝对照品(A)和样品(B)可见光光谱图(400~700 nm) |
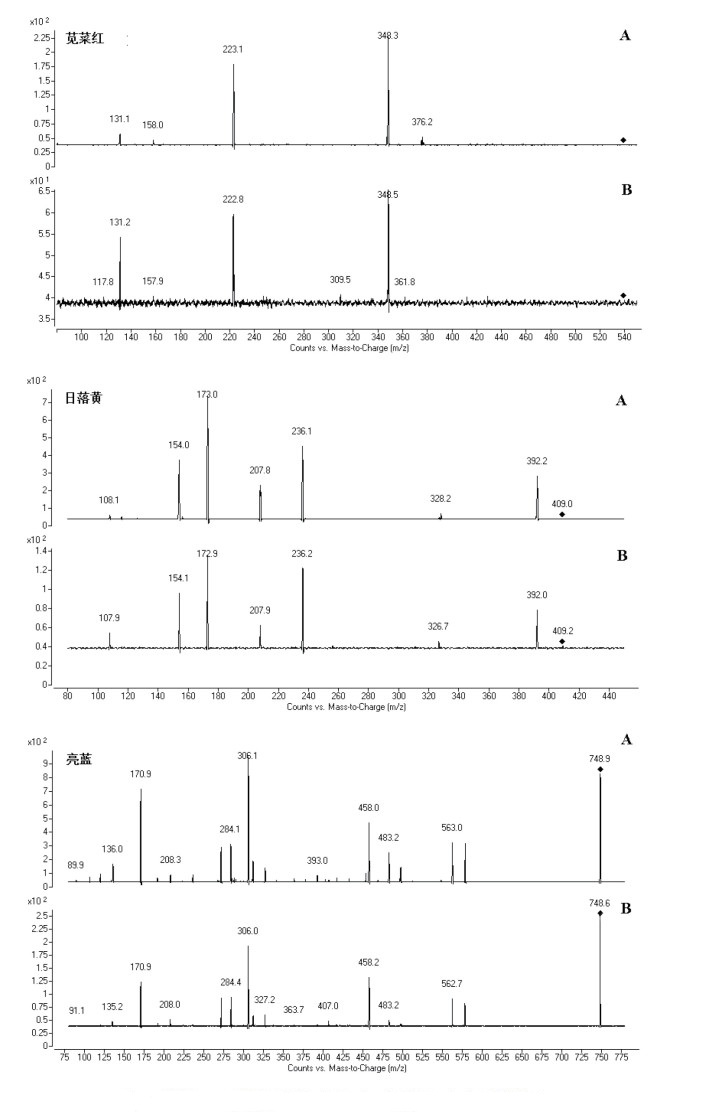
|
图 5 苋菜红、日落黄及亮蓝对照品(A)和样品(B)质谱谱图 |
为进一步确认合成色素的存在部位, 在刮取丸剂表层后, 采用HPLC-DAD分别对丸剂表层与内层样品进行测定。
3.1 对照品溶液制备制备方法同"2.2"节。
3.2 丸剂外层和内层供试品溶液制备取8批次样品各1丸, 刮取表层, 置2 mL塑料离心管中备用。刮除表层丸剂样品用研钵研细后置于另一2 mL塑料离心管中。在各离心管中分别加入1.5 mL 70%乙醇溶液, 超声提取30 min, 静置使沉淀, 分取乙醇液用0.45 µm微孔滤膜滤过, 取续滤液, 作为丸剂外层和内层供试品溶液。
3.3 色谱条件色谱条件同"2.3 "及" 2.4"节。
3.4 样品测定取对照品及供试品溶液各10 µL, 分别注入高效液相色谱仪, 记录色谱图, 结果见图 6。从图 6可以看到, 丸剂外层供试品溶液中可明显检出合成色素, 但内层供试品溶液中未检出或仅可检出微量的合成色素。8批次样品均呈现相似结果。由此可以判断合成色素主要存在于丸剂外层, 推断可能在丸剂成型后加入, 以改善成品外观性状。

|
A.对照品;B.丸剂内层样品(批号160102);C.丸剂外层样品(批号160102);1.苋菜红;2.日落黄;3.亮蓝。 图 6 色素存在部位考察HPLC-DAD色谱图(400~700nm) |
红黄蓝是构成不同颜色的三原色, 不同浓度的三原色可调配出丰富的颜色。苋菜红、亮蓝、日落黄就是较常用的红色、蓝色和黄色食用色素。食用色素大都为水溶性色素, 色牢度较苏丹红等化工染料差, 受潮时容易脱落, 在中药非法染色中较少使用。在国家药品监督管理局批准的乌梅(炙乌梅)药品补充检验方法和检验项目中, 针对苋菜红、亮蓝、日落黄3种色素进行检查, 方法正文中描述供试品溶液为墨绿色[17]。本次测定中, 丸剂外层供试品溶液呈蓝黑色, 也是上述3种色素调配的结果。
苋菜红、亮蓝、日落黄等食用色素极性较大, 质谱较难裂解, 只有在浓度较大时方可得到其二级质谱谱图。同时, 色素类成分的共轭体系较大, 在可见区均有较大吸收, 使用液相紫外可见波长检测器测定的灵敏度较高。由于已使用质谱确认在制剂中含有合成色素, 在进行色素存在部位考察时, 我们仅使用了DAD检测器进行检测。
在刮取丸剂表层时, 有可能存在被染色的部分刮取不完全的情况。此外, 在丸剂外层染色时, 部分色素也可能渗入丸剂内层。丸剂内层供试品溶液可检出少量色素, 可能由上述原因导致。
目前, 文献报道的中药染色, 其研究对象大都是染色中药材或使用染色中药材投料生产的中成药[1-2, 5-6, 9, 15]。本研究发现某厂生产的女金丸中合成染料大都集中于丸剂外层, 分析原因可能是生产厂家为了保持各批次产品外观颜色的一致, 使用染料对丸剂进行染色, 是生产过程中的染色。虽然在制剂中检测到的合成色素属于可食用色素, 毒性较小, 但仍具有一定毒性[18-20], 其在中成药中的使用也应加以控制。此外, 该工艺如未上报药品监管部门批准, 就属于私自更改生产工艺的违法行为, 应严厉查处。在今后的中成药染色物质检测研究中也应考虑对制剂染色部位进行分析, 以推断其染色原因, 便于监管。
| [1] |
苏晶, 程显隆, 张聿梅, 等. 伪品血竭中染色剂苏丹红Ⅳ的检测[J]. 中国药事, 2008, 22(4): 318-320. |
| [2] |
闵春艳, 付凌燕, 汪祺, 等. 红花药材掺伪染色检测方法的实验研究[J]. 中国药事, 2011, 5(8): 772-775. |
| [3] |
卢士英, 邹明强. 食品中常见的非食用色素的危害与检测[J]. 中国仪器仪表, 2009(8): 45-50. DOI:10.3969/j.issn.1005-2852.2009.08.007 |
| [4] |
中华人民共和国国家卫生和计划生育委员会.食品中可能违法添加的非食用物质和易滥用的食品添加剂名单(第1-5批汇总)[EB/OL].(2011-04-22)[2018-09-06]. http://www.nhfpc.gov.cn/zwgkzt/wsbysj/201104/51441.shtml.
|
| [5] |
何凤艳, 何轶, 余新启, 等. 牛黄消炎片中孔雀石绿的检测方法研究[J]. 药物分析杂志, 2014, 34(4): 698-701. |
| [6] |
何轶, 丁宁, 王瑞忠, 等. 冠脉宁片中化工染料检查及血竭素高氯酸盐含量测定研究[J]. 中国药学杂志, 2015, 50(2): 120-124. |
| [7] |
黄宝斌, 许明哲, 杨青云, 等. 中成药和中药材添加化学物质补充检验方法分析[J]. 药物分析杂志, 2014, 34(9): 1701-1708. |
| [8] |
肖凌, 侯俊杰, 徐箐, 等. 红花中一种新掺伪染料的确认及6种染色成分检测方法研究[J]. 药物分析杂志, 2014, 34(7): 1231-1236. |
| [9] |
连云岚, 杜娟, 乔玉峰. HPLC-MS法检测少腹逐瘀丸及原料药材中非法添加的7种黄色素[J]. 中草药, 2016, 47(18): 3219-3223. DOI:10.7501/j.issn.0253-2670.2016.18.014 |
| [10] |
胡青, 林媛, 张甦, 等. 超高效液相色谱-三重串联四级杆质谱法测定乌梅中19种深色染色色素[J]. 食品安全质量检测学报, 2016, 7(7): 2663-2670. |
| [11] |
He F, He Y, Zheng X, et al. Screening of Chemical Dyes in Traditional Chinese Medicine by HPTLC-MS[J]. Journal of AOAC International, 2018, 101(3): 686-694. DOI:10.5740/jaoacint.17-0298 |
| [12] |
焦建东, 牟卫伟, 权勤波, 等. 中药染色色素金胺O、日落黄和苋菜红的离子迁移谱技术快检方法研究[J]. 中国药学杂志, 2016, 51(6): 483-487. |
| [13] |
胡青, 孙健, 于泓, 等. 快速液相-四级杆串联高分辨飞行时间质谱定性测定中药中50种染色色素[J]. 中国药学杂志, 2016, 51(15): 1316-1323. |
| [14] |
苟琰, 耿昭, 张燕飞, 等. 液质联用法快速筛查中药材及饮片中常见染色掺假物质的方法研究及数据库建立[J]. 药物分析杂志, 2017, 37(3): 101-110. |
| [15] |
何轶, 雷银瓶, 鲁静, 等. HPLC-DAD-MS/MS法结合谱库筛查5种中药中21种合成染料[J]. 中成药, 2016, 38(12): 2631-2635. |
| [16] |
中华人民共和国药典: 一部[S]. 2015: 521-522.
|
| [17] |
乌梅(炙乌梅)药品补充检验方法和检验项目: 2009001[S]. 2009.
|
| [18] |
郑立新, 邹志飞, 吴赤蓬. 苋菜红和日落黄对蚕豆根尖细胞微核率的影响[J]. 职业与健康, 2009, 25(12): 1240-1242. |
| [19] |
陈玉银, 杜鑫, 靳远祥. 食用色素对家蚕毒性的试验[J]. 蚕桑通报, 2005, 36(3): 27-30. DOI:10.3969/j.issn.0258-4069.2005.03.008 |
| [20] |
栾秀坤, 吴桂珍, 李淑珍, 等. 药用胶囊和片剂中合成色素含量的调查[J]. 中国药学杂志, 1990, 25(1): 48-50. |
 2019, Vol. 33
2019, Vol. 33 

