2. 中山大学药学院, 广州 510006
2. Pharmaceutical College of Zhongshan University, Guangzhou 510006, China
肌酸激酶(creatine kinase,CK)是一个与细胞内能量转运、肌肉收缩以及三磷酸腺苷(adenosine-triphosphate,ATP)再生直接关联的激酶。体内有四种同功酶形式:肌肉型(MM)、脑型(BB)、杂化型(MB)和线粒体型(MiMi)。MM型主要存在于各种肌肉细胞中,BB型主要存在于脑细胞中,MB型主要存在于心肌细胞中,MiMi型主要存在于心肌和骨骼肌线粒体中。在临床疾病诊断中,血清CK浓度检测常用于肌肉萎缩和心肌梗塞等疾病的诊断[1-2]。乳酸脱氢酶(lactic dehydrogenase,LDH)是一种糖酵解酶,存在于机体所有组织细胞的胞质内,其中以肾脏含量较高。LDH常联合CK-MB、肌红蛋白以及肌钙蛋白等检测用于心肌梗死的诊断[3]。血清肌酐(serum creatinine,CRE)和血尿素(blood urea,UREA)水平是肾脏毒性的常规检验指标,常常联合肾毒性早期标志物胱抑素C的检测对肾脏损害的程度进行评价[4]。目前,这4项指标都在药物安全性评价研究中得以广泛应用,来检测药物在实验动物体内的毒性作用。实验室对这些指标的检测能力直接影响药物的毒性评价结果,从而对能否进一步研发这些药物产生重要影响。为了评价各检测实验室检测这4项指标的准确性和可比性,促进检验能力提高,故开展了本次能力验证研究。
能力验证(proficiency testing,PT)是利用实验室间比对,按照预先制定的准则评价参加实验室的检测能力[5]。能力验证组织者必须是经过CNAS认可的合格的能力验证提供者,并按照能力验证的相关指南开展能力验证研究[6-7]。本研究由中国食品药品检定研究院组织,由安全评价研究所负责实施。本文总结了本次能力验证研究的相关内容,并对不满意结果进行了分析,为实验室采取纠正措施,促进质量改善以及监管部门评价实验室检测能力提供参考依据。
1 材料与方法 1.1 材料能力验证样品为市售的某品牌高、低2个浓度的血清冻干粉,批号分别为875UE和1144UN,有效期至2020年7月。
1.2 仪器与试剂HITACHI 7180型全自动生化分析仪(日本日立公司);HB-RO/60制水机(杭州惠邦净水设备有限公司);IGS60通用型培养箱(美国Thermo公司);P1000 Gilson移液枪(美国吉尔森公司);CK试剂和校准品、LDH试剂和校准品、UREA试剂和校准品以及CRE试剂和校准品,均购自日本和光纯药工业株式会社。
1.3 试验方法 1.3.1 样品制备及发放对高、低2个浓度的血清冻干粉进行均匀性和稳定性检验,结果符合要求后,再分装成5个样品瓶,即1号(低)、2号(高)、3号(低)、4号(高)和5号(高),4 ℃冷藏保存。运输时将样品瓶放入塑料泡沫盒中,内置冰袋冷藏运输。使用时,每瓶加入5 mL去离子水,室温放置30 min,混匀、配制成上机样品。
1.3.2 均匀性和稳定性检验依据CNAS-GL03《能力验证样品均匀性和稳定性评价指南》,对高、低浓度能力验证样品的均匀性和稳定性进行检验,检验结果符合要求后,再进行标记[8]。采用单因素方差分析法(F检验)对样品进行均匀性检验。稳定性检验是以均匀性检验测定结果作为第1次稳定性数据,分别对室温条件保存8 d的样品、模拟运输条件保存7 d的样品以及在温度37 ℃加速试验条件下保存16 h的样品进行检测,采用t检验法判定样品的稳定性。
1.3.3 数据统计方法和能力评价方法随机抽样、均匀性和稳定性数据分析以及能力验证结果均采用SPSS19.0软件进行分析。通过单样本Kolmogorov-Smirnov检验进行能力验证结果数据的正态性检验,设置显著性水平P<0.05。
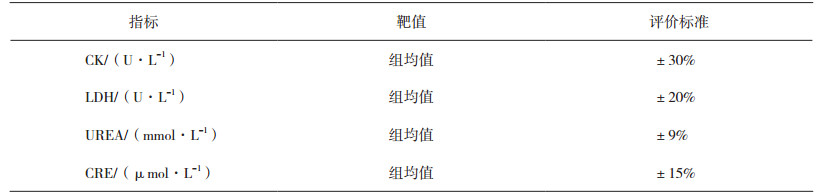
按照CNAS-GL02《能力验证结果的统计处理和能力评价指南》的评价原则以及美国临床实验室改进法案(CLIA’88)中生化指标的质量分析要求,制定本研究的评价标准,如表 1所示。依据美国病理学家学会(College of American Pathologists,CAP)组织的生化指标能力验证的评价要求,每个指标分配5个样品,一个样品通过记20分,得分大于或等于80分判定为该指标评价结果满意[9-10]。
|
|
表 1 生化指标的评价标准 |
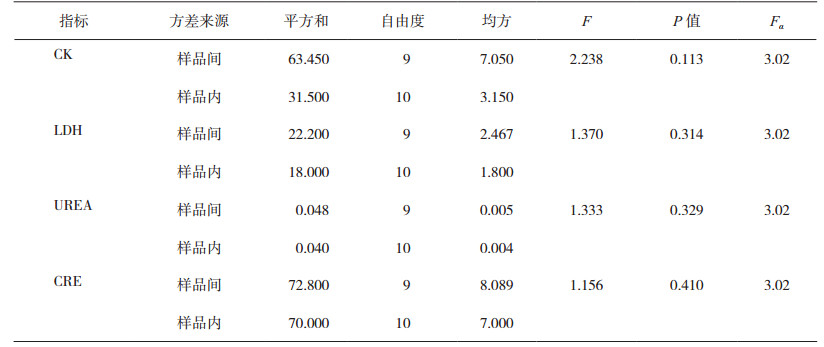
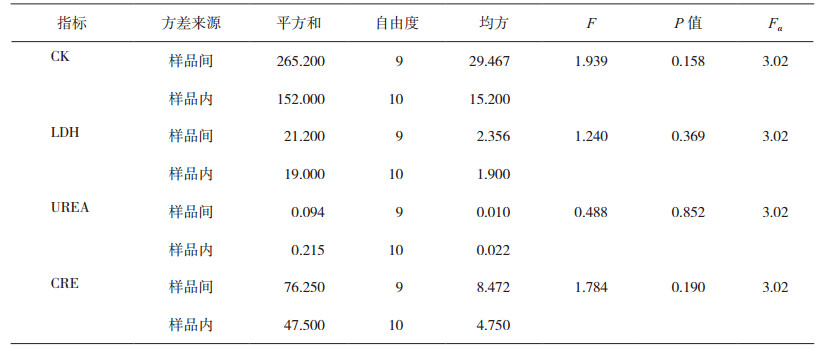
按照随机化原则,随机抽取高、低浓度样品各10瓶,混匀后每瓶再分装成2份,随机测定20次,对结果进行单因素方差分析,当F值<Fα(v1, v2)时,判定样品均匀分布[8]。研究中高、低浓度样品的各指标检验F值<Fα(9,10),样品是均匀的分布,能满足本次能力验证的要求,均匀性检验结果如表 2和表 3所示。
|
|
表 2 低浓度样品的均匀性检验结果 |
|
|
表 3 高浓度样品的均匀性检验结果 |
随机抽取高、低浓度样品各6瓶,将样品在温度37 ℃培养箱中放置16 h,进行加速稳定性研究。随机抽取高、低浓度样品各6瓶,按照实际运输时的要求进行包装后,放置在室外环境中7 d,进行运输条件下的稳定性研究。随机抽取高、低浓度样品各6瓶,放置在室温环境中8 d,进行室温条件下的稳定性研究。当t检验P>0.05时,判断样品稳定。研究结果显示,3种条件下高、低浓度样品的t检验P值都大于0.05,样品的稳定性符合能力验证的要求,稳定性检验结果如表 4所示。
|
|
表 4 样品稳定性试验结果(p值) |
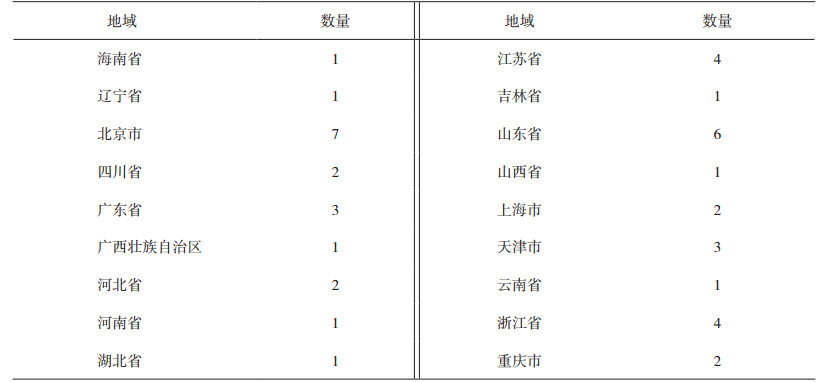
本研究共有43家实验室参加,43家实验室分布于18个省、自治区或直辖市,分布情况如表 5所示。并向这43家实验室发送了能力验证样品,回报CK、LDH、UREA和CRE结果的分别有40、32、41和43家。
|
|
表 5 参加实验室的地域分布情况 |
各参加实验室检测CK、LDH和UREA均分别采用了相同的检测方法,CK和LDH均采用速率法,UREA采用尿素酶法。CRE的检测方法有酶法和苦味酸法两种,分组进行统计分析和评价。37家实验室的生化分析仪器为国外品牌,6家为国产品牌。
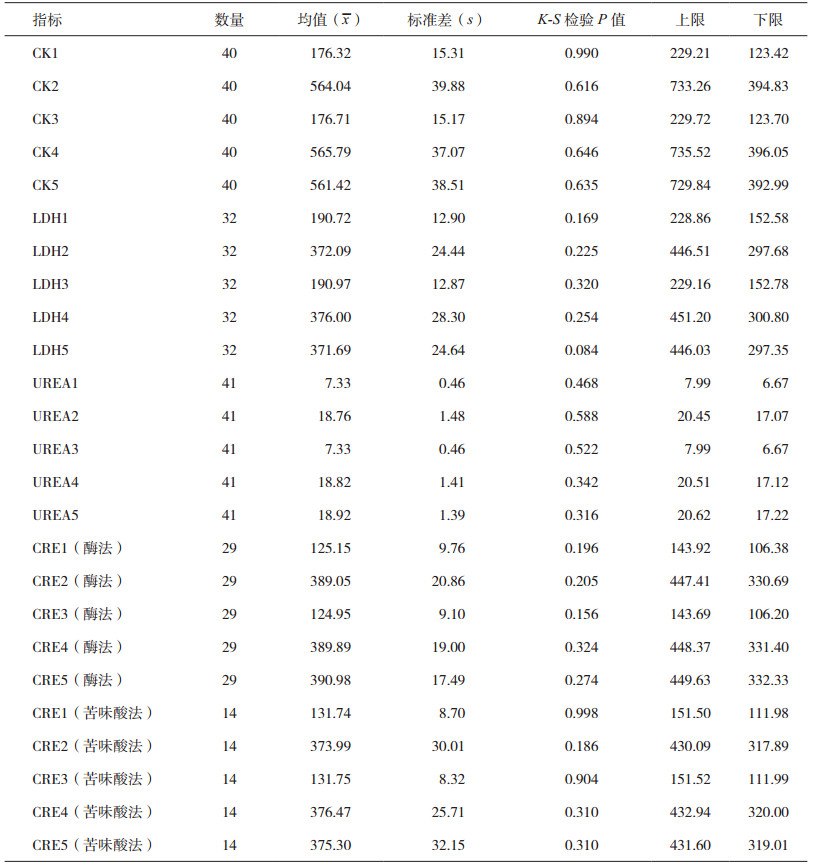
2.2.2 数据正态性检验及统计量结果对能力验证结果数据进行单样本KolmogorovSmirnov检验,P>0.05时,数据成正态性分布,P值小于或等于0.05时,数据成非正态性分布。结果显示,所有指标的Kolmogorov-Smirnov检验P值均大于0.05,数据成正态性分布。5个样品的能力验证结果的统计量如表 6所示。
|
|
表 6 能力验证结果的统计量 |
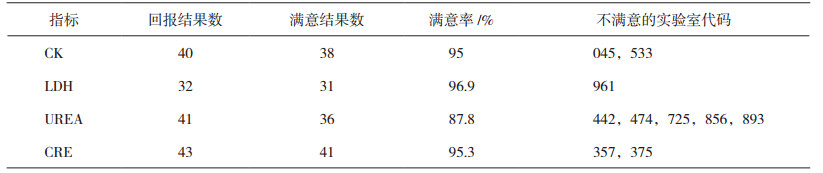
4个指标均出现不满意的结果,评价结果如表 7所示。
|
|
表 7 能力验证评价结果 |
在本研究制定评价标准时,参照了美国临床实验室改进修正法案(CLIA’88)、美国病理学家学会以及中国卫生行业标准《临床生物化学检验常规项目分析质量指标》(WS/T 403-2012)对这4项指标的质量要求,这保证了评价标准的科学性、权威性和适用性[11]。
CRE有酶法和苦味酸法两种测定方法,当CRE浓度处于较低或中等水平时,由于干扰物的影响,苦味酸法测定的结果偏高。而当CRE浓度较高时,由于受到线性检测限的影响,苦味酸法测定的结果偏低[12]。本研究中CRE浓度范围覆盖了高低水平,为了更客观真实地评价实验室的检测水平,避免因方法学不同所导致的误判,因此,将两种检测方法分为两组分别统计分析和评价。各实验室检测CK、LDH和UREA的方法都相同,因此,未进一步分组。本研究中实验室数量为43家,但所用仪器品牌或型号却多达25种,因此,也没有按照仪器品牌或仪器型号进行分组评价。
研究中的4项指标,只有CRE是所有实验室均开展的项目,其余项目均没有全部开展。所有指标均出现不满意结果,多种因素可以导致结果不满意,比如仪器未校准、检测参数设定错误、试剂浓度变化、人员操作以及机械方面的因素等。
实验室应查找不满意结果发生的具体原因,并采取纠正措施。实验室还可以申请测量审核进行再次评价,直至评价结果满意。否则,实验室的检测结果不准确、不具有可比性,也无法通过监管部门的实验室认证或审查。
| [1] |
朱文秀, 杨桂英. 血清肌酸激酶同工酶活性大于肌酸激酶的病例分析[J]. 国际检验医学杂志, 2017, 38(1): 104-105. DOI:10.3969/j.issn.1673-4130.2017.01.040 |
| [2] |
任永霞. 急性脑血管病患者心肌酶的变化及意义[J]. 中国医药导报, 2017, 14(28): 129-132. |
| [3] |
段秀群, 龚国富. 心肌梗死三项联合检测在急性心肌梗死诊断中的价值[J]. 临床和实验医学杂志, 2007, 6(7): 96. DOI:10.3969/j.issn.1671-4695.2007.07.062 |
| [4] |
袁俊蓉. 胱抑素C、肌酐和尿素氮在肾脏损害中的诊断价值[J]. 中外医学研究, 2017, 15(18): 47-48. |
| [5] |
GB/T 28043-2011/ISO 13528利用实验室间比对进行能力验证的统计方法[S]. 2011.
|
| [6] |
GB/T 27043-2012/ISO/IEC 17043: 2010合格评定-能力验证的通用要求[S]. 2012.
|
| [7] |
CNAS-CL03能力验证提供者认可准则[S]. 2012.
|
| [8] |
CNAS-GL03能力验证样品均匀性和稳定性评价指南[S]. 2012.
|
| [9] |
CNAS-GL02能力验证结果的统计处理和能力评价指南[S]. 2011.
|
| [10] |
刘远兴, 吴新伟, 李建杰, 等. 质量控制工具在临床生化项目过程能力验证中的应用[J]. 嘉应学院学报, 2013, 31(5): 73-79. DOI:10.3969/j.issn.1006-642X.2013.05.015 |
| [11] |
WS/T 403-2012临床生物化学检验常规项目分析质量指标[S]. 2012.
|
| [12] |
程开书, 孙建民, 方兰. 血清肌酐两种测定方法偏倚的比较[J]. 检验医学与临床, 2013, 10(16): 2092-2094. DOI:10.3969/j.issn.1672-9455.2013.16.014 |
 2019, Vol. 33
2019, Vol. 33