酶类药物是生化药物的重要组成部分,而蛇毒类血凝酶在酶类药物中的地位日益受到普遍的关注。随着蛋白质纯化分离技术的提高和生物化学、药理学的深入研究,确定了蛇毒类血凝酶在临床上止血应用的巨大价值,其中以瑞士Solco Basle Ltd的立止血(Reptilase)为主要代表[1]。经过几十年的研究和临床应用,已证明这一蛇毒血凝酶具有卓越的止血功效,广泛用于各种出血性疾病[2-5]。我国生产的蛇毒类血凝酶主要包括矛头蝮蛇血凝酶、白眉蝮蛇血凝酶及尖吻蝮蛇血凝酶。其中矛头蝮蛇血凝酶(Hemocoagulase Bothrops Atrox)是从矛头蝮蛇(Bothrops Atrox)蛇毒中经过透析、特异性亲层析等多种层析方法分离提取,并经冷冻干燥制得的具有止血作用的蛋白酶类物质[6-8]。
目前,矛头蝮蛇血凝酶及注射用矛头蝮蛇血凝酶已经收入《中国药典》2015年版第一增补本。在原料及制剂的质量标准中需要用到标准品,进行效价测定。在原料质量标准中还需要用到理化对照品,进行肽图鉴别及电泳分子量检查。本文研究建立了首批矛头蝮蛇血凝酶国家标准品及对照品,以此规范并提高矛头蝮蛇血凝酶原料及其制剂的质量。同时,通过对此类血凝酶类标准物质的质量研究,为其他酶类等大分子蛋白质类物质的质量分析及研究提供参考依据。
1 仪器与试药Mettler Toledo,XS205 Dual Range电子天平;Binder恒温恒湿培养箱;Shimadzu LC-20AD高效液相色谱仪;Binder FED115精密恒温真空干燥箱;Mettler Toledo MP230 pH计;Julabo CDBT19恒温水浴槽;Bio-Rad Gel Doc XR+凝胶成像仪;GE EPS601电泳仪;IKA 3D数字脱色摇床;Shimadzu MALDI-TOF/TOF Performance质谱仪;Milli-Q超纯水处理系统;Shimadzu紫外分光光度计等。
矛头蝮蛇血凝酶标准品及对照品原料来自辽宁远大诺康生物制药有限公司,均为冻干制品;凝血质控血浆来自MDC Hemostasis公司;福林试剂、TPCK处理的胰蛋白酶、二硫苏糖醇(DTT)、碘乙酰胺(IAA)及PNGase F酶均来自Sigma公司;色谱纯乙腈、三乙胺及三氟乙酸均来自Fisher公司;电泳试剂来自Bio-rad公司;等电点3~10混合Marker来自GE Healthcare UK公司;牛血清白蛋白(批号140619)来自中国食品药品检定研究院;其他试剂均为国产,分析纯。
2 方法 2.1 矛头蝮蛇血凝酶标准品的标定方法 2.1.1 理化分析(1)酸碱度
取待标品,加水溶解,用pH计测定酸碱度。
(2)干燥失重
采用减压干燥法,称取待标品适量,用精密恒温真空干燥箱,在温度60℃、压力约为1kPa条件下,以五氧化二磷为干燥剂,将待标品干燥至恒重,测得前后重量,计算减失重量百分比。
(3)装量差异
待标品为冷冻干燥制品,取5支待标品,分别测得总重及空瓶重,计算内容物重量。
(4)引湿性
称取待标品适量,采用恒温恒湿培养箱,在温度25℃、湿度80%条件下放置24h,测得前后重量,计算增重百分比。
2.1.2 效价测定取待标品按预估效价(100单位/支)加水精密稀释至每毫升1单位,作为供试品溶液。取低温保存的凝血质控血浆放至室温后,每支加水1 mL溶解,放置15 min,轻摇,使用前轻轻摇匀。精密量取凝血质控血浆溶液0.2 mL,加入直径1 cm的试管中,置37℃水浴中保温3 min,加入已于37℃预热的供试品溶液0.2 mL,立即混匀并计时,于55秒开始轻轻振摇,记录出现絮团时间,即为初凝时间。每支待标品平行测定5次,若有1次目测时间超过60±2秒时,重新测定;若有2次目测时间超过60±2秒时,则重新调整供试品溶液浓度再行测定,记录供试品溶液浓度,计算效价。在上述条件下,能使0.2 mL人-枸橼酸抗凝血浆在60秒凝固的酶量,定义为1单位[9]。效价计算公式:

|
效价标定方案:组织国内5个具有资质的实验室共同进行协作标定,每个实验室分发待标品6支,凝血质控血浆10支,每支待标品平行测定5次,每个实验室提交5支待标品的测定结果。汇总全部数据,计算25支待标品的均值、标准差、变异系数及95%可信限范围。
2.1.3 稳定性本品的保存条件为-20℃。稳定性研究包括短期稳定性和长期稳定性。短期稳定性模拟可能的极端运输环境,考察了待标品在25℃、相对湿度为75%以及40℃、相对湿度为75%条件下保存0天、5天及10天的效价。
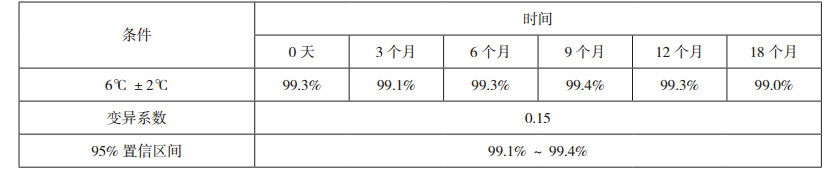
长期稳定性的保存条件为-18℃±2℃,考察了0天、3个月、6个月、9个月及11个月的效价。
2.2 矛头蝮蛇血凝酶对照品的标定方法 2.2.1 结构确证(1)N-末端氨基酸序列
委托北京大学生命科学学院进行N-末端氨基酸序列分析鉴定。
(2)分子量
取待标品1支,加水1 m L溶解,直接进行MALDI-TOF分子量测定。
(3)N-连接糖含量
取待标品1支,加水1mL溶解,作为原液。另取待标品1支,加50 mmol·L-1碳酸氢铵溶液1 mL溶解,取10μL,加100 mmol·L-1的DTT溶液1μL,混匀,56℃保温1 h,再加入250 mmol·L-1的IAA溶液1μL,室温暗处放置1h。取上述还原烷基化后的样品5μL,加入500 units·mL-1的PNGase F酶溶液1μL,37℃保温16 h进行酶切。将酶切后的样品用ZipTip C18柱进行脱盐处理。取原液和酶切后的样品分别进行MALDI-TOF分子量测定,由以下公式计算糖含量。

|
(4)肽图测定
取待标品1支,加水1mL溶解,取800μL,加入胰蛋白酶溶液80μL,于37℃水浴反应24h,取出,加入50%醋酸溶液100μL终止反应,用0.45μm微孔滤膜过滤。平行制备6份样品,分别进行HPLC色谱分析。采用C18色谱柱,流动相A为0.1%三氟乙酸水溶液,流动相B为0.1%三氟乙酸乙腈溶液,紫外检测波长为214 nm,柱温30℃,进样体积100μL,梯度洗脱条件为0~70 min。流动相B为0%~45%,70~75 min,流动相B为45%~70%,75~78 min,流动相B为70%~0%,保持至83 min结束。记录肽图谱并进行相似度计算。
2.2.2 理化分析(1)等电点
采用等电聚焦电泳法,取30%丙烯酰胺/亚甲基双丙烯酰胺5.0 mL,pH3~10两性电解质2.1 mL,水17.5mL,50%甘油3.0 mL,混匀,抽气5~10 min。加10%过硫酸氨溶液150μL,N, N, N', N'-四甲基乙二胺36μL,混匀后缓慢注入水平模具内,室温下聚合。将已聚合的凝胶放在冷却板上,其间涂以液体石蜡并避免产生气泡。用正极液(0.5 mol·L-1磷酸溶液)和负极液(0.2 mol·L-1氢氧化钠溶液)分别润湿正极与负极电极条,然后分别置于凝胶的正极和负极上,将电极对准电极条中心,加盖,按照恒压法,在起始电压200 V下预电泳30 min。然后将加样滤纸放在凝胶上,分别加供试品溶液(待标品1支,加水333μL溶解,加甲基红试液2μL,混匀)10μL,Marker溶液10μL。将电极对准电极条的中心,加盖。进行梯度电泳:电压200 V,维持60 min,电压400 V,维持120 min,电压600 V,维持120 min。电泳结束后,将胶片放入固定液中固定30 min后取出,放入考马斯亮蓝染色液中染色60 min,然后取出放入脱色液中脱色至背景无色,放入保存液中保存。将凝胶放入凝胶成像仪中进行拍照分析,计算等电点。
(2)凝血质样反应
取待标品1支,加水溶解并定量稀释至1 0 mL,作为供试品溶液。取凝血质控血浆1支,按照“2.1.2”节下方法处理,得凝血质控血浆溶液。取血浆溶液0.2 mL,于37℃保温2 min,加供试品溶液0.2 mL,于37℃振摇并计时,记录出现白色絮团时间。
(3)蛋白含量
采用福林酚法,以牛血清白蛋白为对照品,依照《中国药典》四部相关内容[10]进行测定,待标品每支加水5 mL溶解,平行配制3份供试品溶液,供试品溶液取样量为0.5 mL,在650 nm波长下测定对照品溶液和供试品溶液吸光度,以对照品溶液浓度与其对应吸光度进行线性回归,由回归方程计算每支待标品的蛋白含量,求平均值。
(4)酸碱度、干燥失重、装量差异、引湿性
测定方法同矛头蝮蛇血凝酶标准品。
2.2.3 纯度测定(1)电泳纯度
采用SDS-聚丙烯酰胺凝胶(SDS-PAGE)电泳法,依照《中国药典》四部相关内容[10]进行测定,分离胶浓度为12.5%,考马斯亮蓝染色。电泳完毕采用凝胶成像仪进行拍照分析。
(2)液相色谱纯度
色谱条件为采用C4色谱柱,流动相A为含0.1%三氟乙酸的0.1%三乙胺水溶液,流动相B为含0.1%三氟乙酸的0.1%三乙胺乙腈溶液,紫外检测波长为280 nm,柱温30℃,进样体积为50μL,梯度洗脱条件为0 min至20 min,流动相B为20%至66%,20 min至25 min,流动相B为66%至20%,保持至35 min结束。采用面积归一化法计算纯度。
2.2.4 稳定性本品短期稳定性考察方法同矛头蝮蛇血凝酶标准品;长期稳定性的保存温度为6±2℃,考察了18个月的稳定性,考察指标均为液相色谱纯度。
3 结果与讨论 3.1 矛头蝮蛇血凝酶标准品 3.1.1 理化分析结果本品水溶液的pH值为6.6。减压干燥失重为1.8%。平均装量为54.02mg,装量差异在±10%以内。本品引湿增重19.3%,《中国药典》规定引湿增重大于15%时,为极具引湿性[10],因本品为冻干标准品,用于效价测定,因此,在使用说明中注明了开封后一次性使用。
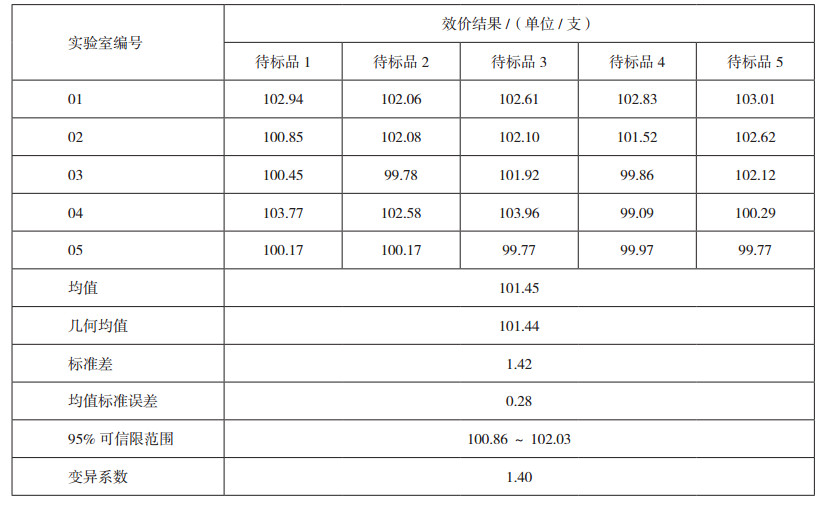
3.1.2 效价赋值作为效价测定用标准品,其最重要的定量指标即为效价。由于本品为首批研制的标准品,且无国际标准品,无法进行相对法的测定,因此采用绝对法对效价进行测定。效价为本品的特性量值,需要赋值准确。本文采用了协作标定的方式,组织了国内5家药检所及企业分别对本品进行效价测定,以5家实验室的测定结果经过统计为本品赋值,保证了结果准确性。统计结果见表 1,由结果可见各实验室之间变异系数为1.40,全部数据均在95%置信区间内,所有25个实验数据全部采纳。根据统计结果取均值,本品效价最终定值为101单位/支。
|
|
表 1 矛头蝮蛇血凝酶标准品效价协作标定统计结果 |
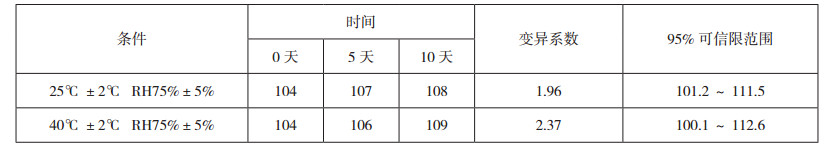
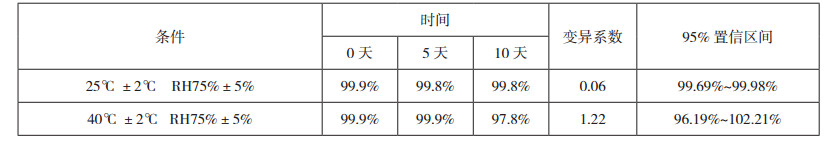
短期稳定性及长期稳定性的考察结果见表 2及表 3。由结果可见本品在25℃,75%RH(相对湿度)及40℃,75%RH条件下放置5天及10天后,其效价与-20℃条件下保存的样品效价比较,变异系数均小于5%,各时间点效价均在95%可信限范围内,本品短期极端条件下效价稳定。在-18℃±2℃条件下保存,长期效价稳定,目前已进行11个月的稳定性考察,更长期的稳定性考察仍在进行中。
|
|
表 2 矛头蝮蛇血凝酶标准品短期稳定性试验效价测定结果(效价:单位) |
|
|
表 3 矛头蝮蛇血凝酶标准品长期稳定性试验效价测定结果(效价:单位) |
作为鉴别及检查用对照品,首先需要保证其结构的准确且稳定,作为首批对照品,本文对其结构进行了一定的研究,保证其结构与理论值基本一致,并为后续的换批研制提供了比对的依据。其次,纯度研究也是考察对照品优劣的重要指标,本文采用SDS-PAGE电泳法和液相色谱法分别考察本品的纯度,两种方法互相佐证补充,保证了结果的准确性。
3.2.1 结构确证结果(1)N-末端氨基酸序列
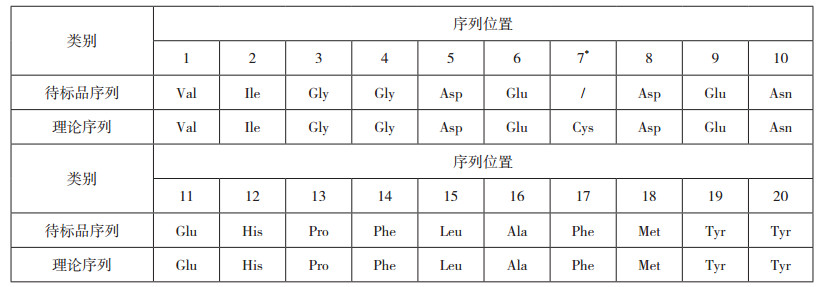
本品N-末端20个氨基酸测序结果见表 4,测得序列结果与理论序列一致。
|
|
表 4 矛头蝮蛇血凝酶对照品N端序列分析结果 |
(2)分子量及N-连接糖含量
经MALDI-TOF测定,本品分子量为32382。N-连接糖基化修饰的含量为19.1%。
(3)肽图
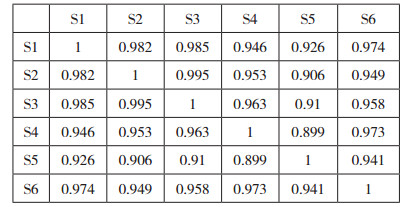
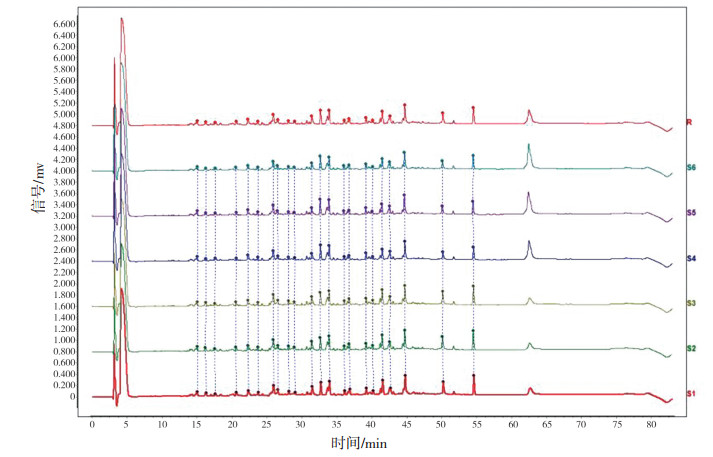
平行制备6份供试品,进行肽图测定,得到6份肽图谱,进行指纹图谱相似度计算,由6份图谱按平均值生成对照图谱(R)。图谱及相似度结果见图 1和表 5,结果显示各供试品之间相似度良好。
|
图 1 矛头蝮蛇血凝酶对照品肽图谱 |
|
|
表 5 肽图谱相似度计算结果 |
(1)等电点
经等电聚焦电泳法测定,本品测得等电点为6个,结果依次为4.021、4.203、4.499、4.899、5.495和6.370。
(2)凝血质样反应
按照2.2.2(2)节操作,本品供试品溶液在8.5秒出现白色絮团。说明本品具有凝血特性。
(3)蛋白含量
采用福林酚法测定,得到对照品溶液线性回归方程y=21.135x+0.0402,相关系数r=0.9993,由方程计算本品蛋白含量平均值为每支1.0 mg。
(4)其他理化指标
本品水溶液的pH值为7.2。减压干燥失重为6.9%。平均装量为4.27 mg,装量差异在±15%以内。本品引湿增重65.6%,《中国药典》规定引湿增重大于15%时,为极具引湿性,因本品为冻干制品,用于肽图鉴别和电泳分子量检查,不作为定量用对照品,引湿性对产品测定结果不产生影响,因此,在使用说明中注明了建议开封后一次性使用。
3.2.3 纯度测定结果(1)电泳纯度
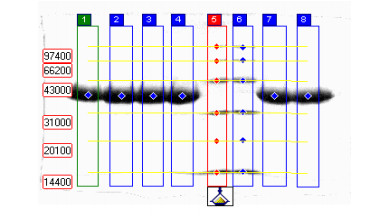
本品经SDS-PAGE电泳检测,其结果显示一条带,见图 2,说明本品电泳纯度较好。
|
图 2 矛头蝮蛇血凝酶对照品SDS-PAGE电泳图谱 |
(2)液相色谱纯度
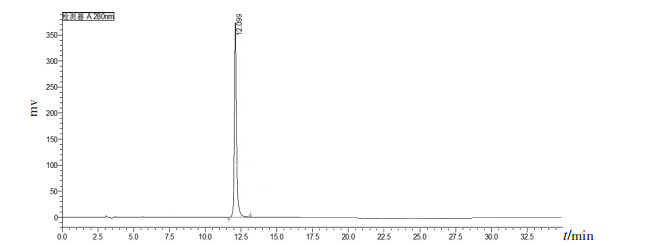
本品采用2.2.3(2)节方法测定,HPLC面积归一化纯度为100%,典型图谱见图 3,结果显示本品纯度较好。
|
图 3 矛头蝮蛇血凝酶对照品纯度测定色谱图 |
本品保存条件为-20℃,短期稳定性和长期稳定性的考察结果见表 6及表 7。由结果可见本品在25℃,75%RH及40℃,75%RH条件下放置5天及10天后,纯度与-20℃条件下保存的样品比较,变异系数均小于2%,各时间点纯度均在95%可信限范围内,本品短期极端条件下稳定。
|
|
表 6 矛头蝮蛇血凝酶对照品短期稳定性试验纯度测定结果 |
|
|
表 7 矛头蝮蛇血凝酶对照品长期稳定性试验纯度测定结果 |
长期稳定性考察了加速条件为6℃下保存18个月的纯度,由结果可见纯度均较好,本品长期稳定,目前已进行18个月的稳定性考察,更长期的稳定性考察仍在进行中。
4 结论本文对矛头蝮蛇血凝酶标准品的理化性质、效价及稳定性进行了研究标定,并通过统计学汇总协作标定的效价结果,为标准品进行赋值,用于矛头蝮蛇血凝酶原料及其制剂的效价测定。对矛头蝮蛇血凝酶对照品进行了一定的结构确证研究,并对其纯度、理化性质及稳定性进行了研究考察,保证了本品结构准确、纯度较高,可用于矛头蝮蛇血凝酶原料的鉴别及检查。
通过以上的研究标定,本文建立了首批矛头蝮蛇血凝酶国家标准品及对照品。作为蛇毒类血凝酶的代表,通过对此类血凝酶标准物质的研究,为其他酶类药物的质量分析及研究提供了依据,并为大分子蛋白类生化药物的研究及发展打下基础。
致谢: 衷心感谢参加协作标定的单位——辽宁省药品检验检测院、辽宁远大诺康生物制药有限公司、山东省食品药品检验研究院、天津市药品检验所。
| [1] |
郑颖, 沈居仁, 范泉水. 蛇毒血凝酶的比较[J]. 蛇志, 2008, 20(3): 218-219. DOI:10.3969/j.issn.1001-5639.2008.03.026 |
| [2] |
郝云飞, 刘国辉, 康强军. 注射用矛头蝮蛇血凝酶应用于腰椎退行性疾病手术中的有效性及安全性[J]. 临床合理用药, 2018, 11(2A): 48-52. |
| [3] |
许海艳, 杨见明. 矛头蝮蛇血凝酶不同用法对功能性鼻内镜手术止血效果的影响[J]. 中医药临床杂志, 2017, 29(12): 2113-2115. |
| [4] |
王兆钺. 注射用血凝酶体内外止血作用的研究[J]. 中国医院用药评价与分析, 2012, 12(6): 486-487. |
| [5] |
曹金铎. 注射用血凝酶临床应用的国内文献综述[J]. 中国医院用药评价与分析, 2012, 12(6): 485-486. |
| [6] |
Castro HC, Zingali RB, Albuquerque MG, et al. Snake Venom Thrombin-like Enzymes:from Reptilase to Now[J]. Cellular and Molecular Life Sciences, 2004, 61: 843-856. DOI:10.1007/s00018-003-3325-z |
| [7] |
Yau Sang Chan, Randy Chi Fai Cheung, Lixin Xia, et al. Snake Venom Toxins:Toxicity and Medicinal Applications[J]. Appl Microbiol Biotechnol, 2016, 100: 6165-6181. DOI:10.1007/s00253-016-7610-9 |
| [8] |
孙东, 石皎, 丁忠福, 等. 一种新的蛇毒凝血酶原激活物的分离纯化及特征[J]. 中国生物化学与分子生物学报, 2011, 27(12): 1141-1148. |
| [9] |
李秀琳, 孙东, 丁忠福, 等. 矛头蝮蛇血凝酶工作标准品的协作标定[J]. 中国药品标准, 2016, 17(2): 123-127. |
| [10] |
中国药典: 四部[S]. 2015: 附录69-70、96-97、378-379.
|
 2019, Vol. 33
2019, Vol. 33