2. 山东大学齐鲁医院, 济南 250012
2. Qilu Hospital of Shandong University, Jinan 250012, China
中药注射液是我国独有的注射制剂,随着中药注射液在临床的广泛使用,其所引起的药品不良反应呈增加趋势。因此,中药注射剂的安全问题得到广泛关注[1]。醒脑静注射液系在中医古方安宫牛黄丸基础上改制而成的静脉注射药物,其主要成分为麝香、冰片、郁金、桅子,辅料为聚山梨酯80、氯化钠,是中药常用的急救药品。2016年我院共发生14例醒脑静注射液所致的药品不良反应。其中,严重ADR病例占71.43%,在我院引起了广泛重视。为进一步了解醒脑静注射液发生不良反应的影响因素,通过对14例醒脑静注射液所致ADR进行总结、分析,探讨其发生规律,以期为儿童合理使用醒脑静注射液、减少不良反应的发生提供依据。
1 资料来源与方法 1.1 资料来源2016年我院醒脑静注射液所致药品不良反应案例,共14例。
1.2 入选标准根据国家药品不良反应监测中心的不良反应判断指导原则,入选案例须符合下列条件:①不良反应发生在用药之后;②符合已知的不良反应类型;③停药后消失或减轻。
1.3 方法对14例醒脑静注射液所致药品不良反应患儿的年龄、性别、原患疾病、过敏史、ADR/ADE发生时间、用法用量、溶媒、ADR/ADE累及器官、归转等进行回顾性分析。
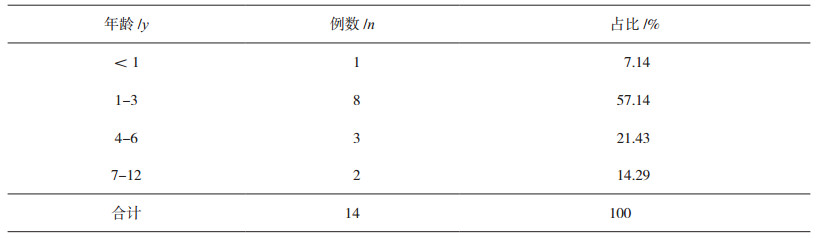
2 结果 2.1 患儿年龄与性别14例醒脑静注射液引起的ADR患儿中:男10例(71.43%),女4例(28.57%);年龄未满11月-7岁不等,具体分布见表 1。
|
|
表 1 患儿年龄分布 |
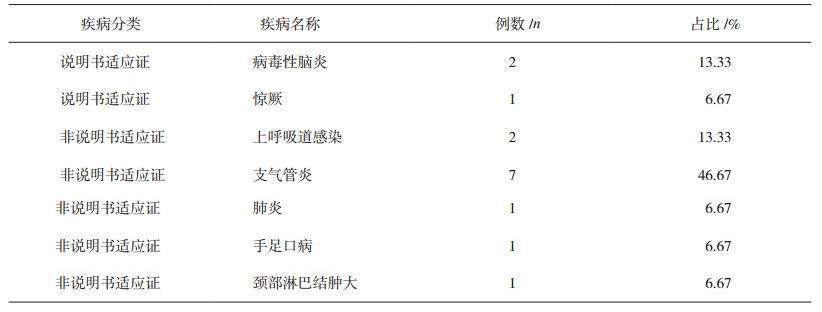
根据醒脑静注射液说明书的功能主治,对14例患儿使用醒脑静注射液的原因进行统计,见表 2。
|
|
表 2 患儿使用醒脑静注射液用药原因 |
醒脑静注射液说明书无儿童用药剂量,成人剂量为10~20 mL,儿童剂量按体重计算:儿童剂量=成人剂量×儿童体重/70 kg。14例患儿用药途径均为静脉滴注。使用醒脑静注射液的患儿体重、使用剂量[以成人最小剂量-中线值剂量-最大值剂量(10-15-20 mL)计算]见表 3,是否为超剂量用药见表 4。
|
|
表 3 使用醒脑静注射液的患儿体重及使用剂量 |
|
|
表 4 患儿年龄与醒脑静使用剂量统计表 |
8例患儿醒脑静注射液使用剂量超过或等于最大剂量,其余6例患儿未超过最大剂量,但均高于中线剂量。
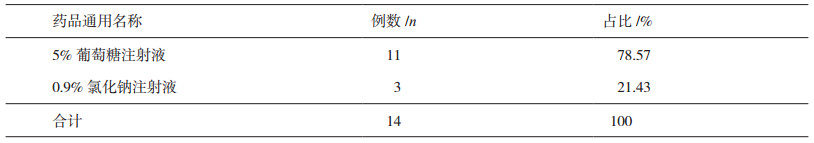
2.4 使用溶媒种类及浓度情况14例患儿使用最多的溶媒种类为5%葡萄糖注射液,其次为0.9%氯化钠注射液,详细情况见表 5,使用浓度情况见表 6。
|
|
表 5 使用每种溶媒的患儿例数及占比 |
|
|
表 6 醒脑静注射液配制浓度与ADR例数及占比 |
在静点醒脑静注射液导致的14例药品不良反应事件中,不良反应发生时间明确的有6例,其余8例未上报具体发生时间,详见表 7。
|
|
表 7 不良反应发生时间 |
根据《WHO药品不良反应术语集》对14例醒脑静注射液所致不良反应累及的系统-器官进行统计,结果见表 8。
|
|
表 8 ADR/ADE累及系统-器官及其临床表现 |
根据国家食品药品监督管理局ADR监测中心制定的ADR监测表及全国ADR监测网对上报人员的设定,将所有上报人员分成3类:医师、药师、护士。在14例醒脑静注射液所致药品不良反应的上报人员中,医师8例,护士6例。
2.8 药品不良反应归转及采取措施ADR归转是指本次ADR经采取相应的医疗措施后的结果,不是指原患疾病的结果。14例醒脑静注射液所致药品不良反应的结果:14例患儿在治疗期间全部治愈。采取的措施:①停药;②吸氧、抗过敏、降温。采取的医疗措施使用时间:2例为2天,12例为5分钟-2小时好转。
2.9 醒脑静注射液所致不良反应严重程度分级按WHO提供的药品不良反应分级标准,对醒脑静注射液所致的ADR严重性进行严重程度分级,详见表 9。
|
|
表 9 醒脑静注射液所致ADR的严重程度分级 |
中药注射剂发生不良反应主要是由于中药材所含的植物蛋白或有机物质在人体内形成半抗原,半抗原与体内血浆蛋白结合成全抗原引起的[2]。醒脑静注射液成分复杂,药物本身所含的大分子蛋白质和脂肪酸作为一种抗原进入机体,刺激免疫系统,产生抗体,在肥大细胞上形成抗原-抗体复合物附着,引起变态反应的发生[3]。其次,辅料聚山梨酯-80是醒脑静注射液常用的助溶剂,近年来,聚山梨酯-80引起过敏的报道常有出现,因此其安全性受到极大关注。目前研究表明,聚山梨酯-80能诱导细胞产生脱颗粒作用,引起过敏活性物质释放,从而导致过敏反应的发生。其引发的过敏反应属于非IgE介导的假阳性过敏反应[4]。
3.2 不良反应与患儿年龄、性别的关系据报道,儿童使用醒脑静注射液所致不良反应明显多于成人[3]。我院为儿童医院,患者是18岁以下患儿,14例醒脑静注射液所致ADR患儿年龄在11月~7岁不等(见表 1),发生不良反应最多的年龄段为1~3岁。儿童作为一个特殊的用药群体,一方面,由于各种生理功能发育尚未完善,外界侵袭的反应能力较差,比成人更易患病。另一方面,由于婴幼儿或新生儿肝、肾功能发育不完善,清除药物的能力差,药物代谢速度较慢,药物易通过血脑屏障,相对于成人而言,儿童对药物作用的敏感性更高,尤其对作用于中枢神经系统的药物,儿童更容易出现药物不良反应。醒脑静注射液能透过血脑屏障,直接作用于中枢神经系统[5],故更易造成不良反应的发生[6-7]。
文献报道[2, 8-9]醒脑静注射液所致不良反应中,男性明显多于女性。我院醒脑静注射液所致不良反应患儿中男性占71.43%,与报道结果一致。这可能与男女激素水平差异有关,可能因为醒脑静注射液成分较复杂,与某些成分对男性患儿影响较大有关[10],也可能与男孩住院治疗人数较多有关。
3.3 不良反应与醒脑静注射液用药原则的关系醒脑静说明书表明,其功能主治为用于气血逆乱,脑脉淤阻所致中风昏迷,偏瘫口喎,外伤头痛,神志昏迷;酒毒攻心,头痛呕恶,昏迷抽搐。脑栓塞、脑出血急性期、颅脑外伤,急性酒精中毒见上述症候者。我院醒脑静注射液所致ADR患儿中,属于说明书适应证的有3例,非说明书适应证11例。据林晓兰等报道[11],热证患者使用醒脑静注射液不良反应发生率为6.1%,非热证患者不良反应发生率为32.4%,非热证患者由醒脑静注射液引起的不良反应明显高于热证患者。根据《中成药临床应用指导原则》,中成药注射剂应用的基本原则:须辨证用药,依据中医理论,辨认、分析疾病的证候,针对证候确定具体治法,依据治法,选定适宜的中成药。中医药治病的精髓在于准确辩证,在使用中药注射剂前,要对患者的虚、实、寒、热、表、里等症候进行辩证,才可对症下药。醒脑静注射液有醒神开窍、清热解毒的效果,药性寒凉。因此,该药对热病实证有较为显著的治疗效果,但对寒证、虚症的患者不宜使用。我院醒脑静注射液均由西医医生开具处方。由于他们不太熟悉中医理论,在使用醒脑静过程中一般对病不对证,不能做到中医辩病与中医辨症相结合。所以,使用醒脑静注射液时,应严格按照药品说明书规定的功能主治使用,辨证施药,禁止超功能主治用药。因而,醒脑静注射液应由中医师开具,通过准确的辩证,减少不良反应的发生。
3.4 不良反应与醒脑静注射液剂量、浓度的关系醒脑静说明书中明确规定用法用量:静脉滴注一次10~20 mL,用5~10%葡萄糖注射液或0.9%氯化钠注射液250~500 mL溶解,未提供儿童用药剂量。根据说明书换算醒脑静注射液静滴溶液浓度为0.04 mL·mL-1。由于醒脑静注射液说明书无儿童用药剂量,临床医师只能根据成人剂量换算出儿童所需剂量。本文根据儿童体重计算相应用药剂量,有一定的科学性。根据表 4,14例患儿用药剂量均在理论用药剂量的中线剂量以上。其中,有8例使用醒脑静剂量大于或等于最高用药剂量,加之醒脑静注射液可透过血脑屏障,直接发挥作用,其成分较复杂,故可能会出现较多的药品不良反应。浓度过高引起药物不良反应的可能性较大,而浓度过低,可能导致药物治疗效果的降低。中药注射剂所致药品不良反应与剂量浓度的关系:剂量与ADR严重程度无关,与发生率有关,剂量越大,不良反应发生率相对较高;而浓度则与ADR严重程度有关,与发生率无关,即浓度越高,不良反应越严重[11]。由于我院醒脑静注射液发生严重不良反应病例数较多,可能与醒脑静注射液配制浓度高有关。此外,我国法律不允许以儿童为临床用药试验个体,生产企业未进行儿童用药相关试验,因而缺乏儿童使用醒脑静注射液的使用剂量依据。儿童使用醒脑静注射液的安全性尚待考证,故此建议临床医师谨慎用于儿童患者。
3.5 不良反应与醒脑静注射液使用溶媒的关系醒脑静注射液是将麝香、郁金、桅子蒸馏提取后,加入冰片、聚山梨酯-80、氯化钠混合溶解,过滤制得,为提取混合物。我院14例醒脑静注射液所致不良反应中,以5%葡萄糖注射液为溶媒的有11例(见表 5),占不良反应发生总例数的78.57%,以0.9%氯化钠注射液为溶媒仅有3例,这与刘宏明[3]等报道的结果极为相似。醒脑静注射液是提取混合物,并没有分离出能够进行完全定性和定量的产品。这决定了其成分复杂、内在质量不稳定,因而导致疗效不稳定,并影响药物安全性。醒脑静注射液与溶媒配伍后,往往导致微粒数明显增加,原因在于,配伍后酸碱度改变,其有效成分因溶解度降低而析出;或因加入其他成分可破坏原有混合物的溶解平衡,而导致溶解度较小的物质析出。另外,《中国药典》(2015版)中要求醒脑静注射液pH值应为5.0~7.0。若以0.9%氯化钠注射液做溶媒,氯化钠注射液的pH值为4.5-7,与醒脑静注射液pH值较为接近,相对于使用5%葡萄糖注射液(pH值为3.5-5.5),稀释后酸碱度改变较少,有效成分相对较稳定、安全。然而,以5%葡萄糖注射液为溶媒时,因为醒脑静注射液溶解于较大量的葡萄糖注射液中,pH值发生较大的变化,导致微粒析出较多,易增加药物不良反应的发生。
3.6 不良反应与醒脑静注射液所致ADR发生时间的关系由表 7可以发现,我院醒脑静注射液所致药品不良反应,均发生在4天以内,当天发生的7例,其中静滴5 min内发生的4例,6~10 min 1例,静滴过程中2例;第2天发生ADR共5例,其中静滴5 min之内1例,静滴过程中3例,静滴结束后1例;第4天发生的2例,均在静滴结束后发生。根据《100例醒脑静注射液的辩证应用及安全性评价》报道,热证不良反应发生时间一般在2周以后,非热证发生时间均在2周以内,2组不良反应发生时间情况的比较,其差异有统计学意义(P<0.01)[12]。我院14例醒脑静注射液所致药品不良反应均发生在4天以内,提示我院醒脑静注射液所致ADR患儿,中医辨症可能属于非热证用药。建议临床医生根据中医辨症使用醒脑静注射液。
3.7 不良反应与醒脑静注射液超说明书用药的关系美国医师协会(American Pharmacists Association)定义超药品说明书用药:适应证、给药方法或剂量在美国食品药品管理局(FDA)批准的药品说明书之外的用法。我国超药品说明书用药是指,药品使用的适应证、给药方法或剂量不在药品监督管理部门批准的说明书之内的用法。药品未注册用法的具体含义包括给药剂量、适应人群、适应证或给药途径等与说明书不同的用法。张小龙2014年《中药注射液超说明书用药调查》表明,中药注射剂超说明书用药情况达42.96%[13]。谭朝丹等在《中药注射剂超说明书使用情况调查分析》中指出,2014年中药注射剂超说明书用药高达56.07%[14]。我院是儿童医院,用药人群均小于18岁,醒脑静注射液使用过程中,超人群、超适应证、超剂量等超药品说明书用药多种情况并存,超药品超说明书用药状况相对成人更为严重。芦小燕等对高龄患者调研发现,超说明书用药引起的ADR概率明显高于常规用药[15]。李红燕等报道,儿童超药品说明书用药导致药品不良反应发生率较高[16]。根据对我院14例醒脑静注射液所致ADR统计,非说明书适应证占80%(见表 2)。非说明书适应证属于超说明书用药,而超说明书用药会增加用药安全隐患,导致较多不良反应的发生,并可能会增加药品不良反应事件发生的风险,故减少醒脑静注射液超说明书用药,可有效减少药品不良反应的发生。
3.8 不良反应严重程度情况分析我院14例患儿发生的不良反应,其严重程度见表 9。其中,严重不良反应占71.43%,这与张彩林等[17]报道不太相符。但鉴于我院醒脑静注射液所致不良反应严重病例较多,建议临床医师一定慎用于儿童,尤其慎用于3岁以下儿童。
4 建议醒脑静注射液作为中医急救药,具有独特的作用。通过对其发生药物不良反应影响因素的讨论,临床医生合理使用醒脑静注射液,能有效减少不良反应的发生,现总结如下:
1)醒脑静注射液成分复杂,易产生过敏反应,用药前应仔细询问患者情况、用药史和过敏史。过敏体质、对食物或药物有过敏史的患者或有过敏家族史的患者应谨慎用药。
2)临床医师应在使用醒脑静注射液前认真阅读说明书,明确其功能主治,严格按照说明书规定的适应证、用法、用量用药,减少超说明书用药;对药品说明书已明确的禁用和慎用情况应高度重视。
3)临床医师应注意中医的辩证施治,做到中医辩病与中医辩证相结合,禁止超功能主治用药,将醒脑静注射液用于热证患儿,可有效减少不良反应的发生。
4)醒脑静所致药品不良反应一般发生在静脉滴注开始前30分钟,建议医务工作者在滴注过程中加强监护。
5)我院醒脑静注射液所致ADR主体是1-3岁儿童,且严重不良反应所占比例较高,故建议在有可替代药物的情况下,3岁以下患儿不使用该注射液。
6)生产企业应加强醒脑静相关安全性研究,或利用现有数据,做科学分析,为临床儿童合理使用醒脑静注射液提供科学依据。
| [1] |
尹婕, 金少鸿. 中药注射剂不良反应现状及风险控制措施浅析[J]. 中国药事, 2013, 27(9): 989-993. |
| [2] |
吴国琳, 张力, 余国友. 中药注射剂发生不良反应常见原因分析及防范对策[J]. 中国中西医结合杂志, 2008, 28(12): 1137-1140. DOI:10.3321/j.issn:1003-5370.2008.12.031 |
| [3] |
刘宏明, 许莉莉, 崔冉, 等. 66例醒脑静注射液不良反应的文献分析[J]. 中国药物警戒, 2016, 13(2): 107-110. |
| [4] |
程欧, 高鹏, 涂家生, 等. 吐温-80质量与致敏关系的研究[J]. 中国药科大学学报, 2010, 41(3): 244-247. |
| [5] |
徐元虎. 醒脑静注射液的药理药效学研究临床应用现状[J]. 现代中西医结合杂志, 2010, 19(4): 507-510. DOI:10.3969/j.issn.1008-8849.2010.04.095 |
| [6] |
李智平. 我国儿童药物不良反应监测的过去、现在与展望[J]. 儿科药学杂志, 2011, 17(1): 11-14. |
| [7] |
Impicciatore P, Choonara I, Clarkson A, et al. Incidence of Adverse Drug Reactions in/out-Patients:a Systematic Review and Meta-analysis of Prospective Studies[J]. Br J Clin Pharmacol, 2001, 52(1): 77-83. DOI:10.1046/j.0306-5251.2001.01407.x |
| [8] |
戴逢伟, 李敏, 雷光远, 等. 15例醒脑静注射液不良反应病例分析[J]. 海峡药学, 2009, 21(8): 191-193. DOI:10.3969/j.issn.1006-3765.2009.08.109 |
| [9] |
邹箴蕾, 杨乐, 郭晓昕. 30例醒脑静注射液不良反应/事件文献分析[J]. 中国药物警戒, 2014, 11(11): 683-686. |
| [10] |
蔡蕴敏, 方欢. 我院1005例药品不良反应报告分析[J]. 中国药房, 2015, 26(11): 1509-1513. DOI:10.6039/j.issn.1001-0408.2015.11.24 |
| [11] |
吴国琳, 张力, 余国友. 中药注射剂发生不良反应常见原因分析及防范对策[J]. 中国中西医结合杂志, 2008, 28(12): 1137-1140. DOI:10.3321/j.issn:1003-5370.2008.12.031 |
| [12] |
林晓兰, 张维, 郭景仙, 等. 100例醒脑静注射液临床辩证应用及安全性评价[J]. 北京中医药, 2010, 29(9): 703-704. |
| [13] |
张小龙, 沈亚兵, 王晓军. 中药注射剂超说明书用药评价与药物研究分析[J]. 中国药事, 2015, 29(9): 993-998. |
| [14] |
谭朝丹, 时扣荣, 刘娟, 等. 中药注射剂超说明书使用情况调查分析[J]. 中成药, 2015, 37(9): 2096-2097. |
| [15] |
芦小燕, 陈维, 龚燕波, 等. 超说明书用药对高龄患者药品不良反应的影响[J]. 中国现代应用药学, 2014, 31(8): 1010-1013. |
| [16] |
李洪燕, 刘恩梅, 谢晓虹. 464例儿童用品不良反应/事件特点及超说明书用药情况分析[J]. 儿科药学杂志, 2017, 23(2): 29-33. |
| [17] |
张彩林, 杨春松, 兰亚佳. 国内儿童应用醒脑静注射液不良反应文献评价[J]. 川北医学院学报, 2016, 31(5): 641-644. DOI:10.3969/j.issn.1005-3697.2016.05.05 |
 2018, Vol. 32
2018, Vol. 32