2. 北京三药科技开发公司, 北京 100176
2. Beijing Sanyao Science & Technology Development Co., Beijing 100176, China
酪蛋白胨是以酪蛋白(从牛奶中提取,又称干酪素、酪朊、乳酪素)作为原材料,经胰蛋白酶消化水解、中和、过滤、浓缩精制而成的粉末。常用名:胰酪胨、胰酶水解酪蛋白等。酪蛋白胨与一般蛋白胨的区别在于酶解工艺处理及蛋白原料上,其水解程度更高、胨分子量分布均衡,具有色浅、易溶、透明、无沉淀等良好的物理性状,含有丰富的氮源、氨基酸等[1]。国际上普遍将酪蛋白胨用于微生物检验培养基的氮源[2],广泛应用于微生物学检验、医学卫生研究、医药工业生产、生物制品制造等领域[3-4]。《中国药典》 2015年版微生物检测体系在与国际接轨过程中全面采用酪蛋白胨替代了我国药品微生物检验长期使用的肉蛋白胨[5]。然而国内外普遍存在培养基质量差异以及批间质量不稳定问题[6]。培养基原料决定培养基品质[7-8],酪蛋白胨的产品质量直接影响微生物试验的结果。目前我国培养基质量标准体系建设较为落后[9],培养基原材料的系统研究较少。为把握当前市面常用酪蛋白胨的整体质量水平,选择具有代表性的国内外6个厂家的14批酪蛋白胨样品,参照B/T20142020-T-469胰酪蛋白胨检测方法(公告标准)[10]中的主要理化和微生物分析方法进行质量研究,为微生物检测实验室培养基配制和培养基企业生产提供参考。
1 材料与试剂 1.1 仪器与设备BINDER BD240/ BINDER KB240生物培养箱;Thermo Class AII生物安全柜;Mettler TOLEDO SevenMulti酸度计;Mettler TOLEDO HG53 Halogen Moisture Analyzer快速水分测定仪。
1.2 试验材料 1.2.1 样品共收集酪蛋白胨样品14批,其中进口样品5批(A企业1批;B企业1批;C企业3批:C1、C2、C3),国内产品9批(D企业3批:D1、D2、D3;E企业3批:E1、E2、E3;F企业3批:F1、F2、F3)。
1.2.2 试剂氢氧化钾(批号:040910,北京化学试剂公司);磷酸氢二钾(批号:050510,北京化学试剂公司);其余试剂均为国产分析纯。
1.2.3 培养基胰酪大豆胨琼脂培养基T S A(批号:4162945)、胰酪大豆胨液体培养基TSB(批号:2208053)均来自BD医疗器械(上海)有限公司。
1.2.4 试验菌株铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104];金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003];藤黄微球菌(Micrococcus luteus)[CMCC(B)28001];枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501];乙型副伤寒沙门菌(Salmonella paratyphi B)[CMCC(B)50094];白色念珠菌(Candida albicans)[CMCC(F)98001];以上菌株均来自中国食品药品检定研究院医学微生物菌种保藏中心。
1.2.5 工作菌液制备色素生成能力测定用菌液:分别取铜绿假单胞菌、金黄色葡萄球菌、藤黄微球菌35℃培养24 h的新鲜培养物,以0.9%氯化钠稀释至103 cfu· mL-1。
促生长能力测定用菌液:分别取铜绿假单胞菌、藤黄微球菌、枯草芽孢杆菌、乙型副伤寒沙门菌35℃培养24 h的新鲜培养物;白色念珠菌25℃培养48 h的新鲜培养物,以0.9%氯化钠逐级稀释至102稀释级(10~100 cfu·mL-1),101稀释级(1~10 cfu·mL-1),100稀释级(<1 cfu·mL-1)。各菌液均于60 min内使用。
2 方法 2.1 理化分析 2.1.1 干燥失重精密称定样品干粉适量,使用快速水分测定仪于105 ℃测定样品干燥失重。
2.1.2 酸碱度制备2%(w/v)的酪蛋白胨水溶液,121 ℃高压灭菌15 min,冷却,采用玻璃电极测定灭菌前后溶液的pH值。
2.1.3 碱性沉淀制备2%(w/v)的酪蛋白胨水溶液,以1 mol·L-1的氢氧化钾调节pH 8.5,121 ℃高压灭菌30 min,放置室温后,观察溶液的澄明度及是否有沉淀。
2.1.4 磷酸盐沉淀制备含0.5%(w/v)的磷酸氢二钾的2%(w/v)的酪蛋白胨水溶液,如需要,调节pH 7.5,121 ℃高压灭菌30 min,放置室温后,观察溶液的澄明度及是否有沉淀。
2.2 微生物学分析 2.2.1 耐热菌数称取样品于0.9%氯化钠中制成10%(w/v)的供试液,100 ℃煮沸30 min后,取1 mL用TSA培养基浇碟,35 ℃培养24 h计数。
2.2.2 色素生成能力测试取各样品(待测酪蛋白胨)10 g、氯化钠5 g、琼脂12 g、水1000 mL,混匀,必要时调节pH 7.0,灭菌后室温放置至约45 ℃,约20 mL/皿注皿,冷却,制成待测平板。
取TSA培养基同法制成对照平板。
分别取“1.2.5”节中各色素生成能力测定用菌液,以0.2 mL/皿同法涂布上述待测平板和对照平板,35 ℃倒置培养48 h,观察各平板上的色素产生情况。
2.2.3 促生长能力测试取样品(待测酪蛋白胨)适量,制备2%(w/v)水溶液,必要时调节pH 7.0,灭菌后无菌分装成10 mL/管(中试管),作为待测培养管。
取TSB同法制备作为对照培养管。
分别取“1.2.5”节下促生长能力测定用菌液各1 mL,分别接种至各待测培养管和对照培养管,每测试菌株每稀释级重复6次,35 ℃培养48 h后,累计各生长管数,按如下公式计算促生长能力。

|
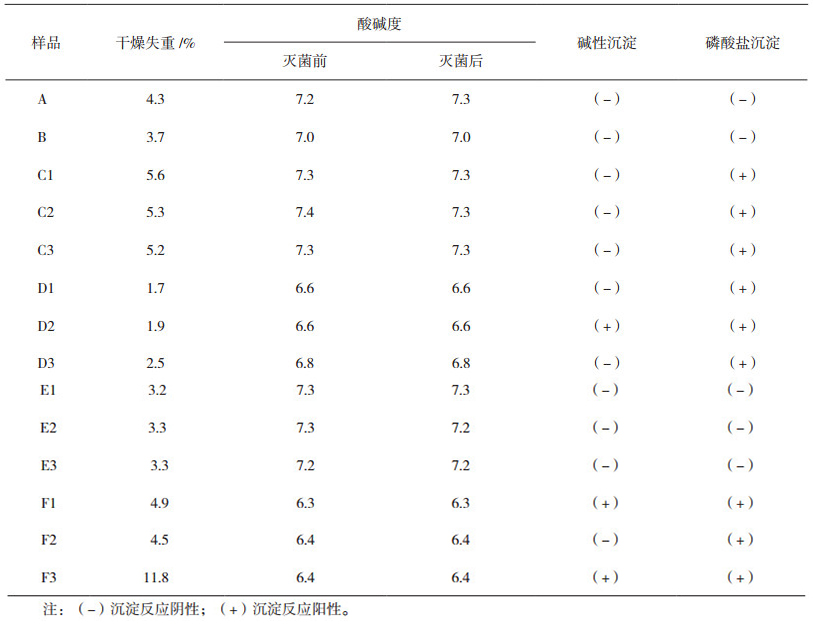
6个企业的14批样品分别呈类白色到淡黄色粉末,干燥失重大多分布在1.7%~5.6%,个别国产样品达11.8%;制成酪蛋白胨水溶液高压灭菌后观察,澄明度良好,均为澄清透明黄色液体,pH值分布在6.3~7.4,灭菌前后pH变化小于0.2;个别样品存在碱性沉淀和磷酸盐沉淀反应阳性(见表 1)。
|
|
表 1 理化分析结果 |
5批进口产品耐热菌计数均小于10 cfu·g-1,个别国产样品耐热菌数达390 cfu·g-1(见表 2)。
|
|
表 2 耐热菌数测定结果 |
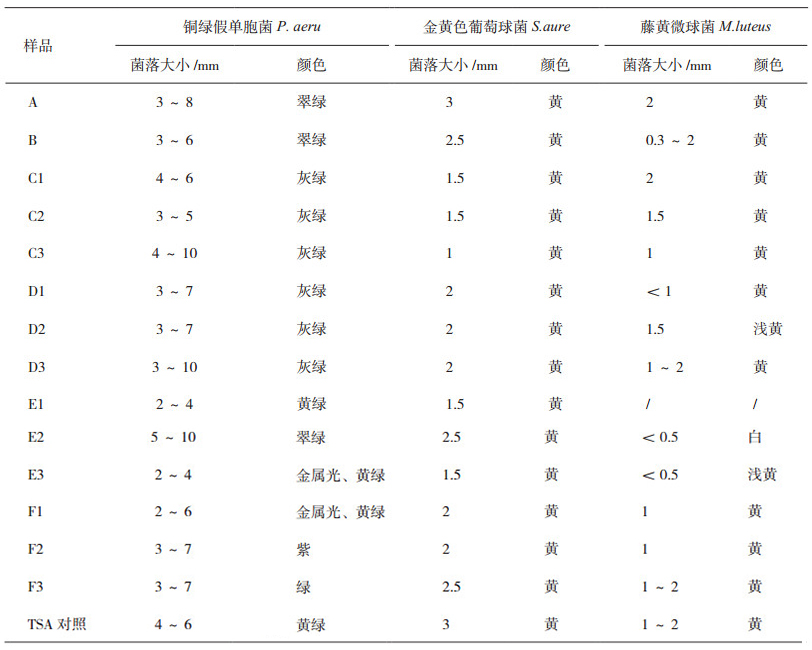
各厂家样品色素生成检验结果见表3。在相同试验条件下,各厂家样品对3种测试菌株的色素生成存在明显差异,国内E、F企业样品批间色素生 成能力差异较大。
|
|
表 3 色素生成试验结果 |
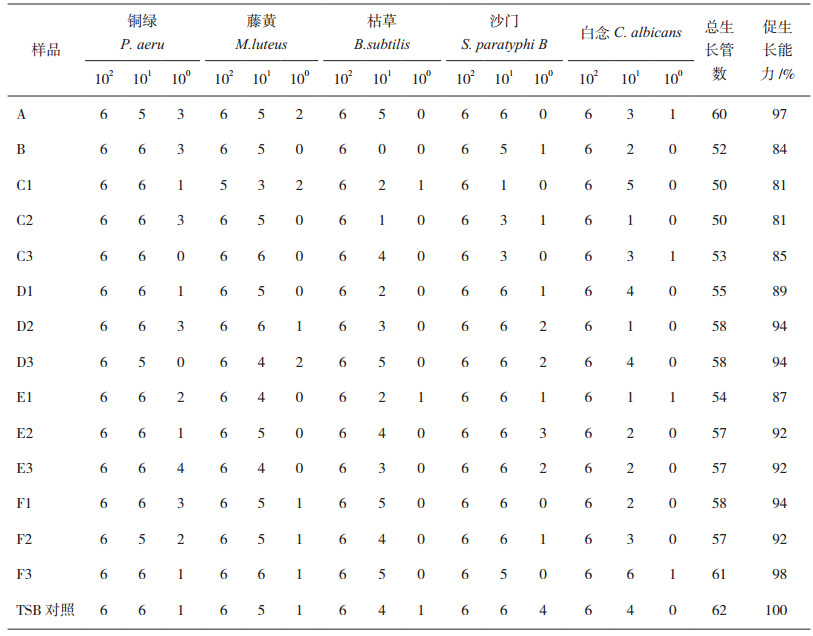
各厂家样品促生长能力检验结果见表 4,国内外企业样品促生长能力均大于80%。国内企业样品在促生长能力方面整体略优。
|
|
表 4 促生长能力检验结果 |
1)《中国药典》2015年版微生物培养体系与国际接轨[11],多个培养基配方中均涉及酪蛋白胨的应用。由于过去几十年我国一直使用以牛肉浸膏为代表的肉蛋白胨为培养基氮源,药典更替后,市面上酪蛋白胨的可及性和质量状况一直令人担忧。本文通过抽取市面流通的国内外酪蛋白胨样品进行比较分析,结果显示在影响培养基主要性能的促生长能力方面,国产酪蛋白胨与国外产品相当,可以满足国产培养基生产需要;但是多个理化和微生物学指标分析结果表明,国产酪蛋白胨在工艺水平和批间质量稳定性方面还有提升空间。
2)由于蛋白胨易吸潮,当水分含量过高时,蛋白胨在储存过程中易结块变质。通常以干燥失重不大于6.0%作为水分控制指标,国产个别批次酪蛋白胨干燥失重达11.8%,不符合规定,应提高干燥工艺水平和包装储存条件。
3)耐热菌数是可以很好地反映培养基应用特点的微生物荷载水平指标。培养基在最终应用时均有无菌性要求,如果原材料微生物荷载过高,必然引入干粉培养基,继而影响实验室配制灭菌效果,所以通常设定一定的耐热菌控制指标,如不得过100 cfu·g-1。国外酪蛋白胨基本检不出耐热菌,而个别国产样品耐热菌数较高,达390 cfu·g-1,不符合规定,应提高生产过程微生物控制水平。
4)色素生成能力、碱性沉淀、磷酸盐沉淀是我国培养基工作者积累的行之有效的蛋白胨质量控制经验指标,可以综合反映产品的工艺水平和产品特点,国内外不同企业产品以及国内同一企业不同批次产品在这几个指标上存在明显差异,很好地印证了这一点。这些差异的存在提示应根据不同原料的特点,关注对相应用途带来的影响,如某些pH条件下可能出现沉淀而影响培养观察、用于某些显色培养基中对菌落指示特性存在的差异等等。
5)本文由于样本量较少,仅就市场常见企业的部分样品进行了研究,有一定的局限性。但通过对《中国药典》新采纳的培养基原材料酪蛋白胨的集中研究,表明作为决定干粉培养基质量的原材料质量问题应引起充分关注。《中国药典》自2010年版开始建立的以对照培养基为核心的培养基适用性试验解决了实验室选择培养基的相对质量保证[12],但要根本提高国产培养基的质量和稳定性,还需要更充分的研究解决原材料质量问题。
| [1] |
齐奇, 刘河涛, 杨文君, 等. 胰蛋白酶水解制备胰酪胨的工艺条件研究[J]. 中国乳品工业, 2014, 42(5): 21-22. |
| [2] |
USP 36-NF31: Vol I[S]. 2013: 62.
|
| [3] |
陈天寿. 微生物培养基的制造与应用[M]. 北京: 中国农业出版社, 1995: 70.
|
| [4] |
纪绍梅. 微生物培养基质控与图解[M]. 北京: 科学技术出版社, 2006: 288.
|
| [5] |
中国药典: 四部[S]. 2015: 无菌检查法通则(1101) 137.
|
| [6] |
宋勤, 袁琳娜. 中国药典与欧洲药典无菌检查培养基灵敏度的比较实验[J]. 药物分析杂志, 2005, 25(11): 1367-1369. |
| [7] |
徐伟东, 许华玉, 范一灵, 等. 胰酪胨大豆培养基和改良马丁培养基的微生物促生长能力考察[J]. 中国药品标准, 2013, 14(4): 271-275. |
| [8] |
蔡芷荷, 严纪文, 卢勉飞, 等. 胰酪胨大豆肉汤培养基和改良马丁培养基在药品无菌检查中的比较研究[J]. 药物分析杂志, 2014, 34(10): 1847-1852. |
| [9] |
吴清平, 孟凡亚, 蔡芷荷, 等. 微生物培养基质量控制技术和标准[J]. 微生物学报, 2006, 33(6): 128-132. |
| [10] |
全国生化检测标准化技术委员会(TC387). G B/T35534-2017胰酪蛋白胨检测方法[S]. 2017.
|
| [11] |
胡昌勤. 药品微生物控制现状与展望[J]. 中国药学杂志, 2015, 50(20): 1747-1751. |
| [12] |
马仕洪, 杨美琴, 刘鹏, 等. 《中国药典》2010年版对照培养基的研制与应用[J]. 中国药事, 2012(8): 847-851. |
 2018, Vol. 32
2018, Vol. 32