2. 甘肃省中藏药检验检测技术工程实验室, 兰州 730070
2. Gansu Inspection and Testing Technical Engineering Laboratory for Chinese Herbal and Tibetan Medicine, Lanzhou 730070, China
大黄为蓼科植物掌叶大黄(Rheum palmatum L.)唐古特大黄(Rheum tanguticum.Maxim.ex Balf.)或药用大黄(Rheum officinale Baill.)的干燥根和根茎[1]。具泻下攻积,清热泻火,凉血解毒,逐瘀通经,利湿退黄之功效;主要用于实热积滞便秘,血热吐衄,目赤咽肿,痈肿疔疮,肠痈腹痛,瘀血经闭,产后瘀阻,跌打损伤,湿热痢疾,黄疸尿赤,淋证,水肿等症的治疗;外用可治疗烧烫伤[2-5]。目前,大黄市场上有以华北大黄、河套大黄等波叶组大黄掺假、混用等问题,因其含有土大黄苷,不含或少含番泻苷,无泻下作用,从而影响了大黄药材及饮片的使用安全和质量[6-9]。为此,2015年全国中药材及饮片评价性抽验选择大黄为其中一个品种,进行全面的质量考察,以确保公众用药安全有效。
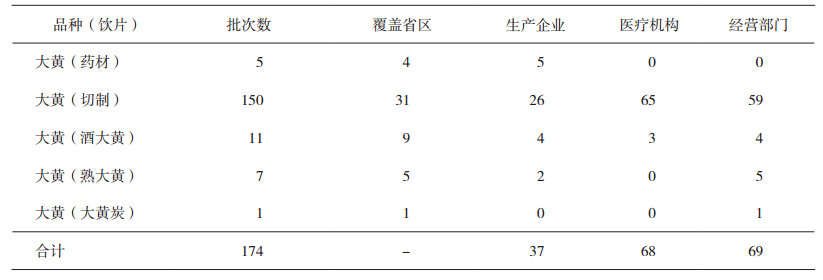
1 样品来源本次评价性检验共收到除香港、澳门、台湾外22个省份、5个自治区、4个直辖市共31个省级行政区的174批大黄样品,包括药材及4种饮片规格,被抽样单位涉及经营部门69个、医疗机构68个、生产企业37个,样品来自142家生产企业。结果见表 1。
|
|
表 1 2015年大黄抽样数据 |
大黄收载于《中国药典》2010版第一增补本,包括大黄药材及其4种饮片规格,明确规定了制法、性状、鉴别、检查、浸出物及含量测定等项[1]。因市场上出现以华北大黄、河套大黄等伪品冒充大黄药用的情况,国家食品药品监督管理局于2010年颁布了药品检验补充检验方法和检验项目批准件(批准件编号2010001),专属检查土大黄苷。甘肃省药品检验研究院选择了针对性强的项目开展检验,见表 2。
|
|
表 2 2015年大黄检验项目和检验依据 |
大黄药材及其饮片共计174批样品,其中152批次合格,22批次不合格,总体合格率为87%。
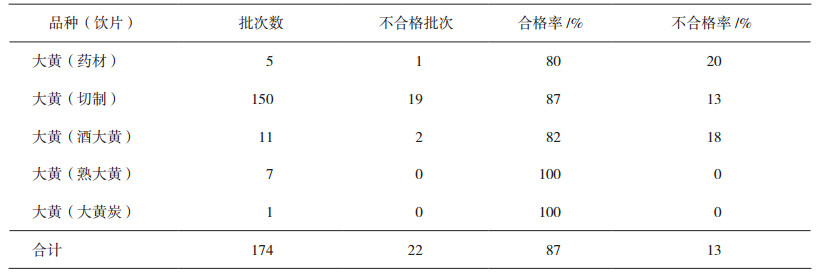
大黄药材共5批,4批符合规定,合格率为80%;但因样品数量太少,不足以反映全面真实情况。大黄饮片共计169批,148批符合规定,合格率为88%。总体情况见表 3。
|
|
表 3 2015年大黄药材及其饮片检验结果 |
22批不合格样品中,有11批检出土大黄苷,为华北大黄、河套大黄掺伪或混用;有1批薄层鉴别和游离蒽醌不符合规定,可能是产地加工不当、贮存时间过长或贮存条件不当所致;有7批因霉变及生虫,性状不符合规定;有3批样品直径在1~3 cm,为甘肃地方习用品种水根[10-11],但抽样地分别在重庆、宁夏、江苏,不能依据甘肃地方标准进行检验,故性状不符合规定。
4 开展的探索性研究2015年,全国大黄药材及其饮片评价性抽验所开展的探索性研究主要有大黄中游离蒽醌的一测多评方法研究;不同加工方法对大黄中蒽醌类成分的影响;大黄中64种农药残留的本底调查与评价;大黄中有害重金属残留的本底调查与评价;大黄中有害重金属残留特征的研究。
在依据现行标准检验过程中发现,大黄及其饮片进行总蒽醌和游离蒽醌含量测定时,均需测定5种成分,配置过程繁琐;且5个对照品中,大黄酸和大黄素甲醚的溶解性差,造成对照品配制的浓度不准确;芦荟大黄素和大黄酚的稳定性差,放置时间较长或放置温度较低,导致对照品析出,最终导致样品中游离蒽醌成分测定出现偏差。为提高检验结果的准确性及检验效率,节约检验成本,开展了建立大黄游离蒽醌一测多评方法的研究。由于大黄素对照品溶解性和稳定性都较好,故选择其作为一测多评法的对照品[12-16]。
4.1 仪器和材料 4.1.1 仪器Waters e2695型液相色谱仪(美国Waters公司),METTLER XS205型电子天平(瑞士METTLER公司),METTLER AE240型电子天平(瑞士METTLER公司),KH-250 DE型数控超声波清洗器(昆山禾创超声仪器有限公司)。
4.1.2 试药芦荟大黄素对照品(中国食品药品检定研究院,批号110795-201308)、大黄酸对照品(中国食品药品检定研究院,批号110757-200206)、大黄素对照品(中国食品药品检定研究院,批号110756-201512)、大黄酚对照品(中国食品药品检定研究院,批号110796-201319)、大黄素甲醚对照品(中国食品药品检定研究院,批号110758- 201013),均为含量测定用;甲醇为色谱纯,水为超纯水。
4.2 方法 4.2.1 色谱条件Agilent ZORBAX Eclipse Plus C18色谱柱(4.6 mm×250 mm,5 µm),流动相为甲醇-0.1%磷酸溶液(85:15),流速1 mL·min-1,柱温为室温,检测波长254 nm。理论板数按大黄素峰计算大于3000。
4.2.2 对照品溶液的制备分别精密称取芦荟大黄素对照品、大黄酸对照品、大黄素对照品、大黄酚对照品、大黄素甲醚对照品适量,加甲醇分别制成每1 mL含芦荟大黄素、大黄酸、大黄素、大黄酚各80 µg,大黄素甲醚40 µg的溶液;分别精密量取上述对照品溶液各2 mL,混匀,即得(每1 mL中含芦荟大黄素、大黄酸、大黄素、大黄酚各16 µg,含大黄素甲醚8 µg)。一测多评法,只需按上述方法配制大黄素对照品。
4.2.3 供试品溶液的制备取本品粉末(过四号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量;加热回流1 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
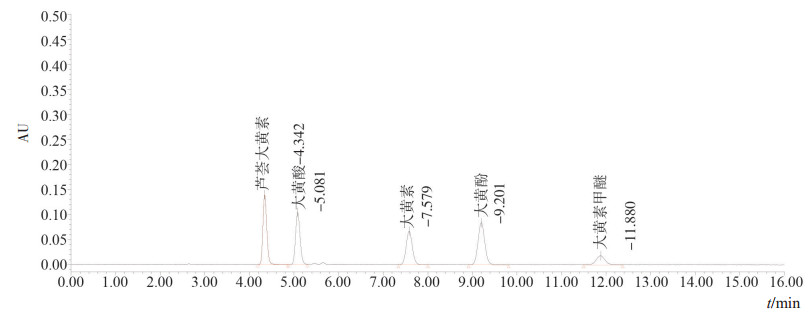
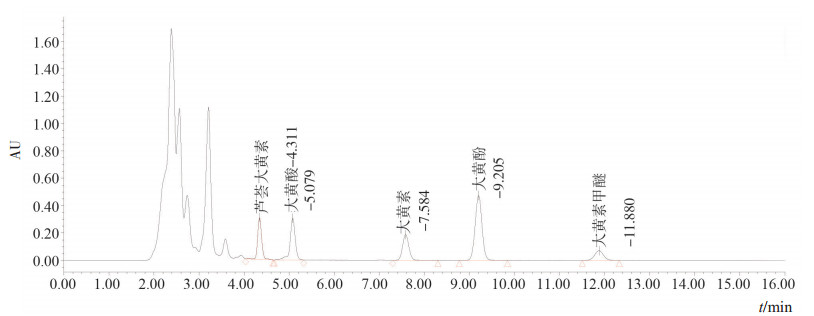
4.2.4 外标测定法分别精密吸取对照品溶液与供试品溶液各10 µL,注入液相色谱仪,测定,即得。色谱图见图 1,图 2。
|
图 1 大黄混合对照品液相色谱图 |
|
图 2 大黄供试品液相色谱图 |
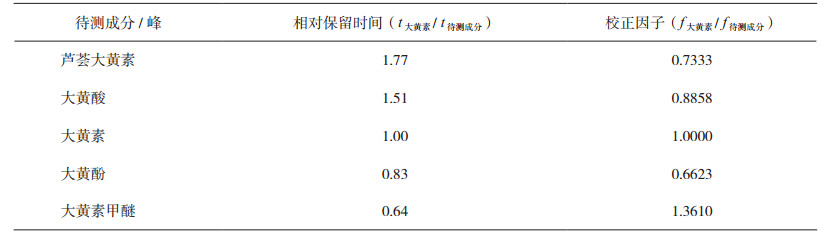
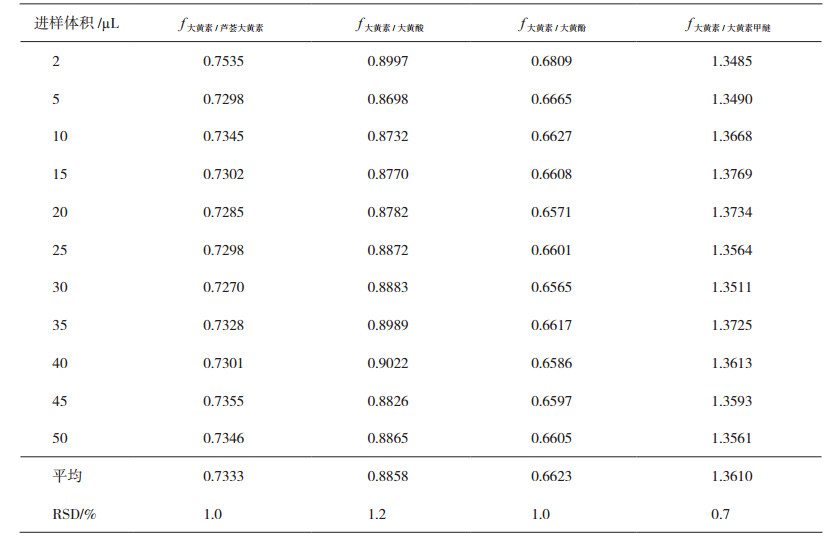
精密吸取大黄素对照品溶液与供试品溶液各10 µL,注入液相色谱仪,测定。以大黄素对照品为参照,计算芦荟大黄素、大黄酸、大黄酚和大黄素甲醚的相对保留时间,其相对保留时间应在规定值的±5%范围之内。相对保留时间及校正因子见表 4。
|
|
表 4 蒽醌类成分的相对保留时间和校正因子 |
以大黄素的峰面积为对照,分别乘以校正因子,计算芦荟大黄素、大黄酸、大黄酚和大黄素甲醚的含量。
4.3 方法学考察 4.3.1 线性关系考察分别配制3.285~82.12 µg·mL-1的芦荟大黄素、3.420~85.50 µg·mL-1的大黄酸、3.476~86.90 µg·mL-1的大黄素、3.263~81.57µg·mL-1的大黄酚和1.633~40.83 µg·mL-1的大黄素甲醚对照品溶液系列浓度,精密量取10 µL,分别注入液相色谱仪,测定峰面积,以各对照品浓度(µg·mL-1)为X轴,以峰面积积分值为Y轴,进行线性回归。各对照品回归方程和线性范围:
Y芦荟大黄素=53559X-35678 r=0.9999
线性范围0.03285~0.8212 µg;
Y大黄酸=43901X-23880 r=0.9997
线性范围0.03420~0.8550 µg;
Y大黄素=39224X-29979 r=0.9999
线性范围0.03476~0.8690 µg;
Y大黄酚=59516X-43102 r=0.9999
线性范围0.03263~0.8157 µg;
Y大黄素甲醚=28933X-11959 r=0.9998
线性范围0.01633~0.4083 µg。
4.3.2 精密度考察精密吸取混合对照品溶液10 µL,连续进样6次,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的峰面积积分值的RSD分别为0.8%、0.9%、0.9%、0.7%、0.8%(n=6),表明精密度良好。
4.3.3 重复性考察取同一批供试品粉末,按照“4.2.3”节下方法平行制备6份供试品溶液,按上述色谱条件测定并计算芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的含量。上述5种成分的测定结果RSD分别为2.3%、3.0%、1.3%、1.2%、3.0%(n=6),表明重复性良好。
4.3.4 稳定性考察取同一份供试品溶液,分别于0、2、4、6、8、10、15、20、24 h进样测定,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的峰面积RSD分别为0.9%、0.8%、1.6%、1.4%、1.3%,表明供试品溶液在24 h内稳定。
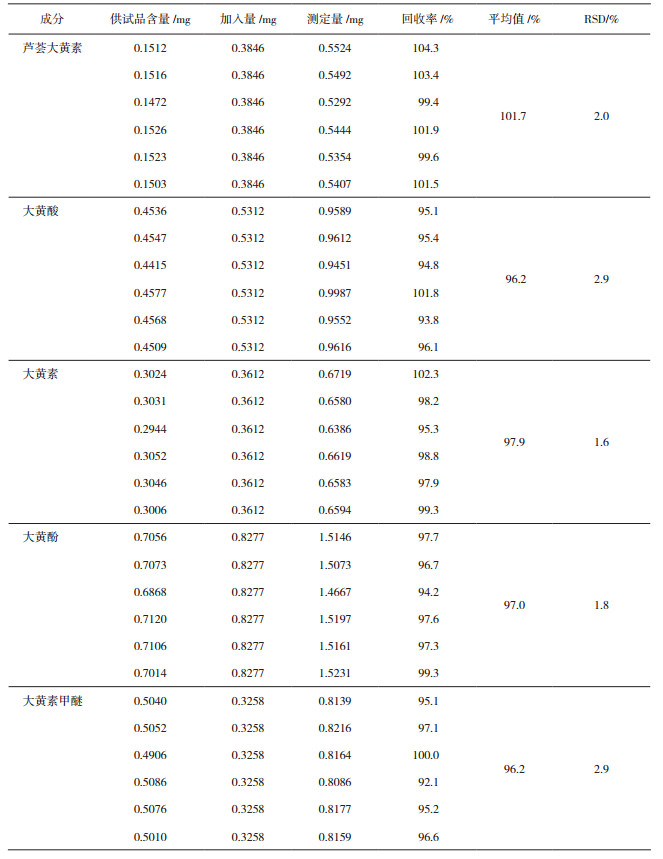
4.3.5 回收率考察取已知含量的供试品粉末6份,每份各约0.25 g,精密称定,分别置具塞锥形瓶中,分别精密加入“4.2.2”节下制备的对照品溶液适量,按照“4.2.3”节下方法平行制备,测得芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的含量。平均回收率见表 5,表明该方法的加样回收试验结果良好。
|
|
表 5 大黄中5种成分加样回收率试验 |
分别精密吸取对照品溶液与供试品溶液10 µL,注入液相色谱仪,测定,即得。
4.3.7 校正因子的计算在一定的线性范围内,紫外检测器的响应值(A)与组分浓度(C)成正比,在对多组分的物质进行含量测定时,可以先选定一个合适的组分作为内标物,建立该组分与其他组分的校正因子(ƒ),如公式所示:
f=(As/Cs)/(Ar/Cr)
用内标物与校正因子测定其他组分含量的计算公式如下:
Cx=(f×Ax)/(As/Cs)
计算公式中,As为内标物质的峰面积;Ar为对照品的峰面积;Ax为供试品的峰面积;Cs为内标物质的浓度;Cr为对照品的浓度;Cx为供试品的浓度。计算结果见表 6。
|
|
表 6 以大黄素为内标,其余4个蒽醌类成分的校正因子 |
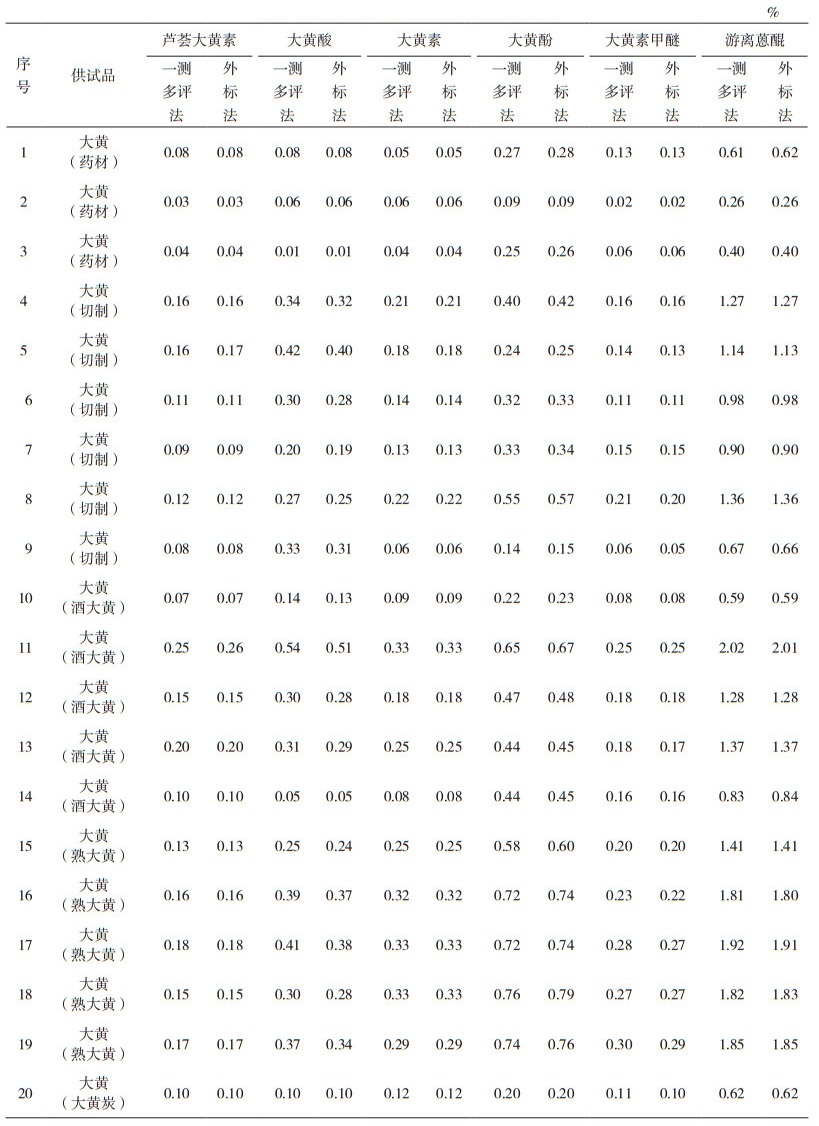
分别采用外标法和内标法计算大黄及其饮片中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的含量,数据结果见表 7。
|
|
表 7 大黄及其饮片游离蒽醌含量的测定结果 |
通过本次抽验发现,大黄药材及其饮片仍存在一些质量问题。首先,存在掺伪掺假问题,伪品主要以华北大黄、河套大黄为主。其次,存在发霉及虫蛀问题。建议加强中药材及其饮片贮存条件和贮存时间的监管。
另外发现,饮片名称不规范,由于各地用药历史文化等差异,中药饮片的名称必较混乱,如出现西大黄、炒大黄等不规范名称。建议进一步规范大黄饮片炮制方法,规范饮片名称。
5.2 标准和检验方法存在的问题通过本次大黄检验,认为现行标准翔实,确切可行,基本可以体现大黄药材及其饮片的质量。尤其是对大黄的4个饮片规格,描述较为详细,各饮片规格项下均列出了检验项目以及标准规定。
但是,大黄药材及其饮片含量测定操作较为繁琐,并且,部分对照品溶解性差。为提高检验效率,建议在保证检验质量的前提下,简化检验操作,用一测多评法测定大黄中总蒽醌和游离蒽醌的含量,避免对照品溶解性差所带来的测定偏差。
5.3 有关监管建议建议加强对大黄药材及其饮片生产、加工、流通、使用多环节的监管,不断完善和修订标准方法。对造假、掺伪及以次充好等违法行为进行跟踪监管,保障公众用药安全有效。
| [1] |
国家药典委员会编. 中国药典2010年版第一增补本[M]. 北京: 中国医药科技出版社, 2010: 77-78.
|
| [2] |
何正显. 大黄的化学成分、药理作用及其在临床急症中的应用[J]. 中国中医急症, 2007, 1(2): 227-229. |
| [3] |
于建玉. 中药大黄药理作用研究进展及其临床应用[J]. 中国现代药物应用, 2016, 10(11): 286-287. |
| [4] |
邬博. 大黄的药理作用研究进展[J]. 中国中医药现代远程教育, 2015, 13(20): 152-154. DOI:10.3969/j.issn.1672-2779.2015.20.079 |
| [5] |
张慧林. 大黄的药理作用及临床应用分析[J]. 光明中药, 2015, 30(5): 1119-1121. |
| [6] |
兰志琼. 大黄叶泻下、止血作用的实验研究[J]. 中药材, 2005, 28(3): 204-206. |
| [7] |
严孝金. 从化学、药效和毒性角度比较认识正品大黄与土大黄[J]. 中国中药杂志, 2014, 39(19): 3876-3880. |
| [8] |
热比姑丽·伊斯拉木. 土大黄研究进展[J]. 科技导报, 2013, 31(30): 67-71. DOI:10.3981/j.issn.1000-7857.2013.30.010 |
| [9] |
刘红淼. 土大黄的药理作用及临床应用研究进展[J]. 中国药房, 2013, 24(15): 1422-1425. DOI:10.6039/j.issn.1001-0408.2013.15.28 |
| [10] |
甘肃省食品药品监督管理局编. 甘肃省中药材标准[M]. 兰州: 甘肃文化出版社, 2009: 51-55.
|
| [11] |
甘肃省食品药品监督管理局编. 甘肃省中药炮制规范[M]. 兰州: 甘肃文化出版社, 2009: 28-30.
|
| [12] |
吴潍. 一测多评法测定清火胶囊中5个大黄蒽醌类成分含量[J]. 浙江中医杂志, 2015, 50(10): 771-773. |
| [13] |
王智民. 一测多评法建立的技术指南[J]. 中国中药杂志, 2011, 36(6): 657-658. |
| [14] |
王智民. "一测多评"法中药质量评价模式方法学研究[J]. 中国中药杂志, 2006, 31(23): 1925-1927. DOI:10.3321/j.issn:1001-5302.2006.23.001 |
| [15] |
张红伟. "一测多评"法在中药质量控制中的研究进展[J]. 海峡药学, 2010, 22(11): 88-90. DOI:10.3969/j.issn.1006-3765.2010.11.039 |
| [16] |
高慧敏. 适合中药特点的质量评价模式-QAMS研究概述[J]. 中国中药杂志, 2012, 37(4): 405-408. |
 2018, Vol. 32
2018, Vol. 32