2. 绍兴民生医药有限公司, 绍兴 312000
2. Minsheng Group Shaoxing Pharmaceutical Co. Ltd., Shaoxing 312000, China
长春瑞滨是半合成的长春花生物碱,具有广谱抗肿瘤活性,属于细胞周期特异性抗癌药,由法国皮尔法伯制药公司(Pierre Fabre)研发。酒石酸长春瑞滨阻断染色体在有丝分裂过程中的分离,临床主要用于治疗非小细胞肺癌、转移性乳腺癌等[1-2]。酒石酸长春瑞滨原料药标准已收载入EP、USP和《中国药典》中。
酒石酸长春瑞滨为白色或类白色粉末或结晶性粉末;无臭[3]。酒石酸长春瑞滨的合成中要用到催化剂四氟硼银(AgBF4)[4],其含量在现行版欧洲药典标准中通过测定硼、氟、银元素作为杂质控制,其中银限度为5 μg·mL-1[5]。EP标准中采用原子吸收火焰法测定杂质银[6],《中国药典》未控制催化剂的残留;同时,两个标准均未对有害元素进行控制。2018年USP要求对进口原料药中的铅、镉、砷、汞等多种有害元素采用ICP-MS方法进行检测[7]。与原子吸收法相比,ICP-MS具有准确稳定、检出限低、基体干扰少、多元素同时测定等优点[8],在化学药品及中药的重金属检测中有很多应用[9-14],采用在线内标测定,更可有效消除ICP-MS的仪器漂移、抑制基体干扰。为更好地保证药品安全性,本研究结合USP要求采用ICP-MS技术,探索建立快速测定酒石酸长春瑞滨中催化剂银残留和多种有害元素的测定方法。
1 试验部分 1.1 仪器与试药 1.1.1 仪器Agilent 7700X电感耦合等离子体质谱仪(Agilent科技);XS205电子天平(梅特勒托利多公司);Milli-Q-Reference超纯水机(密理博公司)。
1.1.2 试剂硝酸(Merck,AR);水为超纯水。
1.1.3 标准物质钒、铬、钴、镍、铜、砷、钼、镉、钡、铅混合元素标准溶液(1000 μg·mL-1,o2si公司,批号:10071238-1);锡、锑混合元素标准溶液(1000 μg·mL-1,o2si公司,批号:10071238-3);汞单元素标准溶液(1000 μg· mL-1,o2si公司,批号:143369-9);银单元素标准溶液(1000 μg·mL-1,Aladdin,批号:S117587-G1224055);钪单元素标准溶液(1000 μg·mL-1,GSB 04-1750-2004);锗单元素标准溶液(1000 μg·mL-1,GSB 04-1728-2004);铟单元素溶液标准物质[100 μg·mL-1,GBW(E)080271-10071];铋单元素溶液标准物质[100 μg· mL-1,GBW(E)080271-12011]。
1.1.4 供试品酒石酸长春瑞滨原料药由绍兴民生医药有限公司提供(批号:VBT01507001-S-G、VBT01507001-S-Y、VBT01507002-S-G、VBT01507002-S-Y、VBT01507003-S-G、VBT01507003-S-Y)。
1.2 试验方法 1.2.1 仪器工作条件镍锥,在He模式下调谐,经优化的工作参数:功率1550 W;采样深度8.0 mm;雾化室温度2 ℃;载气流速1.03 L·min-1;进样速度0.10 r·s-1;氧化物比值0.450%;双电荷比值0.825%。
1.2.2 溶液的制备 1.2.2.1 内标溶液的制备各精密量取钪、锗、铟、铋内标元素溶液0.1 mL,置100 mL量瓶中,加超纯水稀释至刻度,摇匀,即得。各元素浓度为钪1 μg·mL-1、锗1 μg·mL-1、铟0.1 μg·mL-1、铋0.1 μg·mL-1。在仪器测定时通过蠕动泵在线加入内标溶液。
1.2.2.2 标准溶液的制备取银单元素标准溶液(1000 μg·mL-1)0.10 mL,置100 mL量瓶中,用5%硝酸稀释至刻度,摇匀作为储备液(1000 ng·mL-1),同法制得汞元素储备液(100 ng·mL-1),钒、铬、钴、镍、铜、砷、钼、镉、锡、锑、钡、铅12个元素储备液(100 ng·mL-1)。取银元素储备液用5%硝酸稀释成0、1、5、20、50、100 ng·mL-1系列浓度的标准溶液。精密吸取汞元素标准溶液用5%硝酸稀释成0.0、1.0、3.0、4.0、5.0、10.0 ng·mL-1系列浓度的溶液。精密吸取混合元素标准溶液用5%硝酸稀释成含钒、铬、钴、镍、铜、砷、钼、镉、锡、锑、钡、铅12个元素浓度均为0.0、1.0、2.0、4.0、10.0、20.0 ng·mL-1的系列溶液。
1.2.2.3 供试品溶液的制备称取样品约0.25 g,置聚四氟乙烯消解罐内,加硝酸5 mL,混匀,80℃电热板上预消解30 min,放冷,盖上内盖,旋紧外套,置微波消解仪内,进行消解。消解完全后,取消解内罐置电热板上缓缓644中国药事2018年5月第32卷第5期CHINESE PHARMACEUTICAL AFFAIRS zhgysh加热至红棕色蒸气挥尽,用超纯水转移置25 mL量瓶中,并用超纯水稀释至刻度,摇匀,作为供试品溶液。同法制备样品空白溶液(100 mg·mL-1)。
1.3 方法学考察及试验结果 1.3.1 线性关系考察以超纯水为空白背景,在优化的试验条件下,依次测定各个浓度的标准溶液,以测定元素的计数值与其对应内标元素的计数值之比为纵坐标(Y),相应浓度(ng·mL-1)为横坐标(X),绘制标准曲线,各元素线性方程、相关系数、线性范围见表 1,结果表明各元素的标准曲线线性关系良好,相关系数在0.9988以上。
|
|
表 1 各元素线性关系考察结果 |
在最佳试验条件下,连续测定10份试剂空白溶液,计算标准偏差,以连续测定空白样品溶液响应值的3倍标准偏差(3SD)所对应的银元素浓度作为检测限[6]。试验结果:银、钒、铬、钴、镍、铜、砷、钼、镉、锡、锑、钡、铅、汞检出限分别为0.003、0.020、0.141、0.069、0.077、0.362、0.031、0.057、0.022、0.078、0.017、0.724、0.095、0.005 ng·mL-1。
1.3.3 重复性试验取批号为VBT01507001-S-G的样品6份,分别按“1.2.2.3”节方法制备供试品溶液,按“1.2.1”节仪器工作条件进行测定,计算元素含量。结果各元素RSD在2.5%~15.0%,表明重复性结果能满足痕量测试要求。
1.3.4 加样回收率试验取同一批号VBT01507001-S-G样品,共9份,每份约0.25 g,精密称定,置容量瓶中,加入“1.2.2.2”中的标准储备液,加入量以最终样品浓度为标准系列的中间浓度为100%,同时加入50%、150% 2个水平的标准储备液,按供试品溶液制备步骤进行消解处理,并最终定容置25 mL样品管中,测定样品溶液,计算加样回收率及RSD,结果见表 2,表明各元素的回收率均在86%~110%,符合痕量分析要求。
|
|
表 2 各元素回收率试验结果 |
取“ 1. 1. 4 ”节6批供试品,分别按“1.2.2.3”节方法制备供试品溶液,按“1.2.1”节仪器工作条件进行测定。结果表明银残留量比较稳定,在0.23~0.25 mg·kg-1,而其他有害元素是由于污染产生的,含量较低,其中钒在0.004~0.005 m g · k g-1,铬在0. 0 7 ~ 0. 1 9 m g · k g-1,钴在0.001~0.06 mg·kg-1,镍在0.07~0.10 mg·kg-1,铜在0.01~0.50 mg·kg -1,砷在0.0005~0.001 mg·kg -1,钼在0.0006~0.007 mg·kg -1,镉在0.0001~0.0004 mg·kg -1,锡在0.0005~0.003 mg·kg-1,锑在0.0000~0.0008 mg·kg-1,钡在0.00~0.09 mg·kg-1,铅在0.002~0.08 mg·kg-1,汞在0.0002~0.0006 mg·kg-1。
2 测量不确定度的评定通过计算方法的不确定度,可以较系统地分析方法中影响结果的主要因素[15]。根据《测量不确定度评定与表示》,不确定度分为A类、B类。A类不确定度是样品本身的不均匀性引起的不确定度,其公式为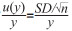
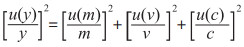
|
其中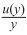
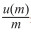

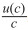
以银残留量为例计算不确定度,其中A类不确定度为同一批号(VBT01507001-S-G)6份样品银含量的结果得到,计算结果为0.0103 ng·mL-1;B类不确定度由以下因素产生,包括万分之一天平(计算结果为3.3×10-4 ng·mL-1)、25 mL容量瓶(计算结果为1.0×10-3 ng·mL-1)、测量得到的浓度(包括配制标准曲线的容器产生的不确定度,计算为0.0147 ng·mL-1,标准曲线拟合产生的不确定度,计算为0.025 ng·mL-1),从计算结果看产生不确定度的主要因素是样品的均一性和标准曲线的线性拟合程度(r2),因此,在试验中要注意样品混合均匀,标准曲线的线性拟合越高越好。
3 讨论相对于火焰原子吸收法(FAAS)、石墨炉原子吸收法(GFAAS)和原子荧光法(AFS),ICP-MS具有极低的检出限,此方法更加准确可靠、灵敏便捷,可用于酒石酸长春瑞滨中银残留级多种有害元素的测定,能有效控制酒石酸长春瑞滨的质量安全。本试验选择铟、锗、钪、铋作为内标元素,并通过蠕动泵在线加入内标溶液,可改善质谱分析时存在的基体效应,一定程度上校正仪器漂移误差,抑制基体干扰效应,提高准确率。由测量不确定度评定可知采用电感耦合等离子质谱法测定酒石酸长春瑞滨中各元素含量时,其测量不确定度主要来源于采用标准浓度系列拟合的曲线求得的样品溶液浓度,而样品称量和溶液定容引入的不确定度影响很小。由元素浓度导致的2个分量中,主要是拟合曲线影响最大,因此,电感耦合等离子质谱仪的稳定性是测量准确与否的关键所在。
| [1] |
RK Gregory, IE Smith. Vinorelbine:A Clinical Review[J]. British Journal of Cancer, 2000, 82(12): 1907-1913. DOI:10.1054/bjoc.2000.1203 |
| [2] |
Bryan A F, Trailokya N P. Safety and Efficacy of Vinorelbine in the Treatment of Non-small Cell Lung Cancer[J]. Clinical Medicine Insights:Oncology, 2011, 5(10): 131-144. |
| [3] |
酒石酸长春瑞滨[S]//中国药典: 二部, 2015: 1182-1183.
|
| [4] |
刘素云, 阙日明. 酒石酸长春瑞滨的合成[J]. 中国医药工业杂志, 2010, 41(9): 645-648. |
| [5] |
EP 9. 0[S]. 2016: 3912-3914
|
| [6] |
Vinorelbini Tartra[S]//EP 8. 0, 2013: 3539-3541.
|
| [7] |
General Chapters〈232〉[S]//USP40, 2016.
|
| [8] |
冯先进, 屈太原. 电感耦合等离子质谱法(ICP-MS)最新应用进展[J]. 中国无机分析化学, 2011, 1(1): 46-52. |
| [9] |
陈阳, 杨永健. 化学原料药中19种金属杂质的检测研究[J]. 药物分析杂志, 2012, 32(4): 631-635. |
| [10] |
李莉, 赵桂莉. 微波消解-电感耦合等离子体质谱(ICP-MS)法测定化学原料药中痕量钯含量[J]. 中国无机分析化学, 2016, 6(1): 6-9. |
| [11] |
陈在敏, 邹义栩, 王传之. ICP-MS法测定莲子中重金属元素含量[J]. 海峡药学, 2013, 25(9): 83-84. |
| [12] |
周海燕, 杨峻山, 周应群, 等. 微波消解/电感耦合等离子体质谱法测定西洋参重金属及有害元素含量[J]. 中国医院药学杂志, 2011, 31(11): 889-891. |
| [13] |
张弓, 黄剑林, 李海涛, 等. ICP-MS法测定青海地区常用40种藏药材中8种重金属[J]. 中成药, 2012, 34(12): 2391-2394. DOI:10.3969/j.issn.1001-1528.2012.12.032 |
| [14] |
李丽敏, 王柯, 季申. 电感耦合等离子质谱法测定肾康注射液中重金属及有害元素[J]. 药物分析杂志, 2012, 32(2): 277-281. |
| [15] |
王欣美, 王柯, 季申. ICP-MS法测定中药中铜、砷、镉、汞、铅含量的不确定度评定[J]. 齐鲁药事, 2012, 31(3): 136-140. |
| [16] |
ISO/IEC17025: 1999 Genera L Requirements for the Competence of Calibration and Testing Laboratories[S]. 1999: 5-8.
|
| [17] |
中国合格评定国家认可委员会. CNAS-GL05测量不确定度要求的实施指南[S]. 2011.
|
 2018, Vol. 32
2018, Vol. 32 

