丙型肝炎病毒(Hepatitis C virus, HCV)慢性感染可导致肝脏慢性炎症坏死和纤维化,部分可发展为肝硬化甚至肝细胞癌,严重危害患者的健康和生命。目前,聚乙二醇干扰素α(PEG-IFN)联合利巴韦林(Ribaviri,RBV)(PR方案)仍然是我国慢性丙型病毒性肝炎(chronic hepatitis C,CHC)主要的抗病毒治疗方案[1]。但PR方案在治疗过程中,几乎所有患者都有不同程度的不良反应(ADR),主要涉及免疫系统、神经系统、血液系统、内分泌系统等,常有贫血、头痛、失眠、食欲下降及白细胞下降等,严重者甚至有抑郁症,大大降低了患者治疗的依从性,影响患者生活质量,从而导致抗病毒药物剂量减少或疗程缩短,达不到抗病毒目的[2-5]。因此,如何通过有效干预抗病毒药物的ADR以达到持续病毒应答的治疗目的是临床亟待解决的问题。地芪固本口服液(批准文号:甘药制字Z12002211)是甘肃省第二人民医院(以下简称“我院”)多年临床验方研制的院内制剂,主要由熟地、黄芪、党参、女贞子、枸杞等中药成分组成,具固本扶正的功效。该药在肿瘤患者化疗过程中可有效改善血细胞减少、疲劳等ADR[6]。本研究将地芪固本口服液与抗病毒药物联合应用,观察其在CHC治疗过程中所致ADR的预防和改善作用,为临床治疗提供安全有效的中医药干预方法和思路。
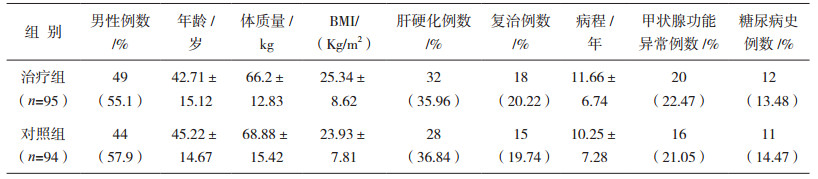
1 资料与方法 1.1 一般资料来自我院感染科于2013年8月-2015年7月门诊或住院收治的189例CHC患者,均符合2004年《丙型肝炎防治指南》 [1]诊断标准。所有患者随机分为对照组94例、治疗组95例。其中脱落16例(治疗组6例,对照组10例),脱落率8.47%,主要原因为患者不愿意继续参加研究(治疗或随访)、ADR和经济原因。两组患者性别、年龄、体重指数(Body mass index,BMI)、病程、HCV RNA水平、ALT、并发症等资料比较,差异无统计学意义(P>0.05),具有可比性。详见表 1、表 2。
|
|
表 1 患者的基线情况(x±s或例/%) |
|
|
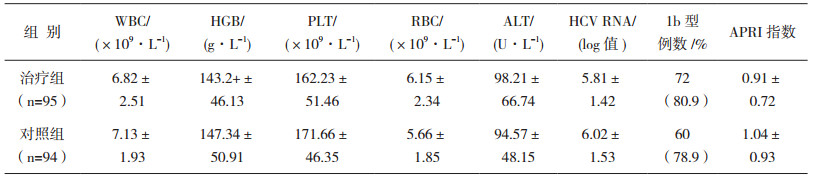
表 2 患者的基线情况(x±s或例/%) |
诊断符合2004年《丙型肝炎防治指南》 [1]。
1.3 纳入标准① 符合2004年《丙型肝炎防治指南》 [1]诊断标准的CHC患者;②年龄18~65岁之间;③男性或者女性;④HCV-RNA定量≥1×103 copies/mL;⑤处于肝功能代偿期;⑥半年内未应用过干扰素治疗的患者;⑦血常规正常者;⑧患者自愿参加本项研究,并签署知情同意书。
1.4 排除标准① 合并其他类型病毒性肝炎或HIV感染的患者;②入组时ALT≥10×正常值上限和/或TBI≥5×正常值上限者;③伴有心、肾、肺、内分泌、血液、代谢及胃肠道等严重原发病者;④西医诊断为重型肝炎(含急性、亚急性及慢性重型肝炎);⑤病人有干扰素和利巴韦林绝对禁忌证者,有相对禁忌证综合患者情况考虑;⑥病人不能合作;⑦长期酗酒、吸毒而未戒断者;⑧哺乳、妊娠或正准备妊娠的妇女;⑨正在参加其他药物的临床试验者。
1.5 剔除标准① 纳入后发现有不符合标准的病例;②在观察中脱落无任何可利用数据者;③虽符合标准,但纳入后未参加干预或无任何随访记录;④非规定范围内联合用药,特别是合用对试验结果影响较大的药物,影响了有效性和安全性判断。
1.6 治疗方法采用随机数字表法将患者随机分为治疗组和对照组。治疗组和对照组均给予聚乙二醇干扰素α-2a180μg,1周1次,皮下注射和按体重口服利巴韦林1000 mg/天(体重<75 kg)或1200 mg/天(体重>75 kg),疗程48周,治疗结束后随访24周。治疗组加用地芪固本口服液,一次50 mL,一日2次,口服。对于ADR的处理用药,参考《慢性丙型病毒性肝炎抗病毒治疗专家共识》(2009)[7]和2004年的《丙型肝炎防治指南》 [1]。
1.7 观察指标 1.7.1 ADR监测及评价标准:ADR的监测和管理参照卫生部2011年版颁布的《不良反应报告和监测管理办法》 [8],ADR术语和分级参照美国国立卫生研究院、国家癌症研究所《常见不良反应事件评价标准(CTCAE)》(v4.02:2009/9/15)[9]。ADR严重程度分5级:1、2、3、4、5级;ADR监测分为三级监测:1)日常监测:患者自我感知的不适症状和每周随访时的一般检查,包括体重、疲劳情况、皮肤、五官、口腔、体温、脉搏、血压等;2)常规监测:按照2004年《丙型肝炎防治指南》 [1]和文献报道[8],定期进行血常规、肝肾功、甲状腺功能、血糖监测等;3)特殊监测:有异常的症状、体征或检查指标或者需要干预治疗时进行的监测,依据患者临床情况制订监测的频率和项目。
1.7.2 患者的抑郁状态评分:参考Zung 1965年编制的抑郁自评量(Selfrating depression scale,SDS)[10],用于衡量抑郁状态的轻重程度及其在治疗中的变化,共20个项目,其中精神病性情感症状2个项目、躯体性障碍8个项目、精神运动性障碍2个项目、抑郁的心理障碍8个项目。按照中国常模结果,SDS标准分的分界值为53分,53~62为轻度抑郁,63~72为中度抑郁,72分以上重度抑郁。
1.8 统计学分析方法 1.8.1 ADR数量的统计:ADR发生率,同一患者同样性质的ADR在治疗和给药结束随访的过程中出现多次,统计为1例;同一患者不同性质的ADR分别统计。
1.8.2 统计方法:全分析集数据采用SPSS 22.0统计软件分析。定量数据采用x±s描述并采用重复测量设计方差分析。同时间点不同组的多重比较采用独立样本的t检验,同组不同时间点的多重比较采用LSD-t法;分类数据采用例数和百分比或率[n(%)]描述,率的比较采用χ2检验;ADR的严重程度采用完全随机设计两独立样本的秩和检验。P≤0.05为差异有统计学意义。脱落病例/缺失数据在随机化后至少接受四次治疗且至少有一次完整的疗效评价和安全性评价数据的,均按照末次观测值结转进行处理。违背方案数据的处理:存在可能影响试验结果的违背方案的患者数据,均予以剔除。
2 结果 2.1 ADR记录和关联性情况本次研究中,随机入组的189例(治疗组95例,对照组94例)患者入组后均至少接受四次治疗且至少有一次完整的病毒学应答指标评价和安全性评价数据,SDS测评对照组有8例因疲劳等ADR中途退出测评。治疗组ADR记录756例次,其中肯定的56.35%(426/756),很可能的23.94%(181/756),可能的12.43%(94/756),其他(可能无关、待评价、无法评价)7.28%(55/756)。对照组ADR记录954例次,其中肯定的57.75%(551/954),很可能的24.32%(232/954),可能的11.64%(111/954),其他(可能无关、待评价、无法评价)6.29%(60/954)。最终进行评价ADR的治疗组患者95例,发生ADR 701例次,对照组患者94例,发生ADR 894例次。本次研究中未发现与地芪固本口服液有关联的ADR。
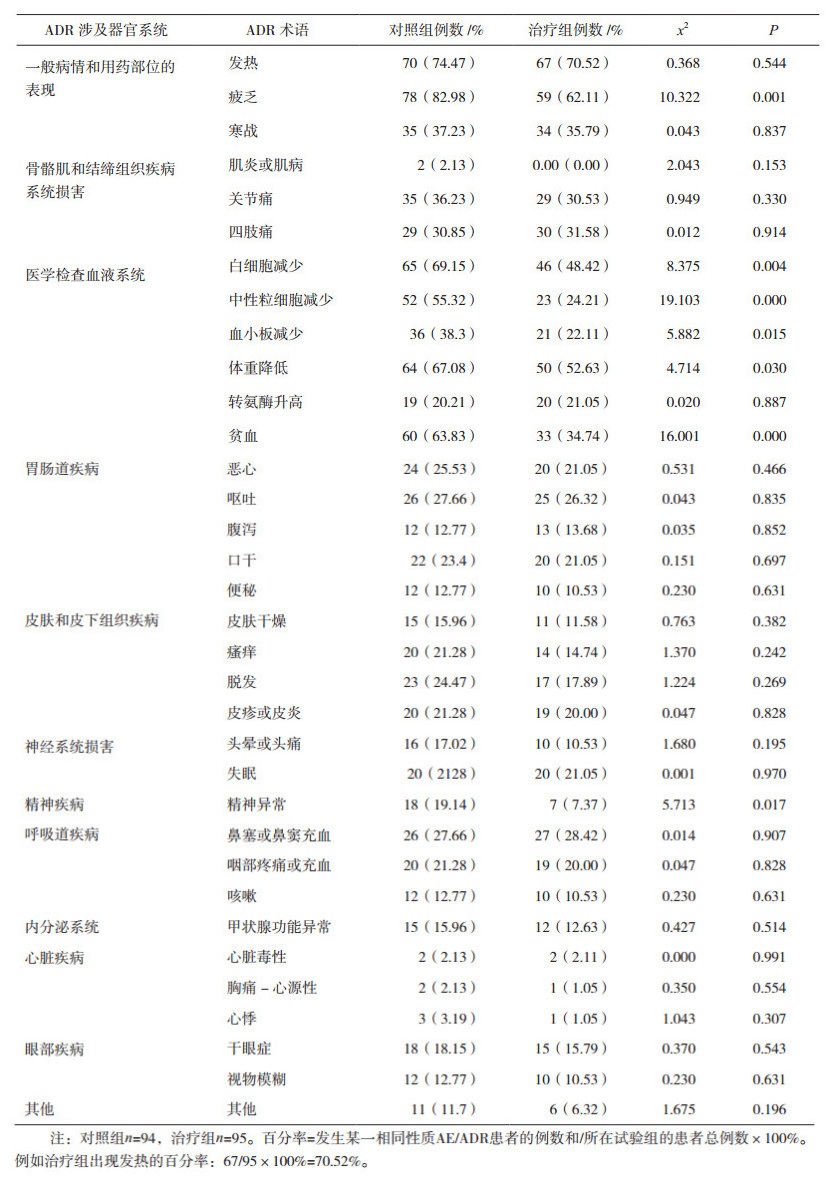
2.2 ADR发生率的基本情况从整体上看发生了至少一次ADR的患者治疗组81.05%(77/95),对照组95.76%(90/94),两者差异有统计学意义(P≤0.05)。两组患者的ADR涉及一般病情和用药部位的表现、骨骼肌和结缔组织疾病系统损害、血液系统、胃肠道疾病、皮肤和皮下组织疾病、神经系统等器官系统和医学检查异常等多个方面;两组发生ADR总例次数分别是701例次和894例次,人均发生例次数治疗组远低于对照组(6.88±4.56,8.95±5.71)(P≤0.05);从具体ADR看,治疗组在多个方面低于对照组,其差异有统计学意义(P≤0.05)详见表 3。
|
|
表 3 两组患者ADR发生率情况 |
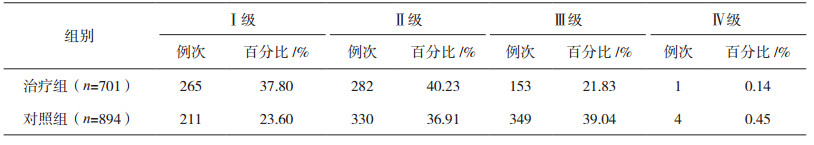
本项研究中未出现因ADR死亡的病例;治疗组和对照组在ADR的严重程度均以1级和2级为主(78.03%,60.51%),两组严重程度的百分率经秩和检验Z=8.030,P<0.05,差异有统计学意义。详见表 4。
|
|
表 4 ADR严重程度情况 |
对照组94例患者中有10例因ADR或其他原因中途退出治疗,8例患者在治疗过程中,自述疲劳、烦躁中途退出各种量表的测评,结果完整参与量表测评的对照组患者76例。治疗组因ADR和其他原因退出6例,剩余89例均全程参与了抑郁量表的测评。两组抑郁评分在治疗的前期(1~24周)与基线相比是增加的(P≤0.05),抑郁评分最高发生在治疗的12~24周,后期的症状明显好于前期,治疗结束抑郁评分基本恢复到基线水平,停药后抑郁评分继续好转,停药12~24周基本稳定。治疗组在治疗期间和治疗结束后的SDS得分均低于对照组,自治疗12周之后的各监测时间点抑郁症状得分显著低于对照组(P≤0.05)。治疗组停药后的得分明显好于基线水平(P≤0.05)。对照组治疗结束后得分恢复到基线水平(25.91±13.53、25.03±10.16)(P>0.05)。对中途退出的患者进行结转,FAS集分析结果与PPS集分析结果一致,差异没有统计学意义(P>0.05)。详见表 5。
|
|
表 5 两组患者SDS评分情况 |
治疗组因ADR退出2例:1例于第6周因全身酸痛用药后不能有效缓解,抑郁评分58分,无法耐受,终止治疗,停药后症状逐渐好转;1例于11周血细胞下降药物不能恢复而停药。
对照组因ADR退出6例,退出时间分别在5周(2例)、13周(1例)、19周(1例)、20周(1例)、26周(1例):其中2例因疲乏、抑郁自觉不能耐受退出;4例因血细胞下降药物不能恢复而停药。完成了整个疗程的84例对照组患者中,有8例患者在治疗的6周、8周、13周、20周、24周、32周及治疗结束后,因疲劳、精神差不愿继续进行生存质量和抑郁量表的测评。两组均未发生违背治疗方案的病例。其他不良情况详见表 6。
|
|
表 6 其他不良情况 |
CHC的治疗策略是长期最大限度地抑制病毒复制,或通过增强机体免疫反应来提高清除病毒的能力。抗病毒治疗的目的是清除或持续抑制体内的HCV,以改善或减轻肝损害,阻止进展为肝硬化、肝衰竭或肝细胞癌,并提高患者的生活质量。目前,CHC主要采用PR方案治疗,研究表明虽然持续病毒学应答率(sustained virological response,SVR)比例升高,但由于治疗方案的局限性和严重的ADR,大大降低了患者治疗的依从性,治疗效果不理想[2-5]。
中医认为CHC“正虚邪恋”是疾病本质,“湿热疫毒”是发病外因。而干扰素治疗CHC从中医理论为祛邪之品,其用于人体不能独祛邪,必借激发人体正气以祛邪[11]。地芪固本口服液是多年临床验方研制的院内制剂,方中熟地、黄芪、党参补气养血为主,辅以女贞子、枸杞、制首乌、炙山萸肉补肝益肾,茯苓、山药益气健脾,白芍养血敛阴。当归养血活血,大枣益气养血,诸药合用共奏补血益气养阴,补肝益肾健脾之功,达到固本扶正的抗病能力。该药配合化疗治疗中晚期恶性肿瘤患者,在白细胞、血红蛋白、免疫球蛋白G、免疫球蛋白M、患者生活质量、WBC低于2.0×109而使用升白药次数、继发感染、延长化疗间隔方面,治疗组显著优于对照组,差异有统计学意义(P≤0.05)[6]。
本研究将地芪固本口服液联合PR方案治疗CHC,结果表明,地芪固本口服液能够有效减少和减轻PR方案引起的ADR。表现在:1)人均ADR发生例数、严重程度,治疗组均低于对照组(P≤0.05);2)不同类型ADR发生率,治疗组大多低于对照组,尤其在血细胞的减低、疲乏程度、抑郁评分等方面有明显的改善(P≤0.05),但四肢痛、转氨酶升高、腹泻、鼻塞或鼻窦充血方面,治疗组高于对照组(P>0.05)。国内研究也表明,中医药在CHC治疗中的不同方面发挥着减少ADR的作用[12-14]。
本项研究中,两组ADR发生率均高于一些同类研究,严重程度3级、4级的较少,尤其是4级(治疗组0.14%,对照组0.45%)远远低于同类研究[15-16]。究其原因:一方面可能与本次研究中,针对ADR制定了规范的ADR三级管理模式,收集到的ADR数据更加全面、及时、完整;另一方面目前关于ADR的严重程度分级国内外的标准有多种[8-9, 17-18],各研究所参考的标准不一致,计算方法也不同,造成各项研究的可比性较差。
抗病毒治疗过程中,治疗组和对照组抑郁等精神异常的发生率分别是7.37%、19.14%(P≤0.05)。两组患者在治疗初期精神状态逐渐变差,到第12~24周降至最差,24周以后逐渐改善,48周停药以后逐渐恢复至治疗前水平。但地芪固本口服液的使用,使得整个治疗过程中治疗组精神状态好于对照组,尤其是治疗12、24周明显好于对照组(P≤0.05),停药后12周、24周的状态好于治疗前(P≤0.05)。分析原因,可能与地芪固本口服液的使用减少和减轻了中性粒细胞等血细胞、贫血等ADR的发生,从而减轻了患者治疗过程中的疲劳引起的负性情绪,提高了患者生存质量有关。CHC患者在日常生活中需要面对各种压力、疾病本身带来的身体不适以及治疗过程中的ADR,因而抑郁等不良的精神疾病和状态普遍存在[19]。本项研究也再次印证了这一点,应引起临床更多的关注,并且积极进行中医药的治疗不失为一种行之有效的干预方法。
地芪固本口服液能有效干预CHC患者抗病毒治疗过程中ADR,特别表现在血细胞、疲劳等方面,张鑫[6]、郑彤[20]在肿瘤患者化疗过程中也有类似的发现。但这种影响的相关机理尚有待进一步研究,2015年《丙型肝炎防治指南》提出的直接抗病毒药物的使用,地芪固本口服液是否能够在其中继续发挥减毒增效的作用,也是我们需要今后探索研究的内容。
| [1] |
中华医学会肝病学分会. 中华医学会传染病与寄生虫病学分会丙型肝炎防治指南(2004)[J]. 中华肝脏病杂志, 2004, 12(4): 194-198. |
| [2] |
Ghany MG, Strader DB, Thomas DL, et al. Diagnosis, Management and Treatment of Hepatitis C:An Update[J]. Hepatology, 2009, 49(4): 1335-1374. DOI:10.1002/hep.22759 |
| [3] |
Asian Pacific Association for the Study of the Liver (APASL) Hepatitis C Working Party, Mc Caughan GW, Omata M, et al. Asian Pacific Association for the Study of the Liver Consensus Statements on the Diagnosis, Management and Treatment of Hep-atitis C Virus Infection[J]. J Gastroenterol Hepatol, 2007, 22(5): 615-633. DOI:10.1111/j.1440-1746.2007.04883.x |
| [4] |
European Association for the Study of the Liver. EASL Clinical Practice Guidelines:Management of Hepatitis C Virus Infection[J]. J Hepatol, 2011, 55(2): 245-264. DOI:10.1016/j.jhep.2011.02.023 |
| [5] |
慢性病毒性肝炎患者干扰素α治疗不良反应临床处理专家委员会. 慢性病毒性肝炎患者干扰素α治疗不良反应临床处理专家共识[J]. 中华实验和临床感染病杂志, 2014, 8(1): 108-113. |
| [6] |
张鑫, 金永新, 吴华, 等. 固本养血口服液临床疗效观察[J]. 甘肃医药, 2010, 29(4): 435-437. |
| [7] |
慢性丙型肝炎抗病毒治疗专家委员会. 慢性丙型病毒性肝炎抗病毒治疗专家共识2009[J]. 中华实验和临床感染病杂志, 2009, 3(3): 347-351. |
| [8] |
卫生部. 中华的人民共和共卫生部第81号药品不良反应监测报告和监测管理办法[S]. 2011.
|
| [9] |
美国卫生与公共服务部国立卫生研究院. 国家肿瘤研究所. 常见不良反应事件评价标准(4. 0版)[S]. 2009.
|
| [10] |
张明园. 精神科评定量表手册[M]. 长沙: 湖南科技出版社, 1993: 35-39.
|
| [11] |
蔡红荣. 孙玉信教授对干扰素治疗丙肝不良反应的辨证论治思路[J]. 明中医, 2011, 26(2): 216-218. |
| [12] |
孟胜喜, 赵文霞, 张照兰, 等. 健脾清化方对干扰素联合利巴韦林治疗慢性丙型肝炎疗效的影响[J]. 光明中医, 2010, 25(5): 834-837. |
| [13] |
常占杰, 李京涛. 益气养肝方联合干扰素和利巴韦林治疗慢性丙型肝炎的疗效观察[J]. 中国肝脏病杂志, 2009, 1(2): 24-27. |
| [14] |
王炳予, 袁星星, 张雅丽. 芪参二莲汤加聚乙二醇干扰素α-2a联合利巴韦林治疗1b型慢性丙型肝炎疗效观察[J]. 中西医结合肝病杂志, 2014, 24(4): 217-219. |
| [15] |
陈新月, 尚佳, 杨瑞锋, 等. 难治性慢性丙型肝炎初治患者优化治疗后的病毒学应答率研究[J]. 中华肝脏病杂志, 2015, 23(6): 412-417. |
| [16] |
李远勤, 刘全艳, 于毅, 等. 利巴韦林联合聚乙二醇干扰素α-2a治疗慢性丙型肝炎临床效果分析[J]. 中国医学前沿, 2016, 8(3): 89-92. |
| [17] |
皋文君, 刘砚燕, 袁长蓉, 等. 国际肿瘤化疗药物不良反应评级系统-通用不良反应术语标准(4.0版)[J]. 肿瘤, 2012, 32(2): 142-144. |
| [18] |
许佼, 龚建军, 王卓, 等. 药品不良反应损害程度评分标准的制定及应用[J]. 药学服务与研究, 2013, 13(2): 93-97. |
| [19] |
陈晓蓓, 杨丽华. 病毒性肝炎患者焦虑及抑郁症状的临床调查[J]. 中华医学杂志, 2002, 82(6): 398-399. |
| [20] |
郑彤, 要林青, 刘琳, 等. 化疗联合地芪固本合剂治疗非霍奇金淋巴瘤的疗效观察[J]. 中国中医药科技, 2015, 22(2): 193-194. |
 2018, Vol. 32
2018, Vol. 32