2. 大连市第二人民医院, 大连 116000
2. Dalian Second People's Hospital, Dalian 116000, China
香丹注射液(又称复方丹参注射液)是由丹参水提液和水蒸气蒸馏的降香饱和水溶液配制而成,具有扩张血管,增进冠状动脉血流量的作用,临床上用于心绞痛,亦可用于心肌梗塞等[1]。中药注射液因处方复杂并且临床应用日益广泛,引起的不良反应也陆续被发现,开展其安全性评价至关重要,由于含有溶血成分(皂苷)或物理、化学及生物等方面的原因,在直接注入血管后可产生溶血作用,另外,因中药制剂的成分复杂,也存在因免疫反应引起的免疫性溶血[2],因此,作为安全性检查的一项重要内容,需要对其溶血作用进行考察,保证用药安全。本试验采用常规体外试管法、分光光度法和氰化高铁血红蛋白法3种不同方法对该制剂的溶血作用进行考察,常规体外试管法为国家标准中溶血试验的常规方法,对于一些临界溶血具有主观判断性[3],而分光光度法和氰化高铁血红蛋白法通过测定数据比较客观地反映溶血现象。
1 仪器与材料 1.1 仪器和试剂美国BECKMAN COULTER Allegra X-30R型台式冷冻离心机;中仪国科(北京)科技有限公司DK-S26型电热恒温水浴锅;日本岛津公司UV-2550型紫外可见分光光度计,Molacular Devices Spectramax Paradigm型酶标仪;德国Sartorius公司BS4202S型电子天平;香丹注射液(批号:20140408、20140302、20140203,规格:5 mL·支-1);氯化钠注射液(批号:1312291307,规格:500 mL,吉林省都邦药业股份有限公司);EDTA·K2真空采血管(批号:120501,规格:5 mL,江苏康健医疗用品有限公司),其他试剂均为分析纯。
1.2 实验动物日本大耳白家兔,雄性,体重2.3 kg以上,由大连医科大学实验动物中心提供,合格证号:211003700000219。
2 方法与结果 2.1 兔血的制备 2.1.1 2%红细胞混悬液的制备取3只健康家兔心脏血液,混匀,分别放入含玻璃珠的锥形瓶中轻轻振摇10 min,以除去纤维蛋白原,使其成为脱纤血液。加入氯化钠注射液约10倍量,轻轻摇匀,然后离心,每分钟1500 rpm,离心15 min,除去上清液,沉淀的红细胞再用氯化钠注射液按上述方法洗涤2~3次,至上清液不显红色为止。将所得红细胞用氯化钠注射液制成2%的红细胞混悬液,即脱纤兔血[4]。
2.1.2 抗凝稀释兔血的制备取3只健康家兔心脏血液,混匀,分别加入EDTA·K2为抗凝剂的真空采血管中,制成新鲜抗凝兔血。取新鲜抗凝兔血8.0 mL,加氯化钠注射液10.0 mL,混匀,取10.0 mL,加氯化钠注射液80.0 mL,混匀,制成抗凝稀释兔血[5-6]。
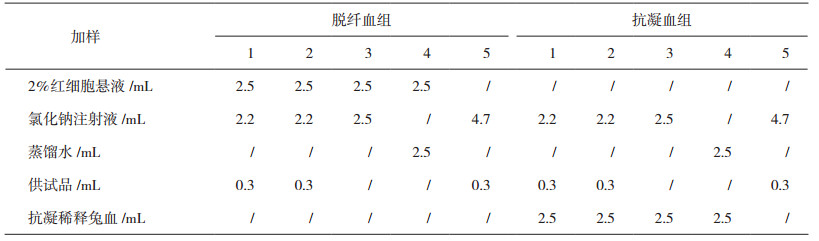
2.2 试验方法 2.2.1 常规体外试管法(肉眼观察法)取洁净玻璃试管5只,编号:1、2号管为供试品管,3号管为阴性对照管,4号管为阳性对照管,5号管为供试品对照管。按表 1所示加样,混匀后,立即置37℃水浴中,1、2、3 h观察溶血反应。如试管中的溶液呈澄明红色,管底无细胞残留或有少量红细胞残留,表明有溶血发生;如红细胞全部下沉,上清液无色澄明,或上清液虽有色澄明,但1、2号管和5号管肉眼观察无明显差异,则表明无溶血发生[4]。
|
|
表 1 溶血试验(肉眼观察法)加样表 |
按“2.2.1”节下制备溶液,供试品管每个时间点各3管,阴性对照、阳性对照和供试品对照各3管,取试管中溶液,然后离心,以每分钟1000 rpm,离心15 min,取上清液,分别在545 nm波长处测定吸光度(A),按下式计算溶血率。溶血率>5%表明有溶血发生[7]。
溶血率(%)=(A供试品-A阴性对照-A供试品对照)/(A阳性对照-A阴性对照)×100%
2.2.3 氰化高铁血红蛋白(HiCN)法取“2.2.2”节下各试管上清液各0.5 mL,分别加Drabkin试液[8](取铁氰化钾0.20 g,氰化钾0.05 g,碳酸氢钠1.00 g,加水溶解,并稀释至1000 mL)4.5 mL,混匀,室温放置15 min,以Drabkin试液为空白,在540 nm波长处测定吸光度。确定上清液中是否有血红蛋白的存在,按“2.2.2”节下公式计算溶血率。
2.3 结果 2.3.1 肉眼观察法结果1 h和2 h均未发生溶血,只有1批3 h时有溶血,且1、2号管和3、5号管肉眼观察有明显差异,说明有溶血发生,阴性对照管无溶血发生,阳性对照管有溶血发生。脱纤血组和抗凝血组结果基本一致。
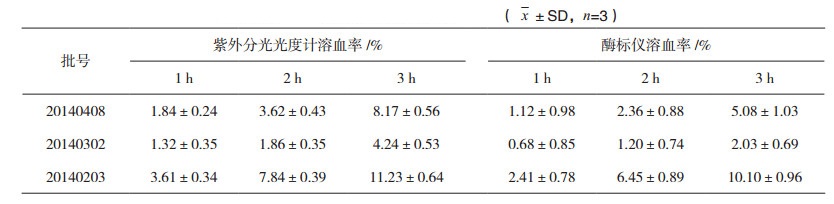
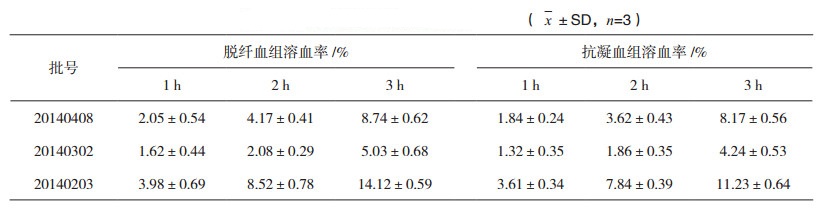
2.3.2 分光光度法结果3批供试品中2批溶血>5%,脱纤血组和抗凝血组结果基本一致,溶血率略有差别,结果见表 2。肉眼观察结果与分光光度法结果有差异。分别用两种不同仪器测定,结果见表 3。紫外分光光度计测定结果与酶标仪测定结果比较,溶血率有一定增加。
|
|
表 2 溶血试验(分光光度法)结果 |
|
|
表 3 不同仪器测定溶血结果的比较 |
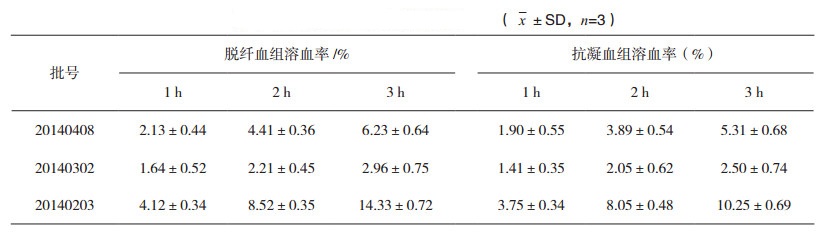
3批供试品中同样有2批溶血率>5%,结果见表 4。
|
|
表 4 溶血试验(Drabkin法)结果 |
1)采用玻璃珠制备脱纤红细胞混悬液后,用显微镜观察红细胞形态,发现红细胞部分破碎,造成阴性对照管吸光度较大(大于0.08),影响溶血率计算的准确性。而抗凝兔血中红细胞形态较完整。因此,脱纤血每次制备的阳性对照管吸光度差异均较大,不易重现,对实验人员要求高,对实验结果也会产生影响。用玻璃珠脱纤振摇可造成红细胞脆性增加,更易发生溶血,导致脱纤组比抗凝组溶血率偏大,对边缘数值结果影响大。因此,用抗凝兔血法代替脱纤兔血法,更容易保持细胞的完整性,更好地控制对照管的吸光度,且操作简便,结果更准确。
2)陈正爱等[9-11]曾采用肉眼观察法考察香丹注射液溶血作用,结论为不溶血;牛慧玲等[12]曾采用两种方法考察其溶血作用,浓度较高时部分溶血,均与本实验结果不尽相同,可从以下两方面分析两者结果的差异:一是香丹注射液为棕色的澄明液体,实验过程中供试品颜色较深会将红细胞变成棕色[13],掩盖溶血产生的红色,主观误差较大,直接影响肉眼观察结果,甚至导致结果难以判断,与扆雪涛[14]等认为增加阳性管可以排除干扰的结论不同;二是由于市场上香丹注射液的生产厂家约十余家,每个生产厂家产品颜色均有差异,且同一生产厂家不同批号间也存在较大差异。因此,肉眼观察法虽能直观地反映出溶血的基本情况,但不能作为准确判断产品是否溶血的方法[15]。
3)分光光度法是根据红细胞破裂释放出的血红素在可见光波长处具有最大吸收的原理,测定供试品的溶血程度,具有操作简便,稳定性好,消除主观误差等优点。酶标仪测得溶血率为10%的供试品结果与肉眼观察结果一致,有溶血现象。而溶血率大于5%的样品,肉眼观察并无溶血现象,将溶血率大于5%的溶液用紫外分光光度计测定,结果较酶标仪结果数值偏大,且多次测定结果较平行。酶标仪测定的优点是可同时测定多批供试品,达到快速筛选的目的,但结果偏差较大,紫外分光光度计测定结果更加准确可靠[16]。
4)HiCN法是目前血红蛋白各种测定法中最准确的方法,除Hbs、HbC外其他血红蛋白均可转化成HiCN,为国际血液学标准化委员会(ICSH)所推荐。其结果与分光光度法结果基本一致,但所用的试剂含有氰化钾,有剧毒;且HiCN法测定过程中吸光度值变化,要求测定时间准确,否则影响测定结果。可能由于中药成分复杂,含有酚类等具有氧化还原作用的组分,影响其专属性,对测定结果有一定的干扰。对于中药注射剂是否采用专属性更高的兔血红蛋白酶联免疫试剂盒确定血红蛋白溶出量,有待进一步研究。
5)本实验为使供试品具有代表性,选取经酶标法筛选的溶血率分别为2%、5%和10%的3批供试品,分别用3种方法进行测定,结果家兔抗凝血分光光度法更加准确。该方法可能也适用于多数中药注射剂的溶血性评价,为药物安全性检测提供参考。
| [1] |
卫生部药品标准中药成方制剂第十七册[S]. 1998: 200.
|
| [2] |
章宝娟. 中药注射剂溶血性试验方法的研究概述[J]. 海峡药学, 2007, 19(8): 79-81. |
| [3] |
朱勤, 许雷鸣. 复方麝香注射液体外溶血反应研究[J]. 安徽医药, 2013, 17(10): 1682-1673. |
| [4] |
中国药典: 一部[S]. 2010: 131-132.
|
| [5] |
国家食品药品监督管理局药包材检验方法标准汇编第三辑[S]. 2003: 10.
|
| [6] |
Foote R.H., Hare E.. Blood Catalase and Haematocrit Values in a Breeding Colony of Dutch-belted Rabbits[J]. Laboratory Animals Ltd, 2001, 35: 140-146. DOI:10.1258/0023677011911507 |
| [7] |
中药、天然药物刺激性和溶血性研究技术指导原则[S]. 2005: 22-25.
|
| [8] |
医療機器の生物学的安全性評価の基本的考え方薬食機発0301第20号[S]. 2012: 87.
|
| [9] |
陈正爱, 王丹, 李美子. 香丹注射液安全性实验报告[J]. 时珍国医国药, 2006, 17(2): 185-186. |
| [10] |
张德波, 蒲旭峰, 杨幼琪, 等. 中药注射剂溶血与凝聚试验方法研究[J]. 中药药理与临床, 2012, 28(1): 183-186. |
| [11] |
陈正爱, 王丹, 李美子. 香丹注射液安全性实验报告[J]. 时珍国医国药, 2006, 17(2): 185-186. |
| [12] |
牛慧玲, 李庆忠, 陈志勇, 等. 含吐温80的不同注射剂溶血试验研究[J]. 中国药品标准, 2012, 13(2): 108-111. |
| [13] |
徐黎玲. 分光光度法测定香丹注射液的溶血率[J]. 医药导报, 2004, 23(8): 585-586. |
| [14] |
扆雪涛, 李昇刚, 孙振平. 对23种中药注射剂溶血与凝聚检查的探讨[J]. 中国药品标准, 2010, 11(6): 430-432. |
| [15] |
陈志勇, 肖佳音, 李庆忠. 有色中药注射剂溶血试验的比较研究[J]. 黑龙江医药, 2015, 25(1): 32-34. |
| [16] |
柯正方. 中药注射剂溶血检查的两种方法比较[J]. 中国药品标准, 2011, 12(3): 216-219. |
 2018, Vol. 32
2018, Vol. 32