过敏性疾病已成为一种普遍的公共健康问题,据估计世界上有30%~40%的人口正遭受过敏性疾病的困扰;而且,过敏性疾病的发生率正逐年增加,造成了巨大的医疗负担[1-2]。过敏性疾病的影响因素包括产前接触微生物、分娩方式、饮食、药物使用以及接触宠物和家畜等,与人类现代生活方式有着直接的关系[3]。采用相关变应原疫苗进行脱敏治疗是治疗过敏性疾病的最佳手段,而对于尚未研制出疫苗的过敏症状,最主要的治疗方式是采用药物治疗来控制(即对症用药);但是,药物治疗并不能改变过敏性疾病的进程,因而也就不能从根本上达到治愈的效果。随着生物技术的发展和生物药物研究的深入,多项研究显示益生菌对过敏性疾病有一定的预防和治疗效果[4]。本文通过查阅近3年来关于益生菌预防和治疗过敏性疾病方面的文献,主要从动物实验、人体临床试验以及可能的治疗机制等方面进行了综述。
1 益生菌和过敏性疾病根据国际粮农组织和世界卫生组织的定义,益生菌是指“一类在宿主摄入适当数量时,能对其机体带来益处的活的微生物[5]。”大多数益生菌是人类健康肠道菌群的成员,传统的发酵乳制品和相关产品也是其重要来源,例如双歧杆菌属和乳酸杆菌属等[6]。益生菌或肠道菌群如今已经成为全球研究的热点。肠道菌群在早期研究中更多被认为和消化、营养作用有关,新的研究发现肠道菌群与人类的健康有着多种多样的复杂联系:肠道菌群与肥胖、糖尿病、艾滋病、心血管疾病、肿瘤,以及本文中讲到的过敏性疾病与免疫等等都存在着关系,甚至肠道菌群与自闭症、抑郁症、帕金森及老年痴呆等精神性疾病有关[7-10]。益生菌作为肠道菌群的重要组成部分,对人类健康发挥着越来越重要的作用。
过敏反应又称超敏反应,根据其发生机制和临床特点可分为四型。益生菌治疗过敏性疾病研究中所指的过敏反应属于Ⅰ型超敏反应,主要是由IgE介导的疾病,如过敏性鼻炎、过敏性哮喘、特应性皮炎(AD)等等[11]。过敏性疾病发生率呈逐年上升趋势,引起过敏反应的过敏原也多种多样,主要包括花粉、霉菌、螨虫、动物皮屑、昆虫毒液,以及食物等[12]。
2 益生菌在过敏性疾病的预防和治疗中应用的研究进展 2.1 益生菌在实验动物中预防和治疗过敏性疾病的研究近年来,研究人员利用动物模型对益生菌预防和治疗过敏疾病进行了多项研究,为临床研究提供了依据。Ondulla T. Toomer等[13]报道用混合有嗜酸乳杆菌(L. acidophilus)、干酪乳杆菌(Lactobacillus casei)、双裂双岐杆菌(Bifido bacterium bifidium)和粪肠球菌(Enterococcus faecium)的食物喂养卵清蛋白(OVA)致敏的新生小鼠(0~10周),能诱导调节性T细胞数量的增加,增强转化生长因子β(TGF-β)基因表达并减少过敏介质IL-13等的表达。EMM Velez等[14]使用含有保加利亚乳杆菌(Lactobacillus bulgaricus,108 CFU·mL-1)、嗜热链球菌(Streptococcus thermophilus,108 CFU·mL-1)和副干酪乳杆菌亚种CNCMI-1518的益生菌发酵乳(PFM)喂饲5周龄的BALB/c小鼠,使用OVA对小鼠致敏,发现小鼠抗OVA特异性IgE水平显著降低,而抗OVA特异性IgG和总分泌型IgA(S-IgA)没有发生变化。PFM能调节Th2反应向Th1反应转变,增加IL-10和IFN-γ水平。Hana Kozakova等[15]将含有鼠李糖乳杆菌LOCK0900(L. rhamnosus LOCK0900)、鼠李糖乳杆菌LOCK090833和干酪乳杆菌LOCK0919的混合益生菌(Lmix)定植于近交系BALB/c小鼠(8周龄),3周之后用重组桦树花粉致敏原蛋白Bet v1致敏小鼠,最终结果显示Lmix定植能提高肠道上皮的屏障作用并降低对Bet v1的敏感性;血清中抗原特异性IgE、IgG1和IgG2a水平明显降低,同时却提高了血清中总IgA水平和TGF-β水平。Bo Yang等[16]通过OVA敏感小鼠模型研究发现益生菌能够降低血清中OVA-IgE和OVA-IgG1水平,降低脾脏Th2细胞因子的释放并改善腹泻症状;而且通过16S rRNA分析发现起主要作用的益生菌是粪球菌属和立克菌属。
很多研究人员对单一种属益生菌以及益生菌某些成分的效果也进行了研究。Chia-Ta Wu等[17]用鼠李糖乳杆菌GG(LGG)对OVA致敏的哮喘小鼠模型过敏症状进行预防和治疗试验,发现LGG能显著减少支气管肺泡灌洗液与血清中炎症浸润细胞和Th2细胞因子数量;并减少血清中特异性OVA-IgE水平以及肺部基质金属蛋白酶9(MMP-9)的表达等。Vamshi Saliganti等[18]利用瑞士白化小鼠(Swiss albino mice)研究鼠李糖乳杆菌MTCC 5897对OVA所诱发小鼠过敏症的预防和治疗效果,发现MTCC 5897能减轻新生小鼠过敏症状,增加杯状细胞(goblet)和小肠中IgA+细胞数量;同时显著减少血清中特异性抗OVA抗体(IgE、IgG、IgG1)数量以及IgE/IgG2a和IgG1/IgG2a的比值;促进IL-4水平的降低和TGF-β水平的增加。Jing Yang等[19]利用副干酪乳杆菌L9和BALB/c雌性小鼠(3周龄)研究L9对小鼠牛β-乳球蛋白(Bovine β-Lactoglobulin,BLG)过敏的预防作用,研究发现L9能上调CD4+CD25+Foxp3+Treg细胞反应,从而平衡Th1/Th2反应,CD4+CD25+Foxp3+Treg细胞数量在肠系膜淋巴结中上升了51.85%;另外,L9在肠系膜淋巴结、派尔集合淋巴结和脾脏中能显著地诱导CD103的表达并减少成熟DC细胞的数量。Hangeun Kim等[20]将植物乳杆菌K8(L. plantarum K8,KCTC 10887BP)培养后超声波破碎,制成裂解物冻干粉,利用NC/Nga小鼠(6周龄)进行AD的预防研究,结果显示口服植物乳杆菌裂解物能有效抑制NC/Nga小鼠皮肤角质层和表皮增厚,口服8周后皮肤屏障功能损害明显减少;进一步研究证明该裂解物能通过诱导IL-12和IFN-γ的产生,同时抑制IL-4和IgE来促使免疫反应向Th1发展。ChungHsiung Huang等[21]用罗伊乳杆菌饲养OVA过敏小鼠模型,发现罗伊乳杆菌能通过调节肠道菌群和增强肠道免疫耐受来抵抗肠道食物过敏,并由此认为罗伊乳杆菌是一种有效的对抗食物过敏的益生菌。
上述研究表明,无论混合益生菌、单一益生菌,还是益生菌的某些成分,在动物实验中对过敏性疾病有一定的预防和治疗作用。动物实验初步证明了益生菌对过敏性疾病的预防和治疗效果,为益生菌的临床应用提供了重要依据。
2.2 益生菌在临床试验中预防和治疗过敏性疾病的研究益生菌虽然在动物模型中证明是有效的,但人类和动物在生活环境和饮食习惯上存在着重大差异,益生菌是否对人有效还需要得到临床应用的证实。
Melanie Rae Simpson等[22]采用随机双盲对照平行试验,让415名孕妇在36孕周时开始随机服用含有益生菌鼠李糖杆菌GG、嗜酸乳杆菌La-5和动物双歧杆菌乳酸亚种Bb-12(Bifidobacterium animalis subsp. lactis Bb-12)的牛乳或安慰剂直到产后3个月,6年后对他们的孩子进行过敏疾病发病情况的评估,发现孕产妇单独摄入益生菌足以长时间地减少AD累计发病率,而对其他诸如哮喘和过敏性鼻炎等过敏性疾病没有显著的效果。I-Jen Wang等[23]采用双盲、前瞻性、随机、安慰剂对照的方法,研究副干酪乳杆菌(LP)、发酵乳杆菌(LF)以及混合菌对AD严重程度、生活质量和儿童免疫标志物的影响。结果表明LP+LF混和益生菌能够减轻AD的严重性,并能够提高患儿的生活质量,LP+LF混和益生菌效果优于单一的LP或LF益生菌。Michele Miraglia Del Giudice等[24]临床试验发现,双歧杆菌合剂(长双歧杆菌BB536、婴儿双岐杆菌M-63和短双歧杆菌M-16V)能够显著改善花粉过敏性鼻炎和间歇性哮喘儿童的过敏症状,并大大提高他们的生活质量。
对单一益生菌在临床上的研究也取得了一些进展。D J Costa等[25]在花粉过敏性鼻炎患者中就益生菌副干酪乳杆菌亚种LP-33对过敏性鼻炎治疗的有效性和安全性进行评估,研究期间患者同时接受氯雷他定和H1抗组胺药治疗。结果显示LP-33能显著改善患者生活质量,鼻炎患者眼部症状持续改善,但鼻部症状没有显著变化。Niccoli Antonio A等[26]招募了43名0~11周岁的AD患者(男/女=1:1),每天服用2袋(1×109 CFU/袋)唾液乳杆菌(L. salivarius)LS01(DSM 22775),连续8周后,改为每天服用1袋,再连续服用8周。在此期间检测瘙痒指数(itch index)和SCORAD/SCORAD指数,结果显示服用LS01能够改善AD儿童的生活质量。Cinzia Lucia Randazzo等[27]采用随机双盲对照的方法研究了罗伊氏乳杆菌(Lactobacillus reuteri)DSM 17938对系统性镍过敏综合征(SNAS)的治疗效果,初步结果显示,DSM 17938可能是SNAS病人低镍饮食中的有益补充,它能通过调节胃肠道的稳态环境来增加胃肠道益生菌种群多样性。Mimi L. Tang等[28]采用随机双盲对照的方法,将益生菌(Lactobacillus rhamnosus CGMCC 1.3724)与花生口服免疫治疗联合起来(PPOIT)进行儿童花生过敏的研究,研究显示PPOIT疗法能使患儿过敏反应持续无应答,在皮肤点刺试验中能使机体对花生抗原不敏感,能降低花生特异性IgE水平,同时增加花生特异性IgG4水平。
还有研究者从基因方面进行了研究。Angharad R. Morgan等[29]同样采用双盲随机对照试验的方法,研究鼠李糖乳杆菌HN001和动物双歧杆菌乳酸亚种HN019是否能影响湿疹易感基因的表达,结果显示服用HN001之后,携带湿疹基因变异体的儿童虽然处于湿疹高风险环境中也很少患上湿疹;HN019也能够防止一些单核苷酸多态性基因(SNPs)的影响,HN001还能修改严重性湿疹和过敏症风险易感基因的易感性。Anna Forsberg等[30]也采用双盲随机对照试验的方法,研究罗伊乳杆菌ATCC 55730对TLR(Toll like receptor)的识别应答影响,研究发现ATCC 55730在儿童12个月龄时能降低LTA(lipoteichoic acid)诱导CCL4、CXCL8、IL-1β和IL-6产生的反应,并能在24月龄时减少CCL4和IL-1β的分泌,TLR2 mRNA的表达不受益生菌的影响,但益生菌的作用似乎与TLR mRNA下游因素的表达有关。
同时,也有一些研究结果显示益生菌对过敏性疾病没有效果。Evelyn X. Loo等[31]进行了一项长达5年的随访研究,试图证明在生命早期给予益生菌是否能长期预防治疗过敏性疾病,结果发现,在儿童五周岁时,罹患哮喘、过敏性鼻炎、湿疹、食物过敏和吸入性过敏原过敏疾病的概率与对照组没有什么不同。Hyeon-Jong Yang等[32]采用双盲随机对照的方法,研究混合益生菌(干酪乳杆菌、鼠李糖乳杆菌、植物乳杆菌、双歧杆菌乳酸菌等)对儿童(2~9岁)中重度AD的治疗效果,发现益生菌能在6周后成功定植于胃肠道,然而并没有发现益生菌对AD有治疗和调节的效果。Chiara Nembrini等[33]同样通过双盲随机对照临床试验研究副干酪乳杆菌NCC 2461在花粉过敏性鼻炎患者中的抗过敏效应,发现与之前的研究结果相反,口服NCC 2461并没有展现出对过敏性鼻炎具有有益的效果。
临床试验显示,益生菌对过敏性鼻炎、AD、哮喘和食物过敏等疾病具有一定的治疗效果;对过敏性疾病有效的益生菌一般为鼠李糖杆菌、嗜酸乳杆菌、双歧杆菌等;益生菌单一菌种和混合益生菌都能起到治疗的作用。但也不能忽视,有些试验得出了相反的结论,益生菌对过敏性疾病的治疗研究还不够深入,其间的许多关系还需要进一步的研究。
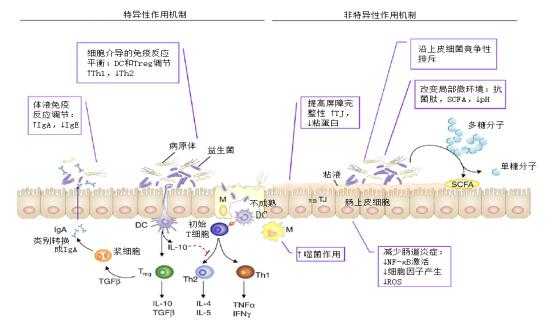
3 益生菌预防治疗过敏性疾病的可能机制关于益生菌预防治疗过敏性疾病的机制目前尚不完全清楚,也没有公认的定论,根据一些动物实验的研究结果,大致可以总结出以下几种可能的机制:①益生菌通过调节胃肠道环境,使胃肠道达到稳态平衡。②益生菌通过诱导免疫细胞释放细胞因子,改变Thl/Th2平衡, 从而促进Th1型免疫反应,抑制Th2型免疫反应。③通过增强调节性T细胞的优势,调节免疫反应。④减少过敏介质IL-13、IgE、IL-4、IgG1和IgG2a等的表达,同时增加IgA、IL-10、IFN-γ、TGF-β等的表达。⑤通过改变过敏原受体(TLR)的敏感性, 缓解过敏症症状。⑥在基因水平上改变mRNA的表达量,增强过敏耐受性等等。这些机制还有待进一步的研究和验证。益生菌预防治疗过敏性疾病机制见图 1[34]。
|
图 1 益生菌预防治疗过敏性疾病机制示意图 注:1. DC:树突状细胞;2. TJ:紧密接头;3. SCFA:短链脂肪酸;4. IgA:免疫球蛋白A;5. IgE:免疫球蛋白E;6. IL:白细胞介素;7. TNF:肿瘤坏子因子;8.干扰素:NF-kB;9.核因子:kB;10. ROS:活性氧。 |
益生菌对人类健康有多种促进作用,尤其是益生菌对过敏性疾病的预防和治疗作用越来越受到人们的重视。从以上文献的调研结果可以看出,益生菌对免疫疾病的预防和治疗起到有益的作用。但是也存在着诸多问题:虽然多数研究显示益生菌有效,但也有一部分试验结果显示其无效,研究结果存在不一致性和不稳定性;益生菌种类繁多,过敏性疾病也多种多样,益生菌与特定过敏性疾病之间的联系还不是很清楚,以及人群的差异化也是导致研究结果不一致的原因之一;益生菌对过敏性疾病的作用机制尚不清楚,因而治疗效果评价方法也多样化,增加了治疗效果评价难度。因此,在今后的研究中,使用特定有效的益生菌株,采用统一的方法和标准,更能推进对益生菌在过敏性疾病预防和治疗作用的理解。
| [1] |
Neau E, Delannoy J, Marion C, et al. Identification of Three Novel Candidate Probiotic Strains with Prophylactic Properties in a Murine Model of Cow's Milk Allergy[J]. Applied and Environmental Microbiology, 2016, 82(6): 1722-1733. DOI:10.1128/AEM.03440-15 |
| [2] |
Gern J E. Promising Candidates for Allergy Prevention[J]. The Journal of Allergy and Clinical Immunology, 2015, 136(1): 23-28. DOI:10.1016/j.jaci.2015.05.017 |
| [3] |
Żukiewicz-Sobczak W, Wróblewska P, Adamczuk P, et al. Probiotic Lactic Acid Bacteria and Their Potential in the Prevention and Treatment of Allergic Diseases[J]. 2014, 39(1): 104-108. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4439985/
|
| [4] |
Van Bever H P, Nagarajan S, Shek L, et al. OPINION:Primary Prevention of Allergy:Will it Soon become a Reality?[J]. Pediatric Allergy & Immunology Official Publication of the European Society of Pediatric Allergy & Immunology, 2016, 27(1): 6-12. |
| [5] |
Araya M., Morelli L., Reid G., et al. Guidelines for the Evaluation of Probiotics in Food[J]. AIP Conference Proceedings, 2002, 61(1): 243-247. |
| [6] |
Kumar H, Salminen S. Probiotics[J]. Encyclopedia of Food & Health, 2016, 75: 510-515. |
| [7] |
Bhattacharjee S, Lukiw WJ. Alzheimer's Disease and the Microbiome[J]. Frontiers in Cellular Neuroscience, 2013, 7(153): 1-4. |
| [8] |
Bested AC, Logan AC, Selhub EM. Intestinal Microbiota, Probiotics and Mental Health:from Metchnikoff to Modern Advances:Part Ⅱ-contemporary Contextual Research[J]. Gut Pathogens, 2013, 5(3): 1-14. |
| [9] |
Schmidt C. Mental Health:Thinking from the Gut[J]. Nature, 2015, 518(7540): 12-15. DOI:10.1038/518S13a |
| [10] |
Hsiao E, Mcbride S, Hsien S, et al. Microbiota Modulate Behavioral and Physiological Abnormalities Associated with Neurodevelopmental Disorders[J]. Cell, 2013, 155(7): 1451-1463. DOI:10.1016/j.cell.2013.11.024 |
| [11] |
Kay A B. Allergy and Allergic Diseases. First of Two Parts[J]. New England Journal of Medicine, 2001, 344(1): 30-37. DOI:10.1056/NEJM200101043440106 |
| [12] |
European Phamacopoeia Commission. European Pharmacopoeia 9. 0[S]. Allergen Products(1063), 2017: 810-812.
|
| [13] |
Toomer O T, Ferguson M, Pereira M, et al. Maternal and Postnatal Dietary Probiotic Supplementation Enhances Splenic Regulatory T Helper Cell Population and Reduces Ovalbumin Allergen-induced Hypersensitivity Responses in Mice[J]. Immunobiology, 2014, 219(5): 367-376. DOI:10.1016/j.imbio.2014.01.003 |
| [14] |
Velez E M, Maldonado Galdeano C, Carmuega E, et al. Probiotic Fermented Milk Consumption Modulates the Allergic Process Induced by Ovoalbumin in Mice[J]. The British Journal of Nutrition, 2015, 114(4): 566-576. DOI:10.1017/S0007114515001981 |
| [15] |
Kozakova H, Schwarzer M, Tuckova L, et al. Colonization of Germ-free Mice with a Mixture of Three Lactobacillus Strains Enhances the Integrity of Gut Mucosa and Ameliorates Allergic Sensitization[J]. Cellular & Molecular Immunology, 2016, 13(2): 251-262. |
| [16] |
Yang B, Xiao L, Liu S, et al. Exploration of the Effect of Probiotics Supplementation on Intestinal Microbiota of Food Allergic Mice[J]. Am J Transl Res, 2017, 9(2): 376-385. |
| [17] |
Wu C, Chen P, Lee Y, et al. Effects of Immunomodulatory Supplementation with Lactobacillus Rhamnosus on Airway Inflammation in a Mouse Asthma Model[J]. Journal of Microbiology Immunology and Infection, 2016, 49(5): 625-635. DOI:10.1016/j.jmii.2014.08.001 |
| [18] |
Saliganti V, Kapila R, Sharma R, et al. Feeding Probiotic Lactobacillus Rhamnosus(MTCC 5897) Fermented Milk to Suckling Mothers Alleviates Ovalbumininduced Allergic Sensitisation in Mice Offspring[J]. The British Journal of Nutrition, 2015, 114(8): 1168-1179. DOI:10.1017/S000711451500286X |
| [19] |
Yang J, Ren F, Zhang H, et al. Induction of Regulatory Dendritic Cells by Lactobacillus Paracasei L9 Prevents Allergic Sensitization to Bovine beta-Lactoglobulin in Mice[J]. Journal of Microbiology and Biotechnology, 2015, 25(10): 1687-1696. DOI:10.4014/jmb.1503.03022 |
| [20] |
Kim H, Kim H R, Kim N R, et al. Oral Administration of Lactobacillus Plantarum Lysates Attenuates the Development of Atopic Dermatitis Lesions in Mouse Models[J]. Journal of Microbiology, 2015, 53(1): 47-52. DOI:10.1007/s12275-015-4483-z |
| [21] |
Huang C H, Lin Y C, Jan T R. Lactobacillus Reuteri, Induces Intestinal Immune Tolerance Against Food Allergy in Mice[J]. Journal of Functional Foods, 2017(31): 44-51. |
| [22] |
Simpson M R, Dotterud C K, Storro O, et al. Perinatal Probiotic Supplementation in the Prevention of Allergy Related Disease:6 Year follow up of a Randomised Controlled Trial[J]. BMC Dermatology, 2015, 15(1): 1-8. DOI:10.1186/s12895-015-0023-0 |
| [23] |
Wang I J, Wang J Y. Children with Atopic Dermatitis Show Clinical Improvement after Lactobacillus Exposure[J]. Clinical and Experimental Allergy:Journal of the British Society for Allergy and Clinical Immunology, 2015, 45(4): 779-787. DOI:10.1111/cea.2015.45.issue-4 |
| [24] |
Giudice M M D, Indolfi C, Capasso M, et al. Bifidobacteriummixture(B longumbb536, B infantism-63, B brevem-16V)Treatment in Children with Seasonal Allergic Rhinitis and Intermittent Asthma:[J]. Italian Journal of Pediatrics, 2017, 43(1): 25-30. DOI:10.1186/s13052-017-0340-5 |
| [25] |
Costa D J, Marteau P, Amouyal M, et al. Efficacy and Safety of the Probiotic Lactobacillus Paracasei LP-33 in Allergic Rhinitis:a Double-blind, Randomized, Placebo-controlled Trial(GA2LEN Study)[J]. European Journal of Clinical Nutrition, 2014, 68(5): 602-607. DOI:10.1038/ejcn.2014.13 |
| [26] |
Niccoli A A, Artesi A L, Candio F, et al. Preliminary Results on Clinical Effects of Probiotic Lactobacillus Salivarius LS01 in Children Affected by Atopic Dermatitis[J]. Journal of Clinical Gastroenterology, 2014(48): 34-36. |
| [27] |
Randazzo C L, Pino A, Ricciardi L, et al. Probiotic Supplementation in Systemic Nickel Allergy Syndrome Patients:Study of its Effects on Lactic Acid Bacteria Population and on Clinical Symptoms[J]. Journal of Applied Microbiology, 2015, 118(1): 202-211. DOI:10.1111/jam.2015.118.issue-1 |
| [28] |
Tang M L, Ponsonby A L, Orsini F, et al. Administration of a Probiotic with Peanut Oral Immunotherapy:A Randomized Trial[J]. The Journal of Allergy and Clinical Immunology, 2015, 135(3): 737-744. DOI:10.1016/j.jaci.2014.11.034 |
| [29] |
Morgan A R, Han D Y, Wickens K, et al. Differential Modification of Genetic Susceptibility to Childhood Eczema by Two Probiotics[J]. Clinical and Experimental Allergy:Journal of the British Society for Allergy and Clinical Immunology, 2014, 44(10): 1255-1265. DOI:10.1111/cea.2014.44.issue-10 |
| [30] |
Forsberg A, Abrahamsson T R, Bjorksten B, et al. Preand Postnatal Administration of Lactobacillus Reuteri Decreases TLR2 Responses in Infants[J]. Clinical and Translational Allergy, 2014, 4(1): 1-7. DOI:10.1186/2045-7022-4-1 |
| [31] |
Loo E X, Llanora G V, Lu Q, et al. Supplementation with Probiotics in the First 6 Months of Life did not Protect Against Eczema and Allergy in at-risk Asian Infants:A 5-year follow-up[J]. International Archives of Allergy and Immunology, 2014, 163(1): 25-28. DOI:10.1159/000356338 |
| [32] |
Yang H J, Min T K, Lee H W, et al. Efficacy of Probiotic Therapy on Atopic Dermatitis in Children:A Randomized, Double-blind, Placebo-controlled Trial[J]. Allergy, Asthma & Immunology Research, 2014, 6(3): 208-215. |
| [33] |
Nembrini C, Singh A, De Castro C A, et al. Oral Administration of Lactobacillus Paracasei NCC 2461 for the Modulation of Grass Pollen Allergic Rhinitis:A Randomized, Placebo-controlled Study during the Pollen Season[J]. Clinical and Translational Allergy, 2015, 5(1): 1-6. DOI:10.1186/s13601-015-0045-z |
| [34] |
Iacono A, Raso G M, Canani R B, et al. Probiotics as an Emerging Therapeutic Strategy to Treat NAFLD:Focus on Molecular and Biochemical Mechanisms[J]. Journal of Nutritional Biochemistry, 2011, 22(8): 699-711. DOI:10.1016/j.jnutbio.2010.10.002 |
 2018, Vol. 32
2018, Vol. 32 
