2. 淄博市食品药品检验研究院, 淄博 255000
2. Zibo Institute for Food and Drug Control, Zibo 255000, China
药物制剂“逆向工程”是一种药品制备再现过程,即对某一目标药物制剂进行逆向分析研究,从而演绎出该制剂的定性处方、原料药晶型乃至粒度、辅料含量与规格、制剂工艺等要素,以制备出质量和疗效与目标药物制剂一致的产品为目标导向的关键技术。“逆向工程”属于仿制药处方前研究,它能够有效降低仿制药开发的难度、缩短研发时间、提高人体生物等效性试验的成功率,为我国正在开展的口服固体制剂仿制药质量与疗效一致性评价工作开辟了一条新的研究思路。
淀粉、玉米淀粉、预胶化淀粉是口服固体制剂中最常用的粘合剂、崩解剂或填充剂,其不同用法、用量对口服制剂的体外溶出行为影响巨大,剖析其准确用量,不仅可以减少研发时间、提高研发的效率,而且能够使仿制药与目标药物在药剂结构和组成上更接近,确保仿制药体内疗效的一致。目前关于淀粉含量测定方法的报道,大多应用在粮食、植物提取物或食品中的直链淀粉、侧链淀粉或总淀粉的测定[1-3]上,未见口服固体制剂中淀粉含量测定方法报道。对现有的上述淀粉含量测定方法进行分析和测试,发现现有方法受口服固体制剂中的原料药和其他辅料的干扰大,导致方法准确度很低,因此不能直接套用,必须开发新的检测方法,排除原料药和辅料的各种干扰,更快速、准确地测定淀粉类辅料的含量。
1 仪器与试药十万分之一电子天平(Quintix65-1cn,赛多利斯)、万分之一天平(BSA224S-CW,赛多利斯)、紫外-可见分光光度计(Evolution,热电)、离心机(Mirco17,热电)、涡旋振荡器(QT-2A、上海琪特)、数显恒温水浴锅(HH-8,常州智博瑞)。
玉米淀粉(厂家:法国Roquette;批号:S7110)和预胶化淀粉(厂家:上海卡乐康;批号:IN532487)为药用辅料;碘(厂家:天津市北联精细化学品开发有限公司;批号:20170210)、碘化钾(厂家:上海化学试剂有限公司;批号:0012102)、盐酸(厂家:莱阳经济技术开发有限公司;批号:20160810)、氢氧化钠(厂家:烟台市双双化工有限公司;批号:20160106)、乙醇(厂家:烟台市双双化工有限公司;批号:20160801)均为分析纯;盐酸小檗碱片(厂家:日本大峰堂薬品工業株式会社;批号:01MF)、格列吡嗪片(厂家:美国辉瑞;批号:R93091)、卡马西平片(厂家:美国诺华;批号:P0357)、盐酸雷尼替丁胶囊(厂家:美国Sandoz;批号:FV9602-1)、茶碱缓释片(厂家:日本卫材;批号:68A42P)、对乙酰氨基酚片(厂家:GSK;批号:5150090),口服固体制剂均为市售产品。
2 含量测定方法 2.1 测定方法的选择淀粉的含量测定方法大致分为三类:第一类为近红外、红外、旋光法[4-6]等方法,这类方法受口服固体制剂中原辅料干扰,无法准确定量。第二类为淀粉用酸和淀粉酶水解成单糖或葡萄糖醛[7-8],然后测定。这类方法操作繁琐,淀粉不易水解完全,口服固体制剂中的微晶纤维素也能水解成单糖或葡萄糖醛,从而干扰结果,使数据不准确。第三类为碘显色法[9-10],其原理是淀粉遇I2生成包合物,发生显色反应,反应的灵敏度很高,是较为常用的方法,但易受原辅料干扰。本文选择碘显色法,重点研究各种原辅料干扰测定的机理和如何排除其干扰,并参考文献对所建方法进行了验证[11-12],所建立的测定方法原理及操作步骤见图 1。

|
图 1 淀粉测定原理及操作步骤 |
方法A:精密称取口服固体制剂粉末适量(约含淀粉50 mg),置离心管中,加无水乙醇2~10 mL涡旋混匀,高速离心后倾去上清液,重复操作3~5次。沉淀物用1 mol·L-1氢氧化钠溶液4.0 mL转移置10 mL试管中,水浴糊化完全后转移置100 mL量瓶中,用水定容至刻度,摇匀。精密量取5 mL置50 mL量瓶中,并加0.25 mol·L-1盐酸溶液1.0 mL,用水定容至刻度,摇匀,过滤,取续滤液10 mL加碘溶液0.1 mL混匀,作为供试品溶液。按照紫外-可见分光光度法(《中国药典》2015年版四部附录0401紫外-可见分光光度法),在550~650 nm波长处测定吸光度。
方法B:精密称取口服固体制剂粉末适量(约含淀粉50 mg),置三角瓶中,加丙酮或甲醇或混合有机试剂10~50 mL,涡旋震荡,用0.45μm滤膜过滤,沉淀物用上述溶剂洗涤2~3次,每次10~ 50 mL。沉淀物用1 mol·L-1氢氧化钠溶液4.0 mL转移置10 mL试管中,水浴糊化完全后转移置100 mL量瓶中,用水定容至刻度,摇匀。精密量取5 mL置50 mL量瓶中,并加0.25 mol·L-1盐酸溶液1.0 mL,用水定容至刻度,摇匀,过滤,取续滤液10 mL加碘溶液0.1 mL混匀,作为供试品溶液。按照紫外-可见分光光度法(《中国药典》2015年版四部附录0401紫外-可见分光光度法),在550~650 nm波长处测定吸光度。
3 干扰因素分析口服固体制剂处方中的原料药和其他辅料是测定的主要干扰物质。盐酸小檗碱片、格列吡嗪片、卡马西平片、盐酸雷尼替丁胶囊、茶碱缓释片、对乙酰氨基酚片中的主要干扰物质汇总见表 1,分析这些干扰物质影响含量测定的主要机制如下:
|
|
表 1 6种口服固体制剂中淀粉含量测定的干扰物质汇总 |
干扰A:原辅料本身有颜色,在测定波长处有吸收。
干扰B:原辅料与碘液发生反应显色,在测定波长处有吸收。
干扰C:原辅料与碘液反应生产絮状沉淀干扰测定。
干扰D:原辅料消耗碘液,导致回收率低,甚至显色反应失败。
干扰E:糊化过程溶解的原辅料,在降温过程中与淀粉发生共沉淀。
干扰F:显色环境、特殊辅料等影响试验过程。
4 方法学验证 4.1 干扰试验(以方法A为例)空白辅料混合物:以上市口服固体制剂说明书定性处方为依据,根据原料药处方量和各辅料常用量(除待测成分外),称取原辅料混合均匀。
碘溶液:称取碘1.30 g、碘化钾3.60 g置于烧杯中,用水适量溶解后,加水至100 mL,摇匀。
对照储备溶液:精密称取淀粉50 mg,置10 mL试管中,加入1 mol·L-1氢氧化钠溶液4.0 mL,水浴糊化完全后转移置100 mL量瓶中,用水定容至刻度,摇匀,作为对照储备液。
对照溶液:精密量取对照储备溶液5 mL置50 mL量瓶中,并加0.25 mol·L-1盐酸溶液1.0 mL,用水定容至刻度,摇匀,过滤,取续滤液10 mL加碘溶液0.1 mL混匀,作为对照溶液。
空白辅料溶液:精密称取空白辅料混合物适量(约含淀粉50 mg),置离心管中,加无水乙醇2~10 mL涡旋混匀,高速离心后倾去上清液,重复操作3~5次。沉淀物用1 mol·L-1氢氧化钠溶液4.0 mL转移置10 mL试管中,水浴糊化完全后转移置100 mL量瓶中,用水定容至刻度,摇匀。精密量取5 mL置50 mL量瓶中,并加0.25 mol·L-1盐酸溶液1.0 mL,用水定容至刻度,摇匀,过滤,取续滤液10 mL加碘溶液0.1 mL混匀,作为空白辅料溶液。
供试品溶液:精密称取空白辅料混合物适量(约含淀粉50 mg)和淀粉50 mg,置离心管中,加无水乙醇2~10 mL涡旋混匀,高速离心后倾去上清液,重复操作3~5次。沉淀物用1 mol·L-1氢氧化钠溶液4.0 mL转移置10 mL试管中,水浴糊化完全后转移置100 mL量瓶中,用水定容至刻度,摇匀。精密量取5 mL置50 mL量瓶中,并加0.25 mol·L-1盐酸溶液1.0 mL,用水定容至刻度,摇匀,过滤,取续滤液10 mL加碘溶液0.1 mL混匀,作为供试品溶液。
测定法:取对照溶液、空白辅料溶液和供试品溶液,按照紫外-可见分光光度法(《中国药典》2015年版四部附录0401紫外-可见分光光度法),在575 nm波长处测定吸光度。
要求:空白辅料溶液在测定波长处的吸光度值小于0.01(需要将干扰物质完全除去),供试品溶液与对照溶液的吸光度比值在80%~110%。
4.2 线性范围考察精密称取淀粉50.76 mg,置10 mL试管中,加1 mol·L-1氢氧化钠溶液4.0 mL,置水浴锅中煮沸糊化完全,用水转移置100 mL量瓶中,加水定容至刻度,摇匀,作为淀粉储备液。
分别精密量取2、3、4、5、6、7 mL淀粉储备液置50 mL量瓶中,分别加0.25 mol·L-1盐酸溶液1.0 mL,并加入相应体积的0.04 mol·L-1盐酸溶液和0.04 mol·L-1氢氧化钠溶液,使各溶液的pH相同,用水稀释至刻度,摇匀,过滤,精密量取续滤液10 mL,各加入0.1 mL碘溶液,摇匀,作为淀粉线性溶液。
取淀粉线性溶液,按照紫外-可见分光光度法(《中国药典》2015年版四部附录0401紫外-可见分光光度法),在575 nm波长处测定吸光度,以吸光度为纵坐标、浓度为横坐标制作回归曲线。
结果:淀粉浓度在20.288~71.008 μg·mL-1范围内,吸光度与浓度呈良好的线性关系,线性回归方程为y=9.1x-0.018(r=0.999)。
4.3 准确度试验准确度试验前先进行预试验:取口服固体制剂按照“2.2测定法”进行检验,测出口服固体制剂中淀粉的大致含量。
根据预试验结果,分别精密称取40 mg、50 mg、60 mg淀粉各3份,每份添加空白辅料混合物(相当于50 mg淀粉的量),按照“2.2测定法”进行检测,计算回收率,结果见表 2。
|
|
表 2 6种口服固体制剂方法学验证试验结果 |
根据预试验结果,精密称取口服固体制剂粉末适量(相当于50 mg淀粉的量),共6份,按照“2.2测定法”进行检测,计算6份结果的相对标准偏差,结果见表 2。
5 讨论 5.1 方法准确度口服固体制剂“逆向工程”属于制剂处方前研究,其目的是为小试处方开发提供指导、缩短处方用量摸索过程,所有辅料的实际用量还需调整并经过制剂工艺和体外溶出行为检测的再次验证。本研究所使用的2种方法的回收率均在85%~110%、重复性试验RSD小于5.0%,能够满足试验准确度需求,且方法快速、简便,适合口服固体制剂中淀粉类辅料的含量测定。
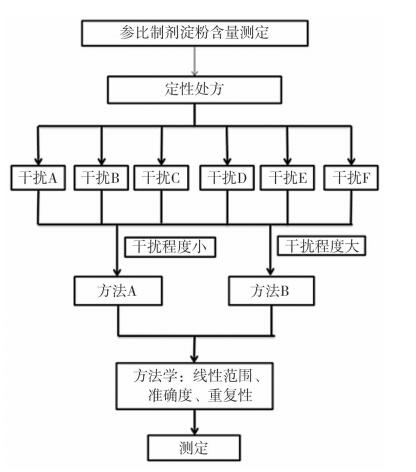
5.2 方法选择本文给出了2种测定法,主要考虑到不同口服固体制剂里的不同成分对方法的影响程度不同。方法A适用于干扰成分含量低、干扰程度低一些的口服固体制剂(采用10~50 mL乙醇能够去除干扰成分),方法回收率较高、重复性良好。方法B适用于干扰成分多、干扰程度高的口服固体制剂,可以用更多的试剂(大于50 mL)去除干扰成分。口服固体制剂中淀粉类辅料含量测定的“逆向工程”分析方法开发思路见图 2。
|
图 2 口服固体制剂中淀粉类辅料含量测定方法开发思路 |
笔者在专属性试验过程中,经历了2个误区。误区一:太过关注干扰成分与碘液显色,忽略其他方面的干扰因素;误区二:发现干扰成分消耗掉碘液,从而陷入碘液加入量研究的误区。口服固体制剂中淀粉类辅料的测定,往往受多种干扰成分的影响,不管何种干扰成分、如何干扰,其排除干扰影响的方式优先选择采用溶剂一次性清洗掉所有的干扰成分。
5.4 多种淀粉类辅料并存口服固体制剂中往往同时含有多种淀粉类辅料,相互干扰。如同时含有玉米淀粉、羧甲基淀粉钠时,可以利用二者在不同溶剂中的溶解度实现分离;如同时含有玉米淀粉、预胶化淀粉时,通过筛选测定波长先测出二者的总含量,然后利用制剂手段结合分析的方式,计算出实际处方中二者最合适的比例。
| [1] |
张建刚, 李生泉, 张丽. 微量淀粉含量测定的新方法研究[J]. 安徽农业科学, 2009, 26(37): 12377-12379, 12398. |
| [2] |
展海军, 崔丽伟, 李婕, 等. 用差热分析法测定玉米中淀粉含量[J]. 河南工业大学学报:自然科学版, 2012, 33(6): 31-35. |
| [3] |
何其芳, 李荣华, 郭培国, 等. 烟叶中淀粉含量测定方法的比较[J]. 现代食品科技, 2012, 28(2): 229-232. |
| [4] |
沈林峰, 沈掌泉. 应用近红外光谱和偏最小二乘回归法预测玉米中淀粉含量[J]. 化学分析计量, 2008, 17(6): 26-28. |
| [5] |
丁龙龙, 张彦华, 顾继友, 等. 傅里叶变换红外测定氧化淀粉的羧基含量初探[J]. 光谱学与光谱分析, 2014, 12(2): 401-404. |
| [6] |
卢林旋. 旋光法测定大米和玉米淀粉含量的条件控制研究[J]. 食品科技, 2010, 35(12): 272-274. |
| [7] |
廖燕芝, 杨代明, 张继红, 等. 气相色谱法测定魔芋食品中葡甘聚糖及淀粉含量[J]. 食品与生物技术学报, 2008, 27(4): 66-69. |
| [8] |
国家卫生和计划生育委员会, 国家食品药品监督管理总局. GB5009. 9-2016食品安全国家标准: 食品中淀粉的测定[S]. 2016.
|
| [9] |
徐昌杰, 陈文峻, 陈昆松, 等. 淀粉含量测定的一种简便方法:碘显色法[J]. 生物技术, 1998, 2(8): 41-43. |
| [10] |
谢跃生, 洪艳艳, 梁承慧, 等. 碘显色分光光度法检验淀粉:丙烯酰胺共聚反应[J]. 广西师范学院院报:自然科学版, 2015, 32(2): 49-52. |
| [11] |
丘进, 黎强. 分光光度法测定甲硝唑片含量的不确定度分析[J]. 中国药事, 2008, 22(9): 797-799. |
| [12] |
陆伟, 赵新静. 分光光度法测定维C银翘片中马来酸氯苯那敏的含量[J]. 中国药事, 2004, 18(7): 435-436. |
 2018, Vol. 32
2018, Vol. 32 