中药对照药材是我国药品监管、检验工作的对照物质之一,是执行中药质量标准的一个组成部分,《药品管理法》 [1]和《药品注册管理办法》 [2]赋予中国食品药品检定研究院为唯一合法的研制、分发中药对照药材的研制机构。目前,我院在发的中药对照药材品种达760余种,保证其质量稳定是保证我国药品质量监管的重要环节,也是标准物质研制工作的重要环节。开展稳定性期间核查,是主动及时地发现中药对照药材在贮存过程中发生的变化,尽早采取预防措施以规避风险的积极措施。本文通过2011年至2016年稳定性期间核查的实例,对影响中药对照药材稳定性的因素及稳定性期间核查方案的制订、实施进行探讨,为标准物质的研制提供参考。
1 稳定性期间核查的基本要求中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment(简称CNAS)发布的CNAS-CL01(即ISO/IEC 17025:2005)《检验和校准实验室能力认可准则》明确规定:对内部标准物质(参考物质)应进行核查(第5.6.3.2条);应根据规定的程序和日程对参考标准、基准、传递标准或工作标准以及标准物质(参考物质)进行核查,以保持其校准状态的置信度(第5.6.3.3条)[3]。《国家药品标准物质管理办法》 [4]第十条规定:国家药品标准物质不规定有效期,但应在规定的储存和使用条件下,定期进行特性量值的稳定性核查。标准物质的稳定性[5],系指在规定的储存和使用条件下、在规定的时间间隔内,使其具有的特性量值保持在规定范围内的能力,是标准物质的重要基本性质之一。标准物质的期间核查,系指相邻两次校准(或检定)期间内,按照标准物质证书上所规定的环境条件、储存方法、检测分析方法等进行稳定性的核查,以验证设备或标准物质是否处于校准状态,确保标准物质量值的准确性,从而确保其质量。
2 中药对照药材的特性中药对照药材为基原准确的原生药材粉末,是药品检验工作中按标准规定、供薄层鉴别使用的对照物质,为定性测量(qualitative measurement)[6](JJF 1005—2005标准物质常用术语和定义[s]),其行使量值的传递功能是通过薄层色谱的定性属性(qualitative attribute)。它对于中药材、中成药检验的规范化、重现性与专属性,具有不可替代的重要作用。例如黄连、黄檗或功劳木中均含有盐酸小檗碱,除此之外其它成分则有不同。因此,在中成药薄层检验中如果仅以盐酸小檗碱对照品作对照,仍无法确定药材投料的准确性;若同时以对照药材作对照,由于对照药材具备该品种的整体色谱特征,从而能够更为专属地鉴定药材投料的品种。
3 影响中药对照药材稳定性的因素及稳定性期间核查的必要性 3.1 中药材自身性质的影响中药对照药材为原生药材粉末,含有多类化学成分,绝大多数品种所含的成分尚为未知,仅个别品种已知含有少量成分,其所含主要成分常通过研制过程中依据文献资料获取信息,并依据其在标准方法中的应用加以判断。影响中药对照药材稳定性的因素及制备、贮存中应采取的措施往往缺乏针对性,尤其是首批研制的品种。例如,首批研制的梅花对照药材,主要含黄酮类成分及挥发性成分,依据药品标准使用时,发现其前处理方法采用甲醇提取,薄层鉴别时采用聚酰胺薄膜为固定相,展开剂采用36%的乙酸,检视方法采用三氯化铝显色剂,在紫外光灯(365 nm)下检视荧光斑点,由此确定其在标准使用中主要针对黄酮类成分进行检验。此类成分通常条件下稳定性较好,对于其可能含有的挥发性成分,通过有针对性地建立薄层色谱鉴别方法进行分析研究,最终依据其在标准中的用途,建议采用棕色西林瓶密封包装,室温、避光保存;但其它成分的稳定性情况难以全覆盖地进行研究,需要通过长期贮存后的期间核查来分析确定。再比如,薏苡仁对照药材主要含油脂及挥发性成分,在依标准使用时针对的也是此类成分,由于挥发性成分及油脂类成分易散失,造成薄层色谱无法检出斑点,故采用棕色安瓿瓶并充氮气封装。其它如含挥发性成分的药材(荆芥、薄荷、乳香等),含糖高的药材(枸杞、五味子等),易变色的药材(金银花等花类及叶类),富含油脂类成分易酸败、走油的药材(大风子、火麻仁、鸭胆子)等,均采取安瓿瓶封装、缩短研制周期或缩短稳定性期间核查间隔的时间等措施。
3.2 外部环境因素的影响中药对照药材受物理(如温度、湿度、日光、水分等)、化学(如氧化、分解等)、生物(生化反应、生霉)等因素的影响很大,含成分类别不同的药材受影响的因素不同、程度也不同,有些易生虫、霉变(如甘遂、红花等);有些易吸潮结块等,这些变化均将对药材质量产生直接影响。
3.3 加工制备过程的影响中药对照药材均为粉碎的粉末,相对加大了与空气接触的比表面积,易发生氧化、分解、转化等变化;粉碎过程中,机械摩擦升温对药材产生的某些潜在影响可能在以后的贮存过程中逐渐产生;有些大装量品种不宜用塑料制品包装,许多对制备有特殊防护措施要求才能保证其稳定性的品种,也需要针对性地进行实际研究。
4 稳定性期间核查方案的制订 4.1 核查项目的选择影响中药对照药材稳定性的因素包含很多的特性量值,如水分、浸出物、指标成分含量测定等等,但期间核查重点考察与其用途直接相关的指标,中药对照药材为粉末状药材,主要用于薄层鉴别,因而选择薄层鉴别作为核查项目最能反映实际应用中的问题。对照药材薄层图谱这一特性量值易因前述的各种影响因素而发生变化,能较全面地反映对照药材内在多类成分的状况;虽然薄层色谱鉴别是一个相对开放性的实验,易受环境因素的影响,尤其是温、湿度影响,出现重现性不佳的问题,但因有随行的溯源样品,可以相对完整地保留成分信息,发现粉末状的成品在贮存中发生的变化[6-7]。
4.2 核查实验方法的选择薄层色谱鉴别方法的选择应保证核查结果的可追溯性,因而应选取标定该批对照药材时使用的薄层鉴别方法。通常为针对不同成分部位的两个鉴别方法。同时还需与该批药材标定的档案图谱比对,有时还需要对薄层展开剂系统进行调整,以尽可能地重现该批药材标定时呈现的色谱状况。由于内在成分的不稳定性主要反映在成分的减少或成分的分解造成斑点增加,故点样量采用两个梯度:第一个梯度采用标准规定的点样量,以反映按标准方法操作时的薄层色谱状况;第二个梯度采用两倍于标准规定的点样量,以反映样品可能发生变化时的薄层色谱状况,如标准规定5μL点样量时,操作中应同时点样5μL和10μL。实验时,对照药材成品与溯源样品应平行操作。
4.3 对照物质的选择对照药材的稳定性是相对的,在一定条件下才能保证其原有特性量值的持续性。完整药材在贮存过程中可能发生变化,但相对来说变化的风险要小一些;对照药材为粉末状,虽然密封分装在棕色瓶中,但因经历过加工制备等环节,其受环境因素的影响及自身发生变化的可能性,较完整药材时增大很多。故应选择与对照药材同批次未粉碎的对照药材留样作为期间核查的参照物,称为溯源样品。临实验前,取未粉碎的完整溯源样品,采用实验室用小型粉碎机粉碎、过筛,与待考察的同批对照药材成品同时取样实验。见图 1。

|
图 1 对照药材稳定性期间核查供试品及溯源样品 |
关于核查品种的选择,首先应选取贮存时间达到3年的品种,但也要同时结合对照药材的换批研制、日常检验使用状况以及其它与质量控制相关的实验工作,以提高核查实验结果的利用效率,不显著增加工作量和对照药材成本的负担。核查对象的通常选择原则为:1)换批次品种,在3年内无稳定性核查记录而仍在使用的品种;2)首批建立的品种,贮存时间达到3年的品种;3)以往使用时或核查中发现有不稳定记录的品种,此类品种需要相对缩短核查时间间隔。
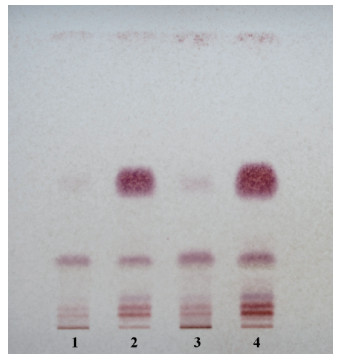
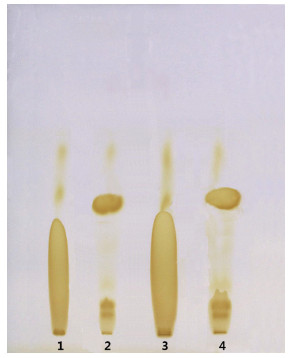
4.5 核查结果的评价通过观察成品对照药材与溯源样品薄层色谱是否一致,评价该批对照药材的稳定状况。由于核查的成品对照药材与溯源样品为同一批原料,薄层色谱斑点在颜色、数量、大小上应无显著差异,故如果这些特征一致,即判定为稳定性合格。若有差异或差异显著时,经重复实验确认,同时与该批对照药材标定的档案图谱比对,以最终得出稳定性不合格的结论。不合格结果主要有两类情况:对照药材成品与溯源样品的薄层色谱比较,一是出现的斑点减弱或缺失;二是出现的斑点增加或拖尾。例如巴豆的核查结果,对照药材成品色谱斑点比较溯源样品斑点在标准规定点样量时有主斑点的缺失;为验证该主斑点是否存在,加大点样量至规定点样量的2倍时,可见该主斑点存在,但颜色极淡,见图 2。又如,大风子的核查结果,不仅出现主斑点的缺失,还出现其它成分且该成分发生了拖尾扩散现象,见图 3。
|
图 2 巴豆对照药材稳定性期间核查不合格薄层色谱图(斑点缺失) 1、3.巴豆对照药材成品 2、4.巴豆对照药材溯源样品 |
|
图 3 大风子对照药材稳定性期间核查不合格薄层色谱图(斑点拖尾) 1、3.大风子对照药材成品 2、4.大风子对照药材溯源样品 |
自2011-2016年,我院大力推行标准物质稳定性期间核查工作,结合对照药材换批标化时的稳定性考察,目前在发的776种对照药材中,85%以上具备了3年内稳定性期间核查记录。对照药材的稳定性核查结果及采取的相应措施主要归结为以下4类情况,具体情况见表 1。
|
|
表 1 2011-2016年中药对照药材稳定性期间核查结果及相应措施 |
中药对照药材的稳定性在贮藏3年期内,大部分品种较稳定;已发现不稳定的品种主要发生在富含挥发性成分、脂类成分、内酯类成分的品种,以及其它特定成分的品种。
针对不稳定品种,采取了立即停发的措施[8],同时分析可能存在的不稳定性因素,采取相应的解决方法,包括改变包装方式、增大原料粉碎粒度、缩短制备周期等。
4.6.1 改变包装方式目前的包装方式主要包括棕色西林瓶装、白色塑料瓶装、直管安瓿包装等,以棕色西林瓶密封包装方式为主。改变包装方式,主要是将原西林瓶密封包装改用直管安瓿包装,或充氮气直管安瓿密封包装。例如,充氮气直管安瓿瓶封装的薄荷,稳定性从可保证1年提高到至少保证3年。
4.6.2 改变原料粉碎粒度一些富含糖类、脂类的药材或树脂类药材,如枸杞、大枣、郁李仁、乳香等,在保证粒度均匀的前提下,增加粒径,可减少与空气接触的表面积,减少结块和颜色变化。例如,受成本条件限制,很多有潜在不稳定因素的品种仍然用棕色西林瓶密封包装,这是日后应着力考虑解决的问题。
目前,在换批标化时稳定性考核及期间稳定性考核方式外,针对一些建立历史长久的品种,不仅有3年内的考察记录,还具备了连续批次考察的一手资料,如大黄、三七、甘草、防风等,在第四或五批换批标化时,同时考察第一、二、三或第四批的稳定性,具备了稳定性考察的多年累积数据。结果显示,一些品种贮藏10年左右均可表现出良好的稳定性。依据此结果,在换批研制时,既可加大此类品种的制备量,这样做不仅可以提高工作效率,减少成本损耗;也易保持对照药材的一致性和延续性。
| [1] |
中华人民共和国主席令第四十五号中华人民共和国药品管理法[S]. 2001.
|
| [2] |
国家食品药品监督管理局. 国家食品药品监督管理局令第28号药品注册管理办法[S]. 2007.
|
| [3] |
中国合格评定国家认可委员会. CNAS-CL01: 检测和校准实验室能力认可准则[S]. ISO/IEC 17025, 2005.
|
| [4] |
国家食品药品监督管理总局. 国家食品药品监督管理总局令第5号体外诊断试剂注册管理办法[S]. 2014.
|
| [5] |
张俊爽, 吕翠杰. 期间核查与稳定性考核的关系[J]. 中国计量, 2013, 3: 49-50. |
| [6] |
于亚东, 刘媛. 标准物质新老定义的理解与比较[J]. 化学分析计量, 2010, 19(4): 4-8. |
| [7] |
曹丽梅, 赵宗阁, 马玲云, 等. 试论国家药品标准物质的稳定性及期间核查[J]. 中国药事, 2012, 26(1): 5-7. |
| [8] |
中国食品药品检定研究院. 中检标物[2011] 1445号国家药品标准物质供应管理规范(试行)[S]. 2011.
|
 2017, Vol. 31
2017, Vol. 31 
