无菌药品的微生物污染是影响药品生产质量和引发临床不良反应的主要原因之一[1],近年来发生的“欣弗”和“刺五加”事件反映了微生物污染为目前药品质量的最大挑战之一,污染微生物的控制和检验在无菌药品生产以及质量控制中起到至关重要的作用[2]。
制药企业微生物实验室必须对使用菌种进行定期的转种传代,并做纯度、特性等实验室所需关键指标的确认[3];实验菌种的保存在药品微生物检验过程中非常重要[4],其原理是营造一个低温、干燥、缺氧和营养缺乏、新陈代谢活动处于高度静止状态的环境[5],通过保持菌种原有的生物学特性以保证实验室质量控制和日常检验使用[6],不良的方法会导致菌种发生老化、退化、变异、污染等情况。
微生物实验室主要对两类菌种进行保存:①标准菌种,用于验证培养基和检验方法的适用性;②污染菌种,源于原材料、半成品及成品监测过程中的污染微生物,经过16S-rRNA基因序列分析法[7]或傅立叶变换红外光谱法[8](Fourier Transform Infrared Spectrometer,FTIR)鉴定细菌后,应用于医药企业微生物污染调查,也可用于指导灭菌验证以及环境分离菌株的消毒剂杀灭效果评估[9]等。
本实验通过复苏率、形态学、染色学和数值分类鉴定方法[10-11](Analytic Products Inc,API),对比液体石蜡覆盖保存法和10%甘油-生理盐水冷冻管保存法,最后选择出一种操作简便、菌种稳定性好、保存时间长的通用菌种保存方法,给同行提供参考。
1 实验材料与方法 1.1 仪器设备和耗材BHC-1000ⅡA/B3型生物安全柜(苏州安泰空气技术有限公司),DENSIMT型细菌比浊仪(法国梅里埃诊断产品有限公司),GNP-9270型隔水式培养箱(上海精华宏实验设备有限公司),BCD-252KBSN型冰箱(海尔集团),DM500型数码显微镜(德国Leica公司),10 μL无菌接种环,2 mL内旋盖无菌冻存管,3 mL无菌巴斯德吸管,梅里埃厌氧培养盒套装,甘油(分析纯),生理盐水(0.85%,5 mL)。
1.2 菌种金黄色葡萄球菌[CMCC(B)26003]、铜绿假单胞菌[CMCC(B)10104]、生孢梭菌[CMCC(B)64941]、枯草芽孢杆菌[C M C C (B) 6 3 5 0 1]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003],均购自中国食品药品检定研究院;藤黄微球菌,来源于洁净环境分离菌;试验用菌种的传代次数不得超过5代。
1.3 实验方法① 培养基制备及灭菌:营养琼脂培养基,取营养琼脂培养基33 g,加1 L纯化水,搅拌溶解,分装,121 ℃灭菌20 min;改良马丁琼脂培养基,取改良马丁琼脂培养基42.5 g,加1 L纯化水,搅拌溶解,分装,121 ℃灭菌20 min;pH 7.0氯化钠-蛋白胨缓冲液,取pH 7.0氯化钠-蛋白胨干粉16.1 g,加水1 L,搅拌溶解,分装,121 ℃灭菌30 min;含0.05%(mL/mL)聚山梨酯80的0.9%氯化钠溶液,取0.05 mL聚山梨酯80溶液置100 mL的0.9%氯化钠溶液中,搅拌溶解,121 ℃灭菌30 min;20%甘油,量取20 mL丙三醇,加100 mL纯化水,搅拌使混匀,装置密闭容器,121 ℃灭菌30 min。
② 菌液制备:接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的新鲜培养物至营养肉汤培养基中,接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,30~35 ℃培养18~24 h;接种白色念珠菌的新鲜培养物至改良马丁培养基中,23~28 ℃培养24~48 h;接种黑曲霉的新鲜培养物至改良马丁琼脂培养基中,23~28 ℃培养5~7 d。
③ 液体石蜡覆盖保存法:取金黄色葡萄球菌、铜绿假单胞菌、生孢梭菌、枯草芽孢杆菌、藤黄微球菌培养物,用一次性无菌接种环取一环在营养琼脂斜面上进行划线,30~35 ℃培养18~24 h,生孢梭菌放置于厌氧盒内培养;取白色念珠菌和黑曲霉培养物,用一次性无菌接种环取一环在改良马丁琼脂斜面上进行划线,分别置23~28 ℃培养24~48 h和5~7 d;将液体石蜡装瓶121 ℃灭菌30 min,再置100 ℃烘箱烤2 h,使水分蒸发,用灭菌吸管吸取处理后的液体石蜡加入长好菌苔的斜面试管内,使液体石蜡液面高出斜面顶端1 cm,直立,2~8 ℃冰箱保存。
④ 10%甘油-生理盐水冷冻管保存法:按液体石蜡覆盖保存法制备菌苔,黑曲霉加入约2~3 mL的含0.05%(mL/mL)聚山梨酯80的0.9%氯化钠溶液,将孢子洗脱,然后用管口带有薄的无菌棉花或纱布能过滤菌丝的无菌吸管吸出孢子悬液置无菌试管内;将已制备好的菌种用一次性无菌接种环轻轻刮取菌苔,并通过接种环与试管壁之间的轻轻摩擦使细菌充分扩散到预先装于试管中的无菌生理盐水中,在细菌比浊仪上测量和调整菌液浓度,使其大于7.5麦氏浓度,黑曲霉直接取洗脱的浓孢子悬液进行保存;将以上各试验菌种以0.5 mL每管的装量分装置2 mL的冻存管中,再分别加入0.5 mL的20%无菌甘油,混匀,制备成10%甘油-生理盐水菌悬液,放置菌种保存盒内(图 1),至-20 ℃冰箱保存。
|
图 1 10%甘油-生理盐水冷冻管保存法 |
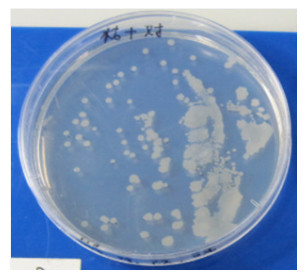
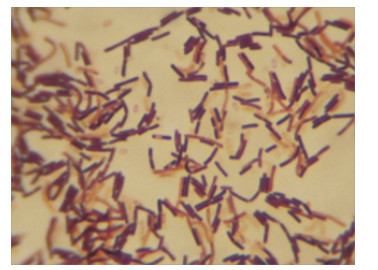
⑤ 检测方法:验证时限至24个月,于6、12、15、18、21、24个月时,分别取出每株液体石蜡覆盖保存法的斜面和10%甘油-生理盐水冷冻管保存法的冻存管菌种20支,置室温下解冻后,用无菌接种环取一环(10 μL)进行平板划线将菌种复苏,检测细菌的存活情况,并对复苏的菌种进行菌落形态[11](图 2)、细胞形态(图 3)、革兰氏染色(图 3)比对,以及API微生物系统鉴定(图 4)。
|
图 2 枯草芽孢杆菌菌落形态 |
|
图 3 枯草芽孢杆菌细胞形态 |

|
图 4 枯草芽孢杆菌API微生物系统鉴定反应结果 |
经复苏后的20支菌株应全部生长,并且菌落形态、细胞形态、革兰氏染色情况与原始菌株一致,API微生物系统鉴定结果为原始菌株,判断该验证有效期内保存方法符合规定。
2 结果采用液体石蜡覆盖保存法,不同菌株之间保存时间差异较大,保存时限最短为6个月;而采用10%甘油-生理盐水冷冻管保存法,金黄色葡萄球菌(革兰氏阳性菌)、铜绿假单胞菌(革兰氏阴性菌)、生孢梭菌(厌氧菌)、枯草芽孢杆菌(芽孢杆菌)、白色念珠菌(酵母菌)、藤黄微球菌(洁净环境微生物)在24个月,黑曲霉(霉菌)在18个月内能100%复苏,且不会发生生物学上的特性变化,复苏结果见表 1。
|
|
表 1 不同复苏时间菌种的存活情况 |
菌种保存方法验证时需要关注的因素包括:①选择验证菌株是否有代表性;②每个保存时限的测试数量为多少;③如何判断与原菌株生物学特性是否发生变异。
本实验针对上述关键因素进行验证:①验证菌株,增加了洁净环境分离菌株,以代表实际生产中可能遇到的污染菌,最后挑选污染比例最高的藤黄微球菌进行测试;②测试数量,通过取20支菌株进行复苏并确认存活情况,如有1支不能生长则复苏率低于95%置信限[12],保存时限存在显著性差异,该限期不能用于菌种保存;③变异程度,通过API微生物鉴定法较形态染色学方法更能准确地判断与原菌株生物学特性是否发生变异[13]。
10%甘油-生理盐水冷冻管保存法与液体石蜡覆盖保存法比较见表 2,10 %甘油-生理盐水冷冻管法较液体石蜡覆盖保存法有以下优点:①保存时间长,经验证细菌和酵母菌能保存24个月,霉菌保存18个月,避免由于传代频繁而造成菌株变异和交叉污染[14];②占用空间少,使用2 mL冷冻管而不是10 mL或更大的试管,适用于微生物实验室大量的菌种保存需求;③操作安全,整个操作过程使用一次性的无菌接种环、冷冻管、巴氏管,减少因试管破碎而造成生物泄漏的风险;④出错风险低,规定1个冷冻管只能使用1次,避免反复冷冻造成菌株死亡或变异情况,以及在操作过程中的交叉污染风险[15];⑤菌种稳定性好,避免保存温度较高、营养成分等因素造成的缓慢繁殖和变异[16],因此,本研究选择10%甘油-生理盐水冷冻管法用于菌种保存。
|
|
表 2 两种菌种保存方法的比较 |
| [1] |
范一灵, 冯震, 钟玮, 等. 无菌药品生产企业核心区微生物污染调查与分析[J]. 中国药事, 2014, 28(6): 586-590. |
| [2] |
曹元, 梁毅. 无菌药品灭菌前微生物控制研究[J]. 中国药业, 2009, 18(22): 9-11. DOI:10.3969/j.issn.1006-4931.2009.22.009 |
| [3] |
中国药典: 四部[S]. 2015: 通则9203.
|
| [4] |
陈晓燕, 林光. 微生物实验菌种保存方式探讨[J]. 临床合理用药杂志, 2014(29): 129-130. DOI:10.3969/j.issn.1674-3296.2014.29.117 |
| [5] |
李文广. 医学微生物菌种长期保存方法探讨[J]. 中国热带医学, 2009, 9(7): 1358-1359. |
| [6] |
田冬梅, 娄志红, 张肖宁. 浅谈药品微生物实验室质量管理[J]. 中国药房, 2017, 28(7): 1003-1006. DOI:10.6039/j.issn.1001-0408.2017.07.39 |
| [7] |
范一灵, 房蕊, 蒋波, 等. 微生物鉴定分型技术应用于医药企业微生物污染调查[J]. 中国医药工业杂志, 2010, 41(11): 810-817. DOI:10.3969/j.issn.1001-8255.2010.11.006 |
| [8] |
裴琳, 胡昌勤, 马仕洪, 等. FTIR法用于药品检出菌与药品微生物检验洁净室环境菌的相关性考察[J]. 药学学报, 2007, 42(11): 1189-1194. DOI:10.3321/j.issn:0513-4870.2007.11.014 |
| [9] |
何国强, 王玮, 张贵良. 制药洁净室微生物控制[M]. 北京: 北京工业出版社, 2013: 168-168.
|
| [10] |
杨燕兰, 梁嘉雯. 浅谈微生物实验室中细菌的鉴定方法建立及探索[J]. 中国卫生标准管理, 2016, 7(9): 116-118. |
| [11] |
车萍, 张颖颖, 田洪波. 形态学实验室菌种保存的实验方法改革[J]. 现代医药卫生, 2013, 29(6): 912-912. |
| [12] |
杜荣骞. 生物统计学[M]. 3版. 北京: 高等教育出版社, 2009: 46-47.
|
| [13] |
杨兰芬. API微生物鉴定系统在实验室质控及微生物检验中的应用[J]. 中国卫生检验杂志, 2003, 13(4): 513-513. |
| [14] |
叶迎春, 赵世鸿, 凌体淑. 3种菌种保存法比较[J]. 中国误诊学杂志, 2004, 4(3): 386-386. |
| [15] |
黄霞云. 人工传代、低温与超低温法保存菌种的效果比较观察[J]. 现代医院, 2006, 6(8): 73-74. |
| [16] |
潘友文, 钱维清, 熊家娟. 现代医药工业微生物实验室质量管理与验证技术[M]. 北京: 中国协和医科大学出版社, 2004: 28-28.
|
 2017, Vol. 31
2017, Vol. 31 