2-氯乙醇(Ethylene Chlorohydrin, ECH)为无色透明液体,熔点-62.6 ℃,相对密度1.2045,沸点95~98 ℃(97.8 kPa),与水、乙醇能按任意比例混溶。2-氯乙醇是一种刺激体表、具有急性毒性,并且能通过皮肤快速吸收的液体。ECH具有轻微的致突变性,具有产生胎儿毒性和致畸性改变的潜能,并对体内的几种器官系统造成损伤,包括肺、肾、中枢神经系统和心血管系统[1],有报道认为,纯ECH对大多数组织有相当大的破坏性[2]。《ISO 10993.7-2008医疗器械生物学评价第7部分:环氧乙烷灭菌残留量》中的“特殊情况”特别提到,含氯粘弹性材料制成的眼用器械其ECH接受水平可能需要被评估,因为ECH残留引起的眼毒性大约是同等水平环氧乙烷(EthyleneOxide,EO)的4倍[3],对于由环氧乙烷灭菌的医疗器械来说,不仅会有环氧乙烷残留,还可能会有2-氯乙醇残留,尤其是有氯离子存在时,氯离子很容易和EO反应生产ECH。《GB/T16886.7-2015医疗器械生物学评价第7部分:环氧乙烷灭菌残留量》对ECH的接触限量做了详细的规定,其中对于持久接触器械(接触超过30天),ECH对患者的平均日剂量不应超过0.4 mg·d-1。《YY0290.8-0290.8-2008眼科光学人工晶状体第8部分:基本要求》也对ECH做了限值规定:每个人工晶状体ECH残留量每天应不超过2.0µg,每个晶状体ECH残留总量不应超过5.0µg[4]。
在实际测试应用中,相同或类似样品的分析结果之间存在着明显差异,量值很难做到统一,很难保证不同实验室的检测结果可比。为了使正常使用的医疗器械对患者造成的危害降至最小,保障公众用械安全,对经环氧乙烷灭菌的医疗器械进行ECH残留量水平评价具有重要意义。为了使医疗器械的检验更加规范化,急需研制准确、有效及可溯源的ECH标准物质,来保证分析数据的准确性和重复性,从而保证产品质量检验的公平。我国目前尚未有ECH纯品的标准物质。因此,研制医疗器械用ECH标准物质是非常必要的。
1 材料与方法 1.1 原料筛选与考核参考国外的标准物质并考虑原材料价格及来源稳定等因素,本文选用标示值在98.0%以上的ECH作为候选物进行标准物质的研制,通过棕色安剖瓶分装,每支包含ECH纯品1 mL,采用气相色谱外标法(GC)定值,多家实验室协作标定。中国食品药品检定研究院首先对原材料进行了结构测定和纯度检查。
1.1.1 主要仪器和试剂气相色谱-质谱联用仪:岛津GCMS-QP2010;天平AE240(梅特勒托利多公司);甲醇(HPLC级,TEDIA公司);ECH原料(纯度98%以上,批号:STBB5988V);甲醇中ECH标准溶液(批号:LB96492 4-8085,2000µg·mL-1,SUPELCO. Inc)。
1.1.2 试验方法采用气质联用仪对ECH原料进行主成分定性。标准溶液配制:精密量取2000µg·mL-1的ECH标准物质1.0 mL,甲醇定容至50 mL,浓度为40 µg·mL-1;ECH原料溶液配制:精密称取ECH原料0.1050 g,甲醇溶解并定容至100 mL,取该溶液2.0 mL,甲醇定容至50 mL,浓度为42 µg·mL-1。色谱与质谱条件:色谱柱型号ZB-624毛细管色谱柱(30 m×0.32 mm×1.8 µm,固定相为6%氰丙基苯基94%二甲基聚硅氧烷,Phenomenex公司);载气种类:氦气(纯度大于99.999%);柱温采用程序升温:初始温度50 ℃,保持1 min,以5 ℃·min-1升温至100 ℃,保持1 min;柱流速1.5 mL·min-1;分流比1︰1;进样口温度180 ℃;进样量1µL;接口温度250 ℃,离子源温度230 ℃,电子轰击电离源(EI, 70 eV),溶剂切除时间4.0 min;Scan全扫描模式,扫描范围为35~500 u。分别测定外购的ECH标准溶液和ECH原料。
1.2 标定方法及方式标准物质的定值是对标准物质特性量赋值的全过程。必须保证其量值具有溯源性。根据《JJG1006-1994一级标准物质技术规范》的要求,结合目前ECH分析技术的发展状况,对ECH标准物质纯度的定值选用气相色谱(GC)外标法。对于在GC中没有响应的水分和无机物,则分别采用卡氏水分分析仪和等离子体质谱(ICP-MS)进行分析[5-14]。
ECH标准物质的定值方式采用多个实验室协作标定。协作标定采用相同精度的分析方法,在对定值方法进行深入研究的基础上进行。为了进一步规避可能产生的系统误差,参照ISO导则35的要求,主要从两方面进行控制:a)要求合作定值实验室具有同等的测定能力,以提供具有可接受准确度的测量结果;b)保证实验室自身以及实验室之间单个测量结果之间的差异在本质上是可以统计的。此外,各实验室得到的每个结果都要满足溯源性要求,即所用仪器设备都要求进行检定。参照ISO导则34︰2000《标准物质生产者能力的通用要求》,从协作标定机构的管理能力、技术能力及硬件设施等方面,对参加协作定值的实验室提出明确要求并自愿报名参加[15-16]。
1.2.1 主要仪器和试剂气相色谱仪:岛津GC-2010;卡氏水分分析仪(梅特勒托利多公司,型号:DL31);等离子体质谱仪(ICP-MS,型号:X Series)。
1.2.2 试验方法用卡氏水分分析仪对ECH中的含水量进行测定,平行测定5份样品。用ICP-MS对样品中的无机物进行测试,平行测定3份样品,样品处理:精密称取样品0.1 g,加入1 mL硝酸和1 mL双氧水,微波消解至溶液澄清,超纯水定容至10 mL后,测定。ECH中的主成分测定采用GC外标法,采用协作标定的方式进行定值。色谱条件:色谱柱:AT-624(30 m×0.25 mm×1.4µm);柱温:100 ℃(5 min);载气:氦气,线速度控制,线速度为27.8 cm·s-1,柱流量1.0 mL·min-1,不分流进样;进样口温度:200 ℃,进样时间:0.04 min;样品加热温度:80 ℃,加热时间:30 min;检测器:电子捕获检测器(ECD),检测器温度:210 ℃,检测电流:1 nA。
1.3 均匀性和稳定性试验标准物质的特性应该是均匀的,即在规定的细分范围内其特性保持不变。为了检验样品是否均匀,通常随机抽取一定数量的最小包装单元,对抽出的各样品在控制同样的实验条件下进行测定,从而使各样品间的差异完全由样品的不均匀性反映出来。方差分析法是用来统计检验均匀性的最常用方法。此法是通过组间方差和组内方差的比较来判断各组测量值之间有无系统性差异,如果二者之比小于统计检验的临界值,则认为样品是均匀的。在ECH的均匀性检验中,随机抽取ECH标准物质6瓶,每瓶重复测定5次。采用GC外标法对每个样品的纯度进行测定。
标准物质的稳定性是指在规定的时间间隔和环境条件下,标准物质的特性量值保持在规定范围内的性质。为了评定标准物质的稳定性,在储存期间定期抽样测定。在测量误差中,除了测量方法、测量仪器、实验条件变化带来测量误差外,标准物质可能发生的变化也会带来误差,因而,在做稳定性检验时,尽可能地控制各种条件,使其保持一致,使测量结果的差异仅仅体现由标准物质变化所引起的误差。在ECH标准物质的研制中,每次随机抽取瓶数均为5瓶,每瓶样品重复测定5次,溶液配制方法和实验条件与标定方法相同。分别于分装后6个月和分装后12个月用GC外标法对主成分ECH占有机成分的百分含量进行测定。
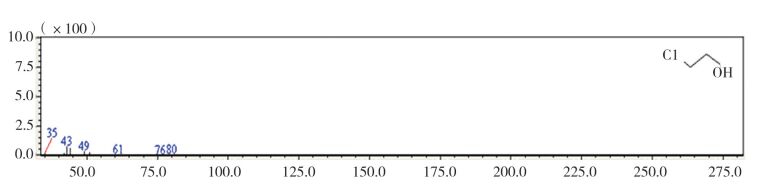
2 结果 2.1 原料筛选与考核结果ECH原料的检索结果与ECH标准物质的检索结果一致;通过与ECH标准物质比对、谱图解析和谱库检索,确定所选择原料的主成分为ECH,表明所选择的原料为高纯度的ECH,是研制ECH标准物质的理想原料。见图 1。
|
图 1 ECH峰检索结果 |
ECH含水量测定结果见表 1。含水量将作为杂质的一部分从标准物质特性量值中扣除。
|
|
表 1 ECH含水量测定结果 |
测试结果见表 2。共测定了16种金属离子,其他离子含量太低没有进行统计,因为样品中存在与测量离子相对应的阴离子,因此进行了2倍扩展。
|
|
表 2 无机物ICP-MS测试结果 |
有机成分中的主成分ECH测定采用GC外标法,采用协作标定的方式进行定值。每个实验室的标定结果均是平行测定3个样品,每个样品重复测定5次后取总平均值。测定结果见表 3。
|
|
表 3 协作标定结果统计 |
ECH待标物中ECH的含量按下式计算:ECH百分含量=(100% -水分百分含量-无机物百分含量),主成分均值百分含量=(100% -0.060% - 0.027%)98.01% =97.92%。
2.2.5 不确定度评定建立数学模型:V=x+Δ,其中:V代表ECH含量测量结果,x代表ECH含量测量值,Δ代表误差的影响。
不确定度传播率:uc2(V)=u2(x)+ u2(Δ),其中:u(x)可通过对测量值进行A类评定获得,u(Δ)可通过对ECH纯度测量有影响的各因素进行B类评定获得。
2.2.5.1 A类不确定度评定A类不确定度评定可通过各分量的平均值的标准偏差得到。根据“2.2.4”节中ECH含量的计算公式可得:
| $\begin{array}{l} u_{\rm{r}}^2\left( {\rm{x}} \right){\rm{ = }}u_{\rm{r}}^2\left( {{\rm{水分}}} \right) + u_{\rm{r}}^2\left( {{\rm{无机物}}} \right) + u_{\rm{r}}^2\left( {{\rm{主成分}}} \right)\\ {u_{\rm{r}}}\left( {\rm{x}} \right){\rm{ = }}\sqrt {{{\left( {\frac{{0.0006{\rm{\% }}}}{{0.06{\rm{\% }}}}} \right)}^2} + {{\left( {\frac{{0.0007{\rm{\% }}}}{{0.027{\rm{\% }}}}} \right)}^2} + {{\left( {\frac{{0.236{\rm{\% }}}}{{{\rm{98}}{\rm{.01\% }}}}} \right)}^2}} \\ {\rm{ = }}0.01。\\ u\left( {\rm{x}} \right) = {u_{\rm{r}}}\left( {\rm{x}} \right) \times {\rm{ECH}}百分含量{\rm{ = }}0.01 \times {\rm{97}}{\rm{.92\% }}\\ {\rm{ = 0}}{\rm{.0098\% 。}} \end{array}$ |
1)多家定值结果不确定度的评定u多家参加定值实验室采用的均为GC外标法,因此方法的响应因子基本相同,由此产生的不确定度可以忽略不计。
2)均匀性分析引入的不确定度评定uH样品不均匀性产生的不确定度,包括样品加工过程的均匀性、分装均匀性以及平行实验分析间的偏差,标准物质的不均匀性,以独立测量的平行实验来表示,即以均匀性检验结果的相对标准偏差来表示。在标准物质均匀性研究中,经过检验证明uH可以忽略不计。
3)稳定性引入的不确定度评定uR在标准物质稳定性研究中,由于ECH标准物质目前只有2组稳定性考察数据,无法进行统计学分析,故稳定性引入的不确定度评定uR暂不予考虑。
因此,ECH标准物质标定的B类不确定度可以忽略不计。
2.2.5.3 扩展不确定度U| $U = k \times u\left( {\rm{x}} \right) = 2 \times {\rm{0}}{\rm{.0098\% }} = 0.02{\rm{\% }}$ |
其中,k=2,因此,ECH标准物质含量的定值结果为97.92%±0.02%。
2.2.6 量值溯源及确定量值的溯源性是实现分析结果有效性和可靠性的重要措施之一。本项目采用多家实验室协作标定的方式进行定值。在协作标定前,要求各个参加协作标定的实验室都要对所用的仪器进行校准,并获得国家法定计量单位颁发的校准证书之后才能进行协作标定实验。因为校准是在测量仪器所指示的量值和测量标准所复现的量值间建立关系的过程,也是建立溯源性最根本的过程,只有通过校准,才能在实践中获得对参考标准的溯源性。
2.3 均匀性和稳定性试验结果 2.3.1 均匀性检验结果按上述方法对标准物质的均匀性数据进行了统计处理。结果见表 4。ECH标准物质的均匀性经F检验后显示,在95%置信概率下F<F(0.05),标准物质是均匀的。
|
|
表 4 均匀性检验结果 |
标准物质稳定性检验结果见表 5。从数据可以看出,ECH标准物质在12个月内是稳定的。有关稳定性的考察在今后的工作中还将继续进行。
|
|
表 5 稳定性检验结果 |
ECH标准物质经过严格的考察和定值,具有明确的量值和不确定度,经过均匀性与稳定性检验,表明ECH标准物质是均匀的和稳定的。ECH标准物质的研制成功,为医疗器械检测实验室提供了量值溯源物质,从而可以提高检测的质量和实验室间检测数据的可比性,以保证检测结果的准确且具有量值的溯源性。另外,还可用来校准仪器,对检测方法进行验证以及对检测实验室进行质量控制。
【致谢:本论文的协作标定工作得到了河南省医疗器械检验所、湖南省医疗器械与药用包装材料(容器)检验所、陕西省医疗器械质量监督检验院、深圳市药品检验所、淮南市医疗器械检测中心的大力协助,在此一并致谢!】
| [1] |
国家质量监督检验检疫总局. GB/T 16886. 7-2015医疗器械生物学评价第七部分: 环氧乙烷灭菌残留量[S]. 2015.
|
| [2] |
Wallace L Guess. Tissue Reactions to 2-chloroethanol in Rabbits[J]. Toxicology and Applied Pharmacology, 1970, 16(2): 382-390. DOI:10.1016/0041-008X(70)90009-8 |
| [3] |
ISO. 10993.7-2008 Biological Evaluation of Medical Devices Part 7:Ethylene Oxide Sterilization Residuals[S]. 2008.
|
| [4] |
国家质量监督检验检疫总局. YY0290. 8-0290. 8-2008眼科光学人工晶状体第8部分: 基本要求[S]. 2008.
|
| [5] |
Tateo F., Bononi M.. Determination of Ethylene Chlorohydrin as Marker of Spices Fumigation with Ethylene Oxide[J]. Journal of Food Composition and Analysis, 2006, 19(1): 83-87. DOI:10.1016/j.jfca.2004.12.003 |
| [6] |
刘成红, 裴燕, 任秀如, 等. GC法测定羟乙基淀粉130/0.4中2-氯乙醇的残留量[J]. 解放军药学学报, 2013, 29(4): 357-359. |
| [7] |
高广惠, 王晓黎, 董宇, 等. 毛细管气相色谱法测定羟乙基淀粉中2-氯乙醇的残留量[J]. 沈阳药科大学学报, 2010, 27(5): 385-387. |
| [8] |
Whitbourne J E, Mogenhanm J A, Ernst R R. Determination of 2-chloroethanol in Surgical Materials by Extraction and Gas Chromatography[J]. Journal of Pharmaceutical Sciences, 1969, 58(8): 1027-1025. |
| [9] |
McDonald T O, Roberts M D, Borgmann A R. Ocular Toxicity of Ethylene Chlorohydrin an Ethylene Glycol in Rabbit Eyes[J]. Toxicology and Applied pharmacology, 1972, 21(1): 143-150. DOI:10.1016/0041-008X(72)90035-X |
| [10] |
付步芳, 冯晓明. 运用气相色谱法评价体外循环一次性血管路中2-氯乙醇残留量的安全性[J]. 中国药物警戒, 2009, 6(6): 332-334. |
| [11] |
尹庆和, 谭周飞, 肖俏霞, 等. 气相色谱法测定缝合针线中2-氯乙醇残留量[J]. 中国药事, 2013, 27(12): 1294-1297. |
| [12] |
吴振兴, 付步芳, 王书晗, 等. 气相色谱-质谱法测定人工晶状体中2-氯乙醇[J]. 理化检验:化学分册, 2015, 51(12): 1644-1647. |
| [13] |
栾琳, 杨锐, 汤龙, 等. 毛细管气相色谱法测定吐温80中氯乙醇、乙二醇、二甘醇的含量[J]. 药物分析杂志, 2010(10): 1869-1872. |
| [14] |
张波, 李太平. 毛细管气相色谱法测定空心胶囊中氯乙醇的残留量[J]. 中国药业, 2010, 19(21): 29-29. DOI:10.3969/j.issn.1006-4931.2010.21.019 |
| [15] |
ISO. Guide 35:2006 Reference Materials:General and statistical principles for certification[S]. 2006.
|
| [16] |
ISO. Guide 34:2009 General Requirements for the Competence of Reference Material Producers[S]. 2009.
|
 2017, Vol. 31
2017, Vol. 31 
