国家药品标准物质是指供国家药品标准中物理和化学测试及生物方法试验用,具有确定特性量值,用于校准设备、评价测量方法或者给供试药品赋值的材料或物质[1],是药品检定的重要物质基础,同时也是国家药品标准的物质基础,是控制药品质量必不可少的工具。药品标准物质不同于一般的药品,是执行国家药品标准的实物对照,是量值传递的安全载体,是国家颁布的一种计量标准品。根据《药品管理法》[2]和《药品注册管理办法》[3],中国药品生物制品检定所(后更名为中国食品药品检定研究院,以下简称“中检院”)负责对药品标准物质从原材料选择、制备方法、标定方法、标定结果、定值准确性、量值溯源、稳定性及分装与包装条件等资料进行全面技术审核,并做出可否作为国家药品标准物质的结论;中央机构编制委员会办公室《关于中国药品生物制品检定所更名的批复》[4](中央编办复字[2010]282号)规定了中检院的主要职责之(七)负责药品、医疗器械国家标准物质的研究、制备、标定、分发和管理工作;另外,2014年7月,国家食品药品监督管理总局(以下简称“总局”)颁布的《体外诊断试剂注册管理办法》[5]第二十五条规定,有国家标准品、参考品的产品应当使用国家标准品、参考品进行注册检验,中国食品药品检定研究院负责组织国家标准品、参考品的制备和标定工作。可见,中检院为国家药品、医疗器械及体外诊断试剂标准物质的合法提供单位,其标准物质的管理工作越来越引起社会的广泛关注[6]。
1 建立国家药品标准物质管理系统的必要性2016年12月底,中检院标准物质品种数已达3886种,主要分为生物标准品和参考品、化学对照品、对照药材/对照提取物、体外诊断试剂标准品、药用辅料对照品及药包材对照物质等。中检院标准物质与标准化管理中心负责标准物质管理工作,组织开展标准物质计划、研究、制备、标定、审核、分发和质量监测,并承担标准物质分包装制备生产、仓储和分发供应工作。
为实现国家药品标准物质的全过程信息化管理,该中心建立了“国家药品标准物质信息管理系统”,主要对国家药品标准物质计划立项、原料登记、分装、标定、报告审核、包装、入库、供应等全部流程进行信息化、自动化管理,及时掌握动态信息,为保障标准物质供应和质量提供现代化的管理手段。
2 国家药品标准物质管理系统的主要功能国家药品标准物质信息管理系统主要模块:生产策划平台、项目化管理、原料管理、制备管理、研制管理、专家审评管理、标准物质库管理、供应管理及保障供应综合数据平台等。通过这些模块,实现对标准物质从计划立项、研制生产到对外供应等环节的全程监控,从而确保标准物质供应。国家药品标准物质管理系统界面见图 1。
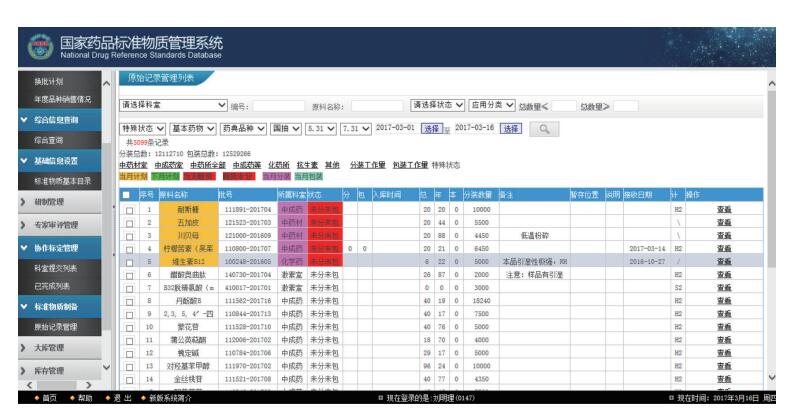
|
图 1 国家药品标准物质管理系统 |
生产策划平台是整个系统的启动机,承担着标准物质计划立项的重要任务。为了切实保障供应,特别是保障《中国药典》、国家评价性抽验及基本药物所需标准物质的生产供应,中心精心编制了标准物质生产计划,每年发布一次首批研制计划及两次换批研制计划;凡是列入计划的品种,无论是首批计划还是换批计划,都给予唯一计划号,根据计划号安排标准物质生产。原则上,只有纳入计划的品种才能进行制备,优先保障有计划号的品种供应,从而使标准物质的研制生产更有计划性和目的性。
2.2 项目化管理对所有标准物质都建立一份独立的档案,记录每个标准物质的编号、名称、所属科室、管理分类(必供、应供或可供[7])等信息,实时跟踪其工作状态和有关数据,如分装日期、研制报告提交日期、包装日期等。使每个品种的每个批次都有一份涵盖其完整生命周期的独立完整档案,实现了同一标准物质不同批次和不同环节的工作有据可查,做到了规范化实时管理。
2.3 原料管理标准物质研制始于一批合格的原料,对标准物质原料的管理至关重要。在生产策划平台中,对每一个列入计划的标准物质品种都赋予了计划号,研制科室将带有计划号的一批合格原料送到中心进行登记、填写原料信息;中心为原料建立唯一性标识号,这样的原料才能进入下一步的分装制备环节。从而确保原料满足研制计划及质量要求,这是国家药品标准物质研制工作的重要基础[8]。
2.4 制备管理为保证药品标准物质制备生产过程规范、统一,标准物质分包装工作采用电子化办公管理模式。借助标准物质信息管理系统,研制科室将分包装(卡)信息传输给标准物质制备人员,后者根据分包装卡的要求,按照相关规定进行制备;同时,填写制备过程原始记录,如分装日期、分装数量、包装日期及包装数量等[9]。为了及时保障供应,还要注意优先安排即将断货品种的分包装工作。通过系统操作,对有计划号的品种及即将断货的品种制定相关的分装和包装计划并按月排产,实时记录分包装进度与完成情况。
2.5 研制管理该模块用于上传研制申请、研制报告及定价申请,由标准物质标定人员填写有关信息,经审核通过后,由系统递交给中心逐级审签。其中,首批研制的标准物质需要上传上述3个文档;换批标准物质只需上传研制报告,从而解决了标准物质电子文档上传及审签的路径问题。
2.6 专家审评管理通常情况下,首批研制的标准物质需要请有关专家进行技术审评,审评通过后中心才会予以签发。系统单独建立了专家审评管理模块,中心工作人员登录该模块,将待审评的标准物质登记后,转至负责审评的专家名下,专家审评后在系统中填写意见,由工作人员综合专家提出的意见。该模块方便了专家审评过程管理,提高了工作效率。
2.7 标准物质库管理建立标准物质库管理模块, 进一步完善标准物质出入库管理,工作人员通过操作该系统,能够高效准确地完成标准物质成品的入库、出库以及科室人员领用标准物质工作的管理[10],确保标准物质库存数据的准确性。
2.8 供应管理首先根据用户需求生成订单,经财务确认收款后出库分发。以上过程都是在系统上完成,需要邮寄的通常采用EMS快递方式,工作人员将每一个快递包装的EMS号登记在系统中,以便于查询管理。
2.9 保障供应综合数据平台该平台是在项目化管理模块基础上建立的,系统随时追踪每个必供标准物质品种的供应情况,按照百分比计算总体保障供应率的趋势图及实时数据,进一步对各业务所及承担必供品种研制任务的科室保障供应情况进行了统计及展示。同时,该平台详细列出了当日断货品种,明确当前的生产阶段,与生产策划平台相结合,形象地展示了研制计划完成情况。具体情况见图 2、图 3、图 4。
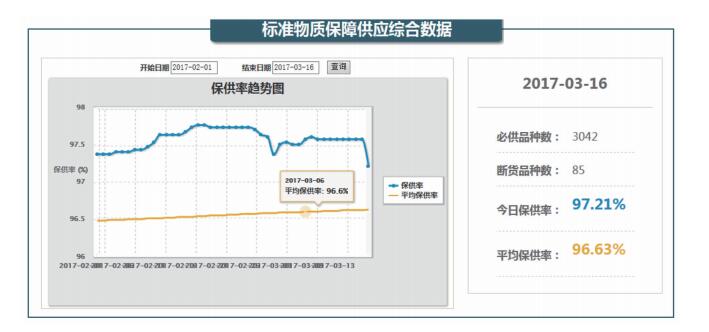
|
图 2 保障供应综合数据平台 |

|
图 3 各业务所的实时供应情况 |
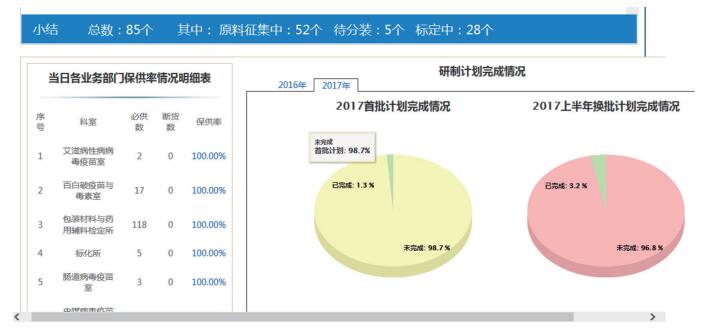
|
图 4 标准物质研制计划完成情况 |
在国家药品标准物质管理系统中除了有以上主要管理模快外,还有综合信息查询、决策支持及相关下载等模块,满足了标准物质基本信息查询及相关数据统计等工作需求。
3 支撑国家药品标准物质管理系统的信息化技术国家药品标准物质管理系统采用B/S架构,技术开发语言采用国际上通用的JAVA语言。采用客户端、服务器端、数据库构成的3层信息管理体系架构,从而提高了系统工作效率。在建设和管理过程中,系统符合国家食品药品监督管理总局信息化标准体系系统要求。为了确保信息安全,系统采取提供身份验证、访问控制等多角度保密措施,采用加密方式传送和存储系统中的重要信息,从而保证信息的安全性,预防可能存在的数据非法窃取。
4 结语国家药品标准物质管理系统的建立和应用,解决了标准物质管理过程中各个环节的数据流转问题,提升了中检院标准物质有关研制科室、管理部门、制备和供应部门的工作协同性,基本能满足管理工作需求。但是,在实际应用过程中还有许多地方需要进一步精细化。例如,应通过系统的延展,摸清全国有多少用户在使用标准物质、用户的具体情况、企业用户和药检所用户各占多少比例、预测年度标准物质需求量等等。系统整体上还有非常大的提升空间,还要结合标准物质管理进一步优化。
【致谢:该系统建设中得到中国食品药品检定研究院信息中心项目工作组的大力支持。在此一并致谢!】
| [1] |
中国药典: 四部[S]. 2015.
|
| [2] |
中华人民共和国主席令第45号药品管理法[S]. 2001.
|
| [3] |
国家食品药品监督管理总局. 国家食品药品监督管理局令第28号药品注册管理办法[S]. 2007.
|
| [4] |
中央机构编制委员会办公室. 中央编办复字[2010] 282关于中国药品生物制品检定所更名的批复[S]. 2010.
|
| [5] |
国家食品药品监督管理总局. 国家食品药品监督管理总局令第5号体外诊断试剂注册管理办法[S]. 2014.
|
| [6] |
曹丽梅, 马双成, 马玲云, 等. 中检所药品、医疗器械标准物质管理新模式-从分散多头管理走向集中统一管理[J]. 药物分析杂志, 2010, 30(10): 1993-1994. |
| [7] |
谢晶鑫, 刘明理. 国家药品标准物质的项目化管理模式研究[J]. 药品监管, 2015, 08: 1370-1373. |
| [8] |
王丹, 王昆, 马玲云. 国家药品标准物质原料的征集采购程序[J]. 中国药事, 2013, 11: 1164-1166. |
| [9] |
张琪, 谢丽华, 赵宗阁. 国家药品标准物质分包装管理工作现状与探讨[J]. 中国药事, 2011, 5: 470-473. |
| [10] |
肖丽华, 马双成, 宋玉娟, 等. 浅谈国家药品标准物质库的科学管理[J]. 中国药事, 2011, 8: 753-756. |
 2017, Vol. 31
2017, Vol. 31 
