风疹病毒(rubella virus,RV)是披膜病毒科风疹病毒属的成员, 为有包膜的单股正链RNA病毒[1-2]。风疹是由风疹病毒引起的急性上呼吸道传染病,一般症状较轻,预后良好。但妊娠期妇女感染风疹病毒可以引起流产、早产,并通过胎盘传染给胎儿,可导致先天性风疹综合征(congenital rubella syndrom,CRS)患儿出生,临床表现为先天性白内障、耳聋和心血管畸形等[3-6]。世界卫生组织(WHO)推荐使用风疹疫苗预防风疹和CRS,也推荐使用风疹疫苗联合其他疫苗控制和消除麻疹[7-8]。1992年,根据风疹流行病学及其他研究结果,国际风疹小组委员会将检测风疹IgG抗体的临界值定为10 IU·mL-1,可以不用接种风疹疫苗[9-10]。因此,对育龄妇女进行风疹病毒IgG抗体检测具有十分重要的意义。
目前国家食品药品监督管理总局批准的风疹病毒IgG抗体检测试剂盒主要是基于酶联免疫法、化学发光法和胶体金法的试剂盒,还包括时间分辨免疫荧光法和多重微珠流式免疫荧光法等其它方法的试剂盒[11-13]。风疹病毒IgG抗体检测试剂盒抽验工作只是针对酶联免疫法和化学发光法的试剂盒进行检测。
1 抽验产品各省(区、市)食品药品监管部门结合体外诊断试剂国家监督抽验工作统筹安排,在规定期限内完成抽样、样品寄送和信息录入等工作。本次抽验共收到17个批次风疹病毒IgG抗体检测试剂盒,包括13个批次酶联免疫法试剂盒,4个批次化学发光法试剂盒,涉及17家生产企业。抽验产品的相关信息,见表 1。
|
|
表 1 抽验试剂盒 |
风疹病毒IgG抗体国家参考品(批号:360005-201101),包括10份阳性参考品(P1~P10)、5份阴性参考品(N1~N5)、1份重复性参考品(R)和1份最低检测限参考品(L)。分别取国家参考品和企业参考品按照试剂盒说明书的方法,使用相应检测仪器(SpectraMax M2酶标仪和化学发光免疫分析仪),进行准确性、特异性、检测限和重复性项目检测。
3 结果 3.1 企业参考品的结果使用企业参考品检测,16批次产品的准确性(阳性参考品符合率)、特异性(阴性参考品符合率)、检测限和重复性项目结果都符合产品标准的要求,合格率为94.1%(16/17)。仅有1个批次化学发光类试剂盒的检测限项目不合格,原因是产品标准为“最低检出量:对稀释度为1:16的血清可检测为阳性或可疑”;但是说明书只有“阴性”和“阳性”的判定,没有“可疑”的判定,稀释度为1:16的血清结果根据说明书判定为阴性,所以不符合产品标准。抽验结果表明使用企业参考品评价试剂盒的性能,产品基本都能合格。
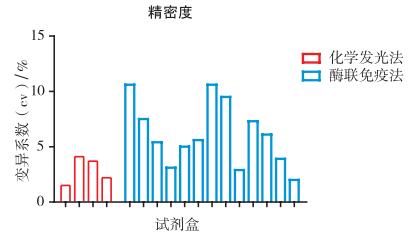
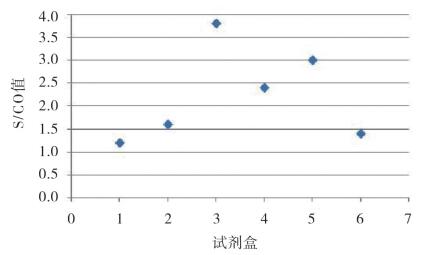
3.2 国家参考品的结果使用国家参考品检测,抽验产品的合格率仅为58.8%(10/17)。国家阳性参考品的结果均为阳性,重复性参考品的结果均为阳性且变异系数(CV)≤15.0%,结果见图 1。在不合格试剂盒中,其中1个批次试剂盒是检测限项目不合格,即国家检测限参考品的结果不是阳性;6个批次试剂盒是阴性参考品符合率项目不合格,包括国家阴性参考品N4为阳性或者N1、N3、N4和N5为阳性两种情况。统计N4的检测值与阳性临界值(Cutoff)的比值(即S/CO值),如果样本的S/CO值≥1,样本为阳性,结果见图 2。抽验结果表明使用国家参考品评价试剂盒的性能,产品的合格率明显下降。
|
图 1 国家参考品的精密度 |
|
图 2 国家阴性参考品N4的S/CO值 |
中国食品药品检定研究院在2011年研制了风疹病毒IgG抗体国家参考品。《风疹病毒IgG/IgG抗体检测试剂(盒)》的行业标准已于2015年7月1日正式实施。大部分企业在产品注册检测时并未采用国家参考品进行检验[14]。在使用国家参考品进行检测时,我们发现国家阴性参考品在部分试剂盒的结果为阳性以及最低检测限参考品的结果为可疑或阴性。而国家阴性参考品(N1~N5)是经过免疫荧光法、Western blot方法、酶联免疫法和化学发光微粒子免疫检测法等方法确认的风疹病毒IgG阴性的血清[15]。国家阴性参考品出现假阳性结果的原因:1)试剂盒的生产工艺存在着缺陷。① 包被抗原的因素:选择的包被抗原的特异性影响,试剂盒包被的抗原与其他类型抗体(如IgM、不同亚型的IgG)有交叉反应以及同种属病原体的交叉反应等;另外包被的基因工程抗原一般为融合蛋白,含有表达载体的一些序列,而且抗原经过大规模表达后需要经过破碎细胞、盐析、粒子交换等分离纯化步骤才能得到一定纯度的抗原,抗原中混有其他杂蛋白,血清中的抗体可能与这些杂蛋白发生反应产生假阳性。② 也有可能是标记抗体筛选不严格,其亲和力、抗体反应性以及特异性未充分验证,导致抗体结合力较高。2)在试剂盒分析性能研究中,正常参考人群的选择出现偏差,其阈值设定偏低,导致出现假阳性。国家最低检测限参考品的结果为可疑或阴性的原因:1)在试剂盒分析性能研究中,将正常参考人群的阈值设定较高,使临界阳性样本的结果为可疑或者阴性。2)试剂盒的生产工艺缺陷:包被抗原和标记抗体等因素影响。企业应该根据发现的问题,及时分析原因,完善和提高试剂盒的质量水平。
抽验中还发现企业提供的资料存在着一些问题,主要是说明书的问题较多:1)说明书的“检验方法”要求做阳性对照,但是在判定中未对阳性对照的结果做出相应的规定。而阳性对照作为质量控制之一,它的结果是试验有效性的前提,是决定试验是否成立的一个重要因素。2)说明书的“检验方法”要求预留空白孔/空白对照,读值时单波长测定OD值,但是并没有说明需要空白孔调零。3)说明书“检验结果的解释”提到“阴性对照的检测结果须为阴性,阳性对照的检测结果须为阳性,阳性校正液1#的OD值须介于临界校正液与阳性校正液2#之间,否则检测结果不可靠,不应出具检测报告”,而在产品注册标准中规定“4.6 OD值:试剂盒中的校正液检测OD值应在规定范围”,并严格规定了阴性校正液、临界校正液、阳性校正液1#和阳性校正液2#的OD值”,两者有一些差异,结果不一致时容易发生混淆。企业应补充或者进行相关内容的修改,使产品注册标准和说明书的内容保持一致。
根据抽验方案,部分试剂盒按照产品注册标准的要求使用企业参考品的结果出具检测报告。由于缺乏统一的评判标准,并不能对抽验的试剂盒质量做出客观的评价,建议在今后抽验工作中应使用国家参考品作为统一的标准。本次监督抽验涉及的抽样企业数量不多,而且没有进口试剂盒,建议今后应加大抽验力度,完善和优化抽样模式,使抽验结果可以覆盖该类产品的真实情况。笔者建议抽验结果可以成为有效的参考数据,将监督抽验作为一项延续性的工作,在不同年度通过连续跟踪的方式动态评价其质量变化,督促企业不断改进产品质量。
| [1] |
Tzeng WP, Xu J, Frey TK. Characterization of Cell Lines Stably Transfected with Rubella Virus Replicons[J]. Virology, 2012, 429(1): 29-36. DOI:10.1016/j.virol.2012.04.003 |
| [2] |
Mangala Prasad V, Willows SD, Fokine A, et al. Rubella Virus Capsid Protein Structure and its Role in Virus Assembly and Infection[J]. Proc Natl Acad Sci U S A, 2013, 110(50): 20105-10. DOI:10.1073/pnas.1316681110 |
| [3] |
Namuwulya P, Abernathy E. Phylogenetic Analysis of Rubella Viruses Identified in Uganda, 2003-2012[J]. J Med Virol, 2014, 86(12): 2107-2113. DOI:10.1002/jmv.23935 |
| [4] |
高冬梅, 李秀义, 蔡瑜, 等. 风疹病毒先天性感染与新生儿临床表现及T淋巴细胞亚群变化的相关性[J]. 中华实验和临床感染病杂志:电子版, 2013, 7(6): 838-842. |
| [5] |
Martínez-Quintana E, Castillo-Solórzano C, Torner N, et al. Congenital Rubella Syndrome:a Matter of Concern[J]. Rev Panam Salud Publica, 2015, 37(3): 179-186. |
| [6] |
Mazaba ML, Monze M, Babaniyi OA, et al. Characterization of Rubella Seronegative Females in the Zambian Blood Donor Community[J]. Front Public Health, 2015(3): 59. |
| [7] |
朱贞, 许文波. 风疹病毒的分子流行病学[J]. 中国计划免疫, 2007, 13(4): 399-406. |
| [8] |
Grant GB, Reef SE, Dabbagh A, et al. Global Progress Toward Rubella and Congenital Rubella Syndrome Control and Elimination, 2000-2014[J]. MMWR Morb Mortal Wkly Rep, 2015, 64(37): 1052-1055. DOI:10.15585/mmwr.mm6437a5 |
| [9] |
Skendzel LP. Rubella Immunity Defining the Level of Protective Antibody[J]. Am J Clin Pathol, 1996, 106(2): 170-174. DOI:10.1093/ajcp/106.2.170 |
| [10] |
Dimech W, Grangeot-Keros L, Vauloup-Fellous C. Standardization of Assays That Detect Anti-Rubella Virus IgG Antibodies[J]. Clin Microbiol Rev, 2016, 29(1): 163-174. DOI:10.1128/CMR.00045-15 |
| [11] |
安莉莎, 孙大光, 侯林浦, 等. 风疹病毒IgG抗体检测方法的研究及应用[J]. 中国计划生育学杂志, 2010(4): 209-211. |
| [12] |
Dimech W, Arachchi N, Cai J, et al. Investigation into Low-level Anti-rubella Virus IgG Results Reported by Commercial Immunoassays[J]. Clin Vaccine Immunol, 2013, 20(2): 255-261. DOI:10.1128/CVI.00603-12 |
| [13] |
谭玉华, 于婷, 李奕辉, 等. 时间分辨荧光免疫法风疹病毒IgG抗体定量测定试剂盒的研制与性能评价[J]. 国际检验医学杂志, 2014, 35(4): 472-474. |
| [14] |
杨振, 黄杰, 于婷, 等. 我国体外诊断试剂国家标准物质现状及对策分析[J]. 中国生物制品学杂志, 2015, 28(7): 765-771. |
| [15] |
黄杰, 刘志远, 孙彬裕, 等. 风疹病毒IgG抗体参考品的建立[J]. 药物分析杂志, 2013, 33(3): 493-497. |
 2017, Vol. 31
2017, Vol. 31 
