琥珀酸美托洛尔(Metoprolol Succinate)是一种选择性β1受体阻滞剂[1-2],是治疗高血压、冠心病、慢性心力衰竭和心律失常[3-7]的常用药物之一。其药理作用为选择性阻断β1受体,从而减慢心率、抑制心收缩率、降低自律性和延缓房室传导时间[8]。作为一种临床应用广泛的治疗高血压药物[9-11],琥珀酸美托洛尔有关物质及含量测定的方法在国外药典USP 34版与BP 2011版均有收载,而我国药典并未收载,建立药品含量和有关物质的检查方法对于控制药品质量是非常重要的[12]。本试验建立了琥珀酸美托洛尔的含量及有关物质的检查方法,为本品的质量控制提供了可靠的检测手段。
1 仪器与试药美国Agilent 1200高效液相色谱仪(VWD检测器,美国安捷伦公司);Mettler Toledo XS105电子天平(瑞士Mettler)。
琥珀酸美托洛尔对照品(USP批号:1441298,含量:99.8%);琥珀酸美托洛尔杂质A:(±)1-乙氨基-3-[4-(2-甲氧基乙基)苯氧基]-2-丙醇(USP批号:1441232,含量:100%);琥珀酸美托洛尔杂质B:(±)1-氯-2-羟基-3-[4-(2-甲氧基乙基)苯氧基]-丙烷(USP批号:1441243,含量:100%);琥珀酸美托洛尔杂质C:(±)4-[2-羟基-3-(1-甲基乙基)氨基丙氧基]苯甲醛(USP批号:1441254,含量:100%);琥珀酸美托洛尔杂质D:(±)N,N-双[2-羟基-3-[4-(2-甲氧基乙基)苯氧基]丙基](1-甲基乙基)胺(USP批号:1441265;含量:杂质D1:50%,杂质D2:50%);美托洛尔原料药(CTX Life Sciences公司提供,批号:120516、120517、120518)。乙腈为色谱纯,水为重蒸水,其余试剂均为分析纯。
2 方法与结果 2.1 色谱条件色谱柱:Agilent Zorbax SB-C8 column(150 mm × 4.6 mm,5μm);流动相为乙腈-十二烷基硫酸钠溶液(取十二烷基硫酸钠1.3 g,加0.1%磷酸溶液1000 mL使溶解)(40︰60);柱温为30 ℃;检测波长为223 nm。
2.2 溶液的制备 2.2.1 有关物质测定溶液取本品适量,用流动相溶解并稀释制成每1 mL中含1 mg溶液,作为供试品溶液。另取琥珀酸美托洛尔对照品适量,加流动相溶解并稀释制成每1 mL含1μg的溶液,作为对照品溶液。
2.2.2 含量测定溶液精密称取本品与琥珀酸美托洛尔对照品各20 mg,分别置25 mL量瓶中,加流动相溶解并稀释至刻度,各精密量取5 mL,分别置50 mL量瓶中,用流动相稀释至刻度,摇匀,制成供试品溶液和对照品溶液。
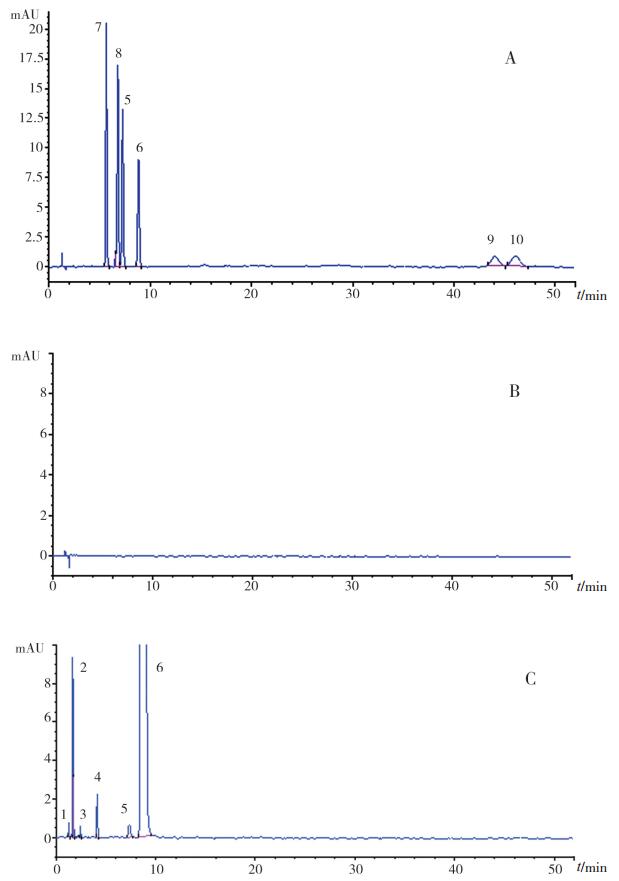
2.3 有关物质考察 2.3.1 系统适用性试验取琥珀酸美托洛尔、杂质A、杂质B、杂质C和杂质D对照品各适量,用流动相溶解并定量稀释制成每1 mL中分别含5 μg的混合溶液作为系统适用性溶液。取10μL注入液相色谱仪,杂质B峰和杂质C峰的分离度应大于2.5,杂质C峰和杂质A峰的分离度应大于1.5。色谱图见图 1A 。
|
图 1 高效液相色谱图 A.适用性溶液(7.杂质C峰;8.杂质B峰;5.杂质A峰;6.主成分峰;9.杂质D1峰;10.杂质D2峰);B.空白溶剂;C.供试品溶液(1、3、4.有关物质峰;2.琥珀酸峰;5.杂质A峰;6.主成分峰)。 |
取流动相10μL,按“2.1”节色谱条件进样,结果显示,流动相对测定无干扰。色谱图见图 1B 。
2.3.3 耐用性试验选用Agilent Zorbax SB-C8(150 mm×4.6 mm,5μm)、Phenomenex Luna (2) C8(150 mm×4.6 mm,5μm)、Waters Symmetry C8(150 mm×3.9 mm,5μm)色谱柱,分别注入系统适用性溶液10μL。结果显示,上述不同厂家的色谱柱均达到系统适用性要求。
2.3.4 检测限和定量限将适用性溶液逐级稀释,按“2.1”节色谱条件进样,取基线噪声的3倍值作为最低检测限,基线噪声的10倍值作为最小定量限。杂质A、杂质B、杂质C、杂质D检测限分别为0.6、0.6、0.5、10.3 ng。杂质A、杂质B、杂质C、杂质D定量限分别为1.7、1.8、1.6、30.1 ng。
2.3.5 破坏性试验取本品3份,各约50 mg,精密称定,分别置50 mL量瓶中,分别加1.0 mol·mL-1盐酸溶液10 mL放置2 h、加1.0 mol·mL-1氢氧化钠溶液10 mL放置2 h、加10%过氧化氢2 mL放置1 h,进行强酸、强碱和氧化破坏;另取本品2份,各约50 mg,精密称定,分别置50 mL量瓶中,置光照(4500±500)Lx条件下照射24 h和120 ℃条件下加热1 h进行光照和高温破坏。分别取上述5种破坏后溶液,加入流动相至刻度,摇匀,分别取10 μL,按“2.1”节色谱条件进样。结果显示,各条件下的降解产物与主成分均能很好分离,证实建立的有关物质方法可行。
2.3.6 有关物质测定取本品适量,用流动相溶解并稀释制成每1 mL中含1 mg溶液,作为供试品溶液。另取琥珀酸美托洛尔对照品适量,加流动相溶解并稀释制成每1 mL中含1μg的溶液,作为对照品溶液。照“2.1”节色谱条件测定,精密量取供试品溶液与对照品溶液各10μL,分别注入液相色谱仪,记录色谱图。在供试品溶液的色谱图中,扣除溶剂峰和琥珀酸峰,如有与杂质A、杂质B、杂质C、杂质D保留时间一致的峰及其他单个杂质,以琥珀酸美托洛尔为对照品,按外标法以峰面积计算,均不得过0.10%,杂质总和不得过0.50%。有关物质见图 1C ,有关物质测定结果见表 2。
|
|
表 2 琥珀酸美托洛尔的有关物质及含量测定结果(n=2) |
取琥珀酸美托洛尔对照品约800 mg,精密称定,置100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,作为标准贮备液。分别精密量取该溶液0.2、0.5、0.8、1.0、1.5、2.0 mL,置100 mL量瓶中,用流动相稀释至刻度,摇匀,分别取上述溶液10μL,按“2.1”节色谱条件进样,记录峰面积,以美托洛尔峰面积(Y)为纵坐标,以美托洛尔进样浓度(X,μg·mL-1)为横坐标,绘制标准曲线,得美托洛尔线性方程:
| $ Y=19.144X-0.9583 \;\;r=1.0000 $ |
美托洛尔浓度在0.01641~0.1641μg·mL-1与峰面积呈良好的线性关系。
2.4.2 溶液稳定性取批号为120516的供试品溶液,分别于配制后0、2、4、8、12、16、24 h进样,记录液相色谱图,结果不同时间色谱峰面积一致,RSD为0.2%,表明供试品溶液在室温条件下放置24 h内稳定。
2.4.3 仪器精密度试验取琥珀酸美托洛尔对照品溶液,连续重复进样6次,结果RSD为0.1%。
2.4.4 重复性试验取批号为120516的样品约16、20、各3份,按“2.2.2”节方法制成供试品溶液,进样10μL,测定含量,结果RSD为0.4%,表明本方法重复性好。
2.4.5 回收率试验取批号为120516的样品约8、10、各3份,分别置9个25 mL量瓶中,加入一定量琥珀酸美托洛尔对照品8、10、12 mg,各3份,按“2.2.2”节方法分别配制成低、中、高3种不同浓度的溶液(80%、100%、120%),各3份,分别取上述溶液10μL,注入液相色谱仪,以外标法测定并计算含量,平均回收率与RSD值分别为100.4%和0.9%。结果见表 1。
|
|
表 1 回收率试验结果 |
取本品3批,按“2.2.2”节方法制成供试品溶液,按“2.1”节色谱条件测定,外标法计算含量,测定结果见表 2。
3 讨论 3.1 主要有关物质的确定目前琥珀酸美托洛尔尚未被《中国药典》收录,在美国药典(USP 34)和英国药典(BP 2011)中共涉及到13种有关物质。其中,美国药典中列出4种,分别命名为USP-A、USP-B、USP-C、USP-D[13];英国药典中则列出12种,分别命名为BP-A、BP-B、BP-C…(以此类推)[14],与美国药典重复3种[15]。美国药典(USP 34)采用的色谱系统为以十二烷基硫酸钠溶液-乙腈(60:40)为流动相,C8色谱柱,检测波长为223 nm,并针对USP-A、USP-B、USP-C、USP-D配制系统适用性试验溶液规定了杂质间的分离度,能较准确地对USP-A、USP-B、USP-C、USP-D这4种杂质进行准确定位与计算。英国药典(BP 2011)采用的色谱系统为以醋酸盐缓冲液(取醋酸铵3.9 g,加水810 mL溶解后,加三乙胺2.0 mL,冰醋酸10.0 mL,磷酸3.0 mL和乙腈146 mL,混匀)为流动相,C18色谱柱,检测波长为280 nm,采用自身对照法计算未配制系统适用性试验溶液,对杂质的定位和计算效果较差。综合考虑美国药典(USP 34)对杂质的定位与计算较合理准确,本研究参照美国药典USP 34版将主要有关物质USP-A、USP-B、USP-C、USP-D确定为检测项目。
3.2 检测波长的确定对琥珀酸美托洛尔、杂质A、杂质B、杂质C及杂质D进行PDA检测,结果显示,均在波长223 nm附近有最大吸收。在破坏试验中,各降解产物均在223 nm波长处有较大吸收,各降解产物能够达到有效分离和检测,故选择223 nm作为检测波长。
| [1] |
蔡其云, 陈莉. β受体阻滞剂在常见几种心血管疾病中的应用[J]. 安徽医药, 2009, 13(8): 867-869. |
| [2] |
中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. B肾上腺素能受体阻滞剂在心血管疾病应用专家共识[J]. 中华心血管病杂志, 2009, 37(3): 195-209. |
| [3] |
张峰. 琥珀酸美托洛尔缓释片治疗原发性高血压60例分析[J]. 安徽医药, 2011, 15(3): 362-363. |
| [4] |
徐宁, 易月婵, 李勤. 琥珀酸美托洛尔缓释片在高龄老年冠心病患者中的应用[J]. 岭南心血管病杂志, 2011, 17(6): 500-502. |
| [5] |
施红. 琥珀酸美托洛尔治疗慢性心力衰竭的效果分析[J]. 药物与临床, 2011, 8(33): 80-81. |
| [6] |
王丙文, 于军会, 周建岭. 老年急性心肌梗死早期使用琥珀酸美托洛尔缓释片的疗效分析[J]. 临床合理用药, 2009, 2(24): 3-5. DOI:10.3969/j.issn.1674-3296.2009.24.002 |
| [7] |
陈新谦, 金有豫, 汤光. 新编药物学[M]. 第17版.北京: 人民卫生出版社, 2011: 356.
|
| [8] |
萧爽. 美托洛尔[J]. 中国医院药学杂志, 1994, 14(5): 285-287. |
| [9] |
周娜, 光雪峰. 琥珀酸美托洛尔片在高血压病治疗中的优势[J]. 中国医药导刊, 2008, 10(6): 861-868. |
| [10] |
姜志荣, 马红婷, 张莉. 美托洛尔治疗高血压临床观察[J]. 中国高血压杂志, 1994, 2(2): 125-126. |
| [11] |
胡贞栓, 李奇成, 饶文康, 等. 美托洛尔逆转高血压性左心室肥厚的效应[J]. 中国高血压杂志, 1994, 2(2): 126-127. |
| [12] |
高文学, 高蕾, 闫美兴, 等. 美托洛尔临床应用的安全性[J]. 中国临床医生, 2012, 40(3): 38-41. |
| [13] |
美国药典[S]. 2011: 3508-3509.
|
| [14] |
英国药典[S]. 2011: 1452-1454.
|
| [15] |
樊琳静, 闫明, 陈灵娟, 等. 琥珀酸美托洛尔有关物质的结构分析[J]. 河北师范大学学报, 2012, 36(3): 269-274. |
 2017, Vol. 31
2017, Vol. 31 