我国中药资源达12万余种,其中药用动物近2215种,约占全部中药资源的18%。动物药在我国应用历史悠久,有资源广、活性强、疗效高、效益大的特点,在我国中药材市场有着巨大潜力和重要地位,在临床上的作用和功效也无法替代。
《中国药典》2015年版收录了94种动物药,其中《中国药典》一部[1]正文收载46种,质量控制方法包括:LC-MS、PCR、HPLC、TLC等方法,《中国药典》四部[2]附录收载48种动物药,仅有药材来源,无具体质量控制项目。《中国药典》2015年版动物类药材质量控制技术及项目情况见表 1。
|
|
表 1 《中国药典》2015年版动物类药材质量控制技术及项目情况 |
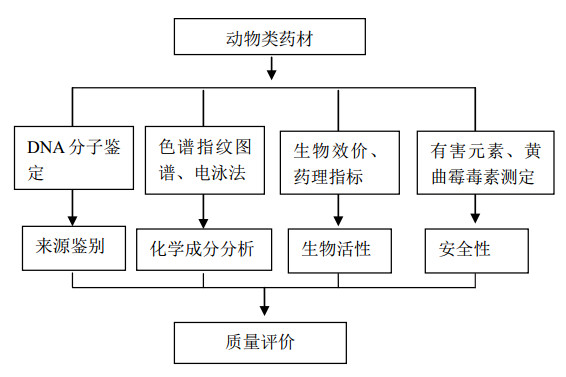
由于动物药材来源多、品种多,因此较为混乱,而且大部分为贵重紧缺药材,通常多以粉末、中成药等形式入药,给动物药材的准确鉴定带来了极大的困难,如外部形态不完整或被破坏、混伪品增多、近缘种鉴定困难等;因此,药用动物以及动物药的品种鉴定与质量评价工作急需现代技术的介入和支持。随着现代科学技术的发展,凝胶电泳、术、液相质谱联用技术、蛋白组学、生物测定等方法在动物药材的鉴定中发挥了重要作用。本文在对《中国药典》2015版动物类药材质量标准技术进行概括的基础上,总结了近十年来国内动物类药材品种鉴定与质量评价研究方法,探讨动物类药材鉴定及质量评价的思路,见图 1。本文针对一些新技术和方法的应用进行了综述。
|
图 1 动物类药材品种鉴定与质量评价研究方法 |
DNA分子鉴定技术不仅能对有形的动物药材整体、破碎部分器官及组织进行准确的鉴定;而且,还可以对以动物粉末、体液、分泌物和排泄物入药的生药及制剂进行有效的真伪鉴定、纯度检查与质量评价。目前,该方法在《中国药典》动物药材鉴定中,已经发挥重要作用。
动物线粒体基因组由于具有长度较小、易于PCR扩增和测序、进化速率快、已知物种线粒体基因组数据丰富、基因组各基因的定位和功能已经研究的比较清楚等优势,成为物种的比较遗传学与系统进化学研究的理想工具。典型的后生动物线粒体基因组序列全长一般为14~20 kb,除少数种类以外都包含有37个基因,即13个蛋白质编码基因(protein-coding gene,PCG),22个转运RNA基因(tRNA)和2个核糖体RNA基因(16 SrRNA和12 SrRNA)[3]; 其中13个蛋白质编码基因,包括:① 2个ATP合成酶亚基(atp6和atp8);② 3个细胞色素C氧化酶亚基基因(cox1-3);③ 1个细胞色素b脱氧辅基基因(Cyt b); ④ 7个NADH还原酶复合体的亚单位基因(nad1-6和4 L)[4]。此外,还有一段富含AT的非编码区(A+T-rich reigion),调控基因组转录和复制,又称为替代环(D-loop)或控制区(control-reigion)。目前,动物类药材DNA研究则是基于线粒体不同的基因片段,用各种引物,进行PCR扩增后,再进行鉴别分析。
1.1.2 基于线粒体12S rRNA基因序列的鉴别研究由于线粒体12S rRNA基因的进化速率较快,不同物种间序列差异大,有利于设计针对目标物种的高特异性引物,加上扩增该基因的稳定性和可重复性好,可以用来作为生物物种种属的鉴定,并在动物药材的分子鉴定中得到应用。利用该基因序列对蛇类药材进行鉴定的报道较多,主要集中在乌梢蛇、金钱白花蛇、蕲蛇及其混淆品的鉴定,如根据乌梢蛇及10种常见混淆品线粒体12S rRNA基因序列,设计一对专用于乌梢蛇的鉴别引物,所设计的鉴别引物对正品乌梢蛇有高度的特异性[5]。运用分子标记技术分别从药材蛇胆的胆衣和胆汁、原动物棕黑锦蛇的肌肉和胆汁中提取DNA,经PCR扩增得到约400 bp的12S rRNA基因片段,并对该基因片段进行测序研究。结果表明,DNA分子标记技术可用于中药材蛇胆和胆汁的鉴定,提示该技术也可用于其他动物分泌物类型药材的鉴别[6]。有学者从乌龟和其他20种产地为中国或东南亚国家的龟类组织材料中提取DNA,扩增约110 bp的线粒体12S rRNA基因片段并进行序列分析,构建了21种龟类的12S rRNA基因片段序列数据库。序列比较的结果表明乌龟与其他20种龟类的这段序列均有差别[7]。基于此设计一对专用于鉴定中药材龟甲原动物乌龟的鉴别引物,对龟甲药材进行了分子鉴定[8]。从5种海马药材中提取DNA,用PCR技术扩增约450 bp的12S rRNA基因片段和约490 bp的细胞色素b基因片段。结果表明,用DNA序列分析方法得到的分子遗传标记可以鉴别所有5种海马[9]。
1.1.3 基于线粒体Cyt b基因序列的鉴别研究Cyt b基因是动物线粒体上一个编码蛋白质的基因,有一定的保守性,根据蛇类药材Cyt b基因片段序列的分析,表明这种在种内个体间的序列差异很小,而种间的序列差异却较大的DNA片段,正是物种鉴别的理想标记。因此,Cyt b基因片段的DNA序列是鉴别蛇类药材原动物种类的一种良好分子标记[10]。设计金钱白花蛇PCR鉴别的一对高度特异性引物,可以对金钱白花蛇及其伪品进行Cyt b基因片段序列分析和PCR鉴别研究。结果表明,在对金钱白花蛇的PCR鉴别中,该对引物可以100%检出金钱白花蛇,并能在混合的药材粉末中检测出被检样品中是否含有金钱白花蛇组分[11-12]。以同样的原理,利用Cyt b基因对蕲蛇药材及其市场收集样品进行了序列测定和分析。结果表明,Cyt b基因序列是一种鉴别蕲蛇药材与其混淆品较好的分子遗传标记[13]。类似的研究还有鸡内金及其伪品的分子鉴别研究,所设计的引物只扩增家鸡DNA,而不扩增其他动物DNA[14]。利用Cyt b基因对鹿类中药材进行分子鉴定研究已见诸多报道。在对鹿类中药材的正品原动物梅花鹿、马鹿及其混伪品原动物的Cyt b基因全序列分析的基础上,设计一对专用于鉴定正品鹿类药材的位点特异性鉴别引物,建立鹿类中药材鹿茸、鹿鞭、鹿筋、鹿胎的DNA分子标记鉴定方法[15-16]。建立的位点特异性PCR方法,能将正品鹿茸与其他近源种鹿茸药材鉴别开来,具有较高的特异性、重复性,可广泛应用于鹿类药材的鉴别[17-18]。
1.1.4 基于线粒体COⅠ基因序列的鉴别研究刘晓帆等[19-20]利用COⅠ基因对水蛭、蚂蟥、柳叶蚂蟥及常见混伪品、乌龟及常见混伪品进行分子鉴定。全国范围内收集水蛭、蚂蟥、柳叶蚂蝗的正品及其混伪品5种,收集龟甲的正品及其混伪品8种,提取DNA,得到其COⅠ序列。变异位点分析,水蛭的正品来源蚂蟥、水蛭、柳叶蚂蟥与其混伪品种间存在较多变异位点。由所构建的系统聚类树图可以看出,同属聚在一起,且各物种又形成相对独立的支,基于COⅠ序列的DNA条形码技术可以很好地鉴定水蛭及其混伪品。龟甲的正品来源乌龟与其混伪品种间存在较多变异位点。由所构建的系统聚类树图可以看出,同属聚在一起,且各物种又形成相对独立的支。基于COⅠ序列的DNA条形码技术可以很好地鉴定龟甲及其混伪品。测定5个不同居群广地龙的线粒体细胞色素酶亚单位COⅠ和16S rRNA基因序列[21],结果COⅠ变异位点、信息位点均高于16S rRNA,COⅠ基因无插入和缺失,16S rRNA存在4个插入和缺失。COⅠ和16S rRNA序列种间遗传距离均明显大于种内,COⅠ和16S rRNA基因均能将广地龙从其他地龙或蚯蚓物种鉴别开来。获得的广地龙COⅠ和16S rRNA序列可为动物性中药材地龙的分子水平鉴定提供参考。长春中医药大学与中国药用植物研究所合作[22],选取药典中45个动物药的51种原动物,考察样品中线粒体COⅠ序列的种内种间变异情况、barcodinggap、鉴定成功率等方面,进而证明COⅠ序列鉴定动物药的有效性和准确性。结果表明,种间变异最小值远大于种内变异最大值,barcodinggap图显示种间变异和种内变异重合较少,鉴定成功率较高,除节肢动物门外,在物种水平和属水平上,鉴定成功率均为100%,所构建的动物药及其混伪品的N J树能很好地区分正品来源与其混伪品。因此,COⅠ序列可作为条形码适用于药典中动物药品种的鉴定。
1.2 高效毛细管电泳指纹图谱技术动物药材成分大多为蛋白质、多糖、核苷等大类化学成分,根据其化学成分的特点,辽宁中医药大学王成芳、李峰等[23],采用高效毛细管电泳法(HPCE)对蛤蚧、蕲蛇、土鳖虫、地龙、僵蚕等品种,测定药材各样品指纹图谱,建立各药材的特征指纹图谱,并计算各药材共有模式的相似度。通过比较各药材样品的相似度发现,单一来源药材中除蛤蚧[24]有一个样品外,大多数药材样品的相似度达到或接近0.9[25],表明各地药材的品种具有相似性;其中土鳖虫药材均为地鳖[26]。多来源药材中,地龙药材各样品的相似度差异较大,与该药材的多来源相吻合;广地龙与沪地龙药材样品比较,广地龙各样品相似度的一致性高于沪地龙,这也与广地龙来源单一相吻合。10批僵蚕药材的相似度在0. 959~0. 997, 2种商品规格具有相似性,炮制品间的差异较生品间的稍大,该方法具有良好的精密度和分离效果,可作为僵蚕品种鉴定与质量控制方法[27]。李峰等[28]建立乌梢蛇药材的HPCE指纹图谱,通过与共有模式比较,10批乌梢蛇药材的相似度在0.865~0.978, 认为该方法可有效用于乌梢蛇药材质量评价。陈昭等[29]采用HPCE法,结合药效学试验,对土鳖虫镇痛作用机理与物质基础进行了初步探索,确定尿囊素和氯氮卓这2个化合物作为指标性成分,该方法以疗效为导向,为动物药的研究及质量控制提供了借鉴。
1.3 蛋白质SDS-PAGE电泳技术SDS-PAGE电泳技术在测定蛋白质分子量、检测特异蛋白等方面具有操作简单、重复性好的优点,因此,在动物类药材分析中具有一定应用。高世杰等[30]用TRICINE-SDS-PAGE系统对全蝎蛋白提取液进行电泳,用Quantity One软件确定各谱带对应的蛋白质分子量,可以较好地进行全蝎粉可溶性蛋白的分离,电泳结束后再通过相应软件处理后可得到各蛋白的分子量,通过比较谱带位置及分子量的大小,即可实现野生全蝎的真伪鉴别。吴文如等[31]探讨聚丙烯酰胺凝胶电泳技术对地龙药材进行鉴别的可行性,电泳图谱中广地龙在分子质量66. 2~14. 4 ku之间存在5条清晰稳定的条带,可初步认定其为广地龙的特征鉴别条带。不同品种的地龙在蛋白质电泳图谱谱型和谱带的强弱、蛋白质相对含量上均有一定的差异,地龙鲜品和干品在蛋白质谱带的强弱上有一定差异。陈振江等[32]用SDS — PAGE测定人工牛黄、鹿蹄筋、蝮蛇、乌梢蛇、金钱白花蛇及其伪品的主要蛋白质分子量,可为蛇类药材、人工牛黄、鹿蹄筋及其制剂的生产、质量控制提供参考。王晶娟等[33]采用水提与盐析法获得全蝎蛋白药效组分,考马斯亮蓝法测定蛋白药效组分的蛋白质含量,SDS-PAGE法和Alpha Ease FC 4.0.0软件测定全蝎蛋白药效组分的蛋白质相对分子质量,能得到较好的全蝎蛋白药效组分的10条电泳谱带,是全蝎蛋白药效组分的特征谱带,可用于全蝎蛋白药效组分的鉴别。但是,由于SDS-PAGE测定蛋白质相对误差较大、分辨率不高,更重要的是很难获得翻译后修饰蛋白质分子量的准确信息,因此逐渐被蛋白质芯片技术、色谱-质谱联用技术等所替代。
1.4 X射线衍射Fourier谱鉴定技术X射线衍射Fourier谱作为一种光谱技术,近年来不断有研究报道在中药材鉴定领域的应用。王丽娟等[34]用粉末X射线衍射Fourier谱法对鹿角、麋鹿角及鹿角伪品牛腿骨进行比较鉴别,结果动物角类药材含有大量无机成分,利用X射线衍射可以得到较为尖锐的X射线衍射峰,根据其几何拓扑图形及特征标记峰值的差异可对各角类药材进行鉴别比较。李兰燕等[35]通过对1个广地龙药材对照品、4个广地龙中药材进行实验分析,获得了广地龙的标准X射线衍射Fourier图谱及特征标记峰值,表明此法可用于中药材广地龙的鉴定。王树春等对熊胆[37]、全蝎[38]、鹿茸[39]、蛤蚧[40]等动物类中药材均用X射线衍射Fourier谱进行鉴定,结果均获得了各类药材的X射线衍射Fourier图谱及特征标记峰值,为X射线衍射Fourier谱应用于动物类中药材的鉴定作了大量基础工作,积累了丰富的数据。
1.5 生物活性测定技术生物检定是根据药物的生物效应或功能主治,利用整体动物、离体组织、器官、细胞以及微生物和相关生物因子等为实验系统,以检测药物生物活性(含药效和毒性)的一种方法。从药物质控模式的适用性来看,生物检定技术由于与安全性与有效性关联密切,往往比化学成分检测更具实际价值[41]。刘涛等[42]建立基于体外酶活性法的地龙质量标准,采用纤维蛋白原平板法,以尿激酶为参照,测定地龙蛋白酶的活性,该法可快速、简便、准确地测定地龙所含蛋白酶的活性,可用于地龙质量控制。肖凌等将生物检定技术应用于水蛭抗凝血活性的测定,对宽体金线蛭、日本医蛭、菲牛蛭、棒纹牛蛭的抗凝活性进行测定,4种水蛭APTT法的量效关系曲线与肝素的量效关系曲线类似,以肝素钠作为标准品,米用生物检定技术APTT法测定水蛭等的抗凝活性是可行的方法。APTT值可以全面反映水蛭的抗凝血作用,测定结果对临床使用更具指导意义[43]。生物检定技术应用于中药质量评价,是对现有中药质量标准控制方法良好的补充。
1.6 色谱指纹图谱、质谱技术色谱指纹图谱或化学成分谱,用化学计量学方法关联相关的检测数据,HPLC指纹图谱上的化学指纹峰经化学计量学、生物信息学和计算机模拟等方法进行处理,确定可用于样品质量控制的模式。肖云芝等[44]采用HPLC-DAD方法结合聚类分析和主成分分析,建立了12个产地鳖甲药材样品指纹图谱共有模式,经主成分分析,共提取出3个主成分,其累积贡献率达82.31%,用SPSS软件对鳖甲药材的指纹图谱进行主成分分析及聚类分析,所建立的模式识别方法操作简便,统计结果具有可靠性,对鳖甲药材化学计量学分类及其质量评价提供有效参考。王欣丽等[45]通过0PA-FMOC在线自动衍生化,建立了土鳖虫及其混淆品HPLC指纹图谱并计算相似度,根据SPSS聚类分析结果,将其分为2类。所建立的土鳖虫HPLC指纹图谱为土鳖虫的质量控制提供了科学依据。姬诚[46]采用HPLC建立评价蟾酥饮片质量优劣的指纹图谱分析方法,方法精密度、重现性均良好,各产地样品的相似度大于0.95, 可较全面地反映蟾酥饮片的内在质量,可用于蟾酥饮片的质量控制。
依照动物药多含蛋白质与多肽类成分的特点,选择特异性强、灵敏高的现代化质谱分析技术,开展相应的基础研究,并最终阐明动物药材的药效物质基础,以达到质量评价的目的,是动物类中药材质量评价的发展方向。刘海洋等[47]利用柱前衍生化GC-MS技术对蜂蜡中成分进行分析,利用指纹图谱对14个来源不同的蜂蜡样品进行鉴定分析,随后采用主成分分析找出引起质量差异的化合物,建立简单快捷的质量评价方法,蜂蜡质量标准应该在控制总烷酸类含量的同时,也控制烷烃及游离烷酸的含量。张晗星等[48]用定量蛋白质组学方法iTRAQ分析技术对冬虫夏草不同生长发育阶段的差异蛋白质组进行比较。对鉴定蛋白质数据进行了主成分分析,冬虫夏草菌核部位的蛋白到子座部位的蛋白呈现由寄主幼虫蛋白向真菌蛋白发育过渡的聚类关系,IK-均值聚类和Gene Ontology注释分析,提供了冬虫夏草成熟过程中能量代谢通路的变化趋势,以及与真菌侵染昆虫和有性生殖相关蛋白质信息。研究结果为理解寄主昆虫对冬虫夏草功能的潜在贡献、子实体形成和发育的分子机制提供借鉴,并为蛋白质组作为冬虫夏草质量标准提供了科学参考。
2 质量评价思路的探讨 2.1 概述动物药材其主要成分大多为蛋白质、多糖、核苷等,研究难度较大,基础相对薄弱,致使动物药材应用中品种混乱,且很难将其各部分成分与药材的功能主治一一对应,进行动物药材的质量评价。如何能结合动物药材的特点,寻找出符合当前动物药材应用实际的品种鉴定与质量检测的方法与指标,是解决动物药材品质评价问题的关键。
2.2 基因分子鉴定原动物及药材来源目前,多数动物药材的来源动物靠人工饲养,动物形态外观较易观察,在原动物传统物种分类基础上,结合基因分子水平进行系统发育进化、遗传变异、系统分类等方面的研究,寻找不同物种间基因分子水平的差异,通过差异设计不同的PCR方法,以达到鉴定目的。采用DNA分子鉴定技术,解决药材质量真与假的问题。
2.3 化学成分研究结合生物指标大多数动物类药材的功能与主治明确,化学成分主要为蛋白质、核苷等,药效即表现为蛋白质的活性,生物效价则是评价药效的直观表现。因此,直接用生物效价测定结果或药理指标,来指导色谱分离、分析化学成分,使化学成分研究体现药效物质基础,引入色谱反映化学成分与生物效价相互关联的概念,利用统计学处理方法,找到反映药效的标志性蛋白成分,作为质量控制的指标。采用色谱法结合生物测定法,解决药材质量优与劣的问题。
2.4 安全性评价目前,对外源性的物质影响中药安全性的问题关注颇多,如有害重金属元素、农药残留,以及二氧化硫、黄曲霉毒素等。动物药材的特点主要是有害元素的量超标,李锋等[49-50]测定10种常用动物类药材,结果显示,各药材样品的5种有害元素含量均不同程度超出2010版《中国药典》的限量要求。如地龙药材样品5种有害元素含量均超出标准;水蛭药材仅有一半样品的铅含量符合标准,其余样品的5种有害元素含量也都超出标准;全蝎药材的镉、铜含量超出标准;蕲蛇药材有一半样品的汞含量超出标准。由此可见,动物药材中有害元素超标导致的药材安全隐患值得关注。
3 结论动物药的安全有效质量控制技术有待进一步摸索,相关质量标准还不够完善[51],目前植物药研究思路不符合动物类药材自身的特点,现代各类生物技术如生化分离、膜分离、蛋白质组学、蛋白质鉴定标记分析、生物芯片、发酵和免疫等在动物药研究中的应用,将有望在动物药质量评价方面获得重要突破。
| [1] |
中国药典: 一部[S]. 2015.
|
| [2] |
中国药典: 四部[S]. 2015: 418-424.
|
| [3] |
Boore J. L., Brown W.M. Big Trees from Little Genomes:Mitochondrial Gene Order as A Phylogenetic Tool[J]. Current Opinion in Genetics & Development, 1998, 8(6): 668-674. |
| [4] |
Da Fonseca, Rute R. The Adaptive Evolution of the Mammalian Mitochondrial Genome[J]. Bmc Genomics, 2008, 9(1): 119. DOI:10.1186/1471-2164-9-119 |
| [5] |
唐晓晶, 冯成强, 黄璐琦, 等. 高特异性PCR方法鉴别乌梢蛇及其混淆品[J]. 中国药学杂志, 2007, 42(5): 3331. |
| [6] |
刘向华, 王义权, 刘忠权, 等. 中药材蛇胆的DNA分子标记鉴定研究[J]. 药学学报, 2001, 36(3): 2291. |
| [7] |
吴平, 周开亚, 徐珞珊, 等. 中药材龟甲的分子鉴定研究[J]. 药学学报, 1998, 33(4): 3041. |
| [8] |
刘中权, 王义权, 周开亚, 等. 中药材龟甲及原动物的高特异性PCR鉴定研究[J]. 药学学报, 1999, 34(12): 9411. |
| [9] |
吴平, 周开亚, 张朝晖, 等. 海马类药材的分子遗传标记鉴定研究[J]. 药学学报, 1998, 33(3): 2261. |
| [10] |
王义权, 周开亚, 徐珞珊, 等. 中药材乌梢蛇及其混淆品的DNA序列分析鉴别[J]. 药学学报, 1999, 34(1): 671. |
| [11] |
王义权, 周开亚, 徐珞珊, 等. 金钱白花蛇及其伪品的Cytb基因片段序列分析和PCR鉴别研究[J]. 药学学报, 1998, 33(12): 9411. |
| [12] |
冯成强, 唐晓晶, 黄璐琦, 等. 金钱白花蛇及其混淆品高特异性PCR的鉴别[J]. 中国中药杂志, 2006, 31(13): 10501. |
| [13] |
宋文成, 宋社吾, 刘道芳, 等. 蕲蛇药材及其市售混淆品的Cytb基因序列与分析[J]. 中草药, 2006, 37(12): 18621. |
| [14] |
曲萌, 崔继春, 董志恒, 等. 鸡内金的分子鉴定研究[J]. 中国中药杂志, 2009, 34(24): 31921. |
| [15] |
刘向华, 王义权, 周开亚, 等. 鹿类中药材的位点特异性PCR鉴定研究[J]. 药学学报, 2001, 36(8): 6311. |
| [16] |
傅文, 唐双焱, 陈永久, 等. 鹿属动物线粒体DNA序列测定的研究[J]. 中国药学杂志, 2000, 35(12): 8031. |
| [17] |
王学勇, 刘春生, 张蓉, 等. 位点特异性PCR方法的建立及对近源种鹿茸药材的鉴别研究[J]. 中国中药杂志, 2009, 34(23): 30131. |
| [18] |
唐双焱, 傅文, 陈永久, 等. 中药材鹿鞭的分子鉴定研究[J]. 中国中药杂志, 2002, 27(8): 5731. |
| [19] |
刘晓帆, 刘春生, 杨瑶珺, 等. 基于COI基因的龟甲及其混伪品的DNA条形码研究[J]. 中国中药杂志, 2013(7): 947-950. |
| [20] |
刘晓帆, 刘春生, 杨瑶珺, 等. 基于COI基因的水蛭及其混伪品的DNA条形码研究[J]. 北京中医药大学学报, 2013(1): 63-66. |
| [21] |
韦健红, 李薇, 吴文如, 等. 基于COⅠ与16S rRNA基因对广地龙的DNA分子鉴定研究[J]. 中国药房, 2012, 35: 3274-3278. DOI:10.6039/j.issn.1001-0408.2012.35.04 |
| [22] |
张辉, 陈士林, 姚辉, 等. 基于COI序列的DNA条形码在药典动物药品种鉴定中的应用[C]//中国药学会中药和天然药专业委员会. 中药与天然药高峰论坛暨第十二届全国中药和天然药物学术研讨会论文集. 2012: 9.
|
| [23] |
王成芳. 动物药材商品高效毛细管电泳指纹图谱的研究[D]. 沈阳: 辽宁中医药大学, 2010.
|
| [24] |
王成芳, 包永睿, 孟宪生, 等. 蛤蚧药材高效毛细管电泳指纹图谱研究[J]. 中药材, 2010, 33(3): 337-339. |
| [25] |
王成芳, 包永睿, 孟宪生, 等. 蕲蛇药材高效毛细管电泳指纹图谱的研究[J]. 辽宁中医杂志, 2010, 37(5): 893-894. |
| [26] |
李峰, 王成芳, 包永睿. 土鳖虫药材高效毛细管电泳指纹图谱鉴别研究[J]. 中国中药杂志, 2011, 36(11): 1471-1473. |
| [27] |
李峰, 沈红薇, 王成芳. 僵蚕HPCE指纹图谱研究[J]. 辽宁中医杂志, 2012, 39(1): 1-3. |
| [28] |
李峰, 张阳, 张振秋, 等. 乌梢蛇药材的高效毛细管电泳指纹图谱研究[J]. 辽宁中医杂志, 2012, 42(10): 1953-1954. |
| [29] |
陈昭, 陈伟韬, 罗文汇, 等. HPCE法研究土鳖虫镇痛作用与其指纹图谱的关系[J]. 中成药, 2016, 38(5): 1074-1077. |
| [30] |
高世杰, 王集会, 王俊香. TRICINE-SDS-PAGE电泳法用于野生全蝎粉鉴定的研究[J]. 山东中医杂志, 2013(2): 114-115. |
| [31] |
吴文如, 李薇, 赖小平, 等. 地龙药材蛋白质电泳鉴定的初步研究[J]. 广东药学院学报, 2011(3): 267-270. |
| [32] |
陈振江, 沈瑜琪, 刘焱文. 贵重动物类中药材蛋白质SDS-PAGE的图谱研究[J]. 中药材, 2007(7): 769-771. |
| [33] |
王晶娟, 张贵君, 李奇豫. 全蝎蛋白药效组分的生物鉴定法研究[J]. 中国实验方剂学杂志, 2010(8): 94-95. |
| [34] |
王丽娟, 朱育凤, 刘训红, 等. 鹿角的X射线衍射Fourier谱鉴别[J]. 现代中药研究与实践, 2009, 23(2): 24-26. |
| [35] |
李兰燕, 王树春, 吴云山, 等. 广地龙的X射线衍射Fourier谱鉴定[J]. 中成药, 2002(5): 58-60. |
| [36] |
王树春, 翁小春, 吴云山, 等. 中药材海马的X射线衍射Fourier图谱鉴定[J]. 西北药学杂志, 2004(6): 248-250. |
| [37] |
王树春, 吕杨, 吴楠, 等. 中药材熊胆的X衍射Fourier谱分析[J]. 中草药, 2000(3): 56-57. |
| [38] |
翁立明, 吴云山, 吕扬, 等. 动物中药材全蝎的粉末X射线衍射Fourier图谱鉴定[J]. 中国医学科学院学报, 2006(5): 700-702. |
| [39] |
王树春, 龚宁波, 陈海明, 等. 中药材鹿茸(花鹿茸)的X衍射Fourier谱分析[J]. 中草药, 2001(12): 70-71. |
| [40] |
朱志峰, 王树春, 刘旭英, 等. 中药材蛤蚧的X衍射Fourier谱分析[J]. 中草药, 2001(10): 71-72. |
| [41] |
肖小河, 鄢丹, 王伽伯, 等. 关于中药质量生物检定的几点商榷[J]. 世界科学技术-中医药现代化, 2009, 11(4): 504-508. |
| [42] |
刘涛, 谭清红, 王晓霞, 等. 基于酶活性的地龙质量标准再评价研究[J]. 中药材, 2014, 37(9): 1535-1537. |
| [43] |
肖凌, 徐小玲, 何开勇, 等. 生物检定技术应用于水蛭抗凝血活性测定的研究[J]. 中国药学杂志, 2015, 50(3): 258-262. |
| [44] |
肖云芝, 万露, 刘朝勇, 等. 鳖甲HPLC指纹图谱的分析模式探讨[J]. 中国实验方剂学, 2015, 21(6): 32-36. |
| [45] |
王欣丽, 李清, 李博惠, 等. 土鳖虫及其混淆品HPLC指纹图谱分析[J]. 中草药, 2016, 47(10): 1780-1784. DOI:10.7501/j.issn.0253-2670.2016.10.025 |
| [46] |
姬诚, 郭万周. 蟾酥的高效液相指纹图谱研究[J]. 光明中医, 2016, 31(12): 1727-1729. DOI:10.3969/j.issn.1003-8914.2016.12.021 |
| [47] |
刘海洋, 耿放, 尹丽颖, 等. 基于GC-MS和主成分分析的蜂蜡质量控制方法研究[J]. 化学工程师, 2015(6): 28-31. |
| [48] |
张晗星, 钱正明, 苏尧, 等. 冬虫夏草不同发育时期蛋白质组iTRAQ质谱分析[J]. 菌物学报, 2016, 35(4): 411-422. |
| [49] |
李峰, 张振秋. 动物药材品质评价体系的构建[J]. 中药材, 2011(11): 1653-1656. |
| [50] |
李俊婕, 于海英, 林钰镓, 等. 电感耦合等离子体发射光谱法同时测定珍珠粉中6种元素[J]. 食品安全质量检测学报, 2016, 7(3): 958-964. |
| [51] |
聂黎行, 胡晓茹, 张聿梅, 等. 基于国家药品抽验任务探讨含动物类成分中成药的质量控制[J]. 中国药学杂志, 2016, 51(6): 506-512. |
 2017, Vol. 31
2017, Vol. 31 
