2. 河南中医学院, 郑州 450046
2. Henan College of Traditional Chinese Medicine, Zhengzhou 450046, China
左归丸为卫生部药品标准中药成方制剂第一册收载的品种。由熟地黄、菟丝子、牛膝、龟板胶、鹿角胶、山药、山茱萸、枸杞子8味中药组成。用于真阴不足,腰酸膝软,盗汗遗精,神疲口燥[1],临床应用广泛。部颁药品标准只对左归丸进行了丸剂项下相关检查,未对其进行含量限定。山茱萸为左归丸方中的主要组成药味,现代药理学研究显示:山茱萸中的环烯醚萜苷类成分具有调节免疫、抗炎、降低血糖、抑制血栓形成、改善神经和记忆功能等作用[2-5]。马钱苷、莫诺苷和山茱萸新苷均属环烯醚萜苷类。马钱苷和莫诺苷的相关研究较多,《中国药典》2015年版一部[6]已将其作为山茱萸及其饮片的质量控制成分,但莫诺苷在山茱萸相关药物质量控制中却多缺失。山茱萸新苷具有抗炎、保护大鼠皮层细胞及保肝护肝等药理作用[7],亦可作为质量控制指标性成分。
一测多评法(QAMS)是多指标质量控制的模式之一,既能够实现多指标性成分的同时测定,又可以解决部分对照品难以获得或价格昂贵的问题,可显著节约检验检测成本[8],该法已经成功应用于双青咽喉片[9]、三黄片[10]、胃苏颗粒[11]等多种中成药的质量控制中。本研究在参考文献[12-16]的基础上,采用一测多评的方法,以较为廉价易得的马钱苷为内参物,通过建立其与莫诺苷和山茱萸新苷之间的相对校正因子,来同步测定3种有效成分的含量,实现了在节约多成分含量测定检验成本的同时,可以较全面地控制左归丸的质量。
1 仪器与试药 1.1 仪器Agilent 1260高效液相色谱仪(美国Agilent公司),Agilent chemstation工作站;Waters 2695高效液相色谱仪(美国Waters公司),Empower工作站。瑞士Precisa XR 205SM-DR分析天平;KQ-250型超声波清洗器(昆山市超声仪器有限公司)。
Phenomenex Luna C18(2)(250 mm×4.6mm,×5μm)色谱柱;Thermo ODS C18(250 mm×4.6mm,5μm)色谱柱;Agilent ZORBAX SB-C18(250 mm×4.6 mm,5μm)色谱柱。
1.2 试剂与药品市售左归丸(水蜜丸)(河南省宛西制药股份有限公司,批号:150208、140904、140207、140910、141001、130704、130517,每10粒重1g)。对照品马钱苷(批号:111640-201005,纯度99.2%,供含量测定用,中国食品药品检定研究院)。莫诺苷(批号:140301,纯度≥ 98%)、山茱萸新苷(批号:131015,纯度≥ 98%),均购自成都普菲德生物技术有限公司,面积归一化法计算对照品的含量在98%以上。乙腈为色谱纯,水为娃哈哈纯净水,其他试剂均为分析纯。
2 方法与结果 2.1 对照品溶液的制备分别取莫诺苷、马钱苷和山茱萸新苷对照品适量,加甲醇配制成浓度分别为莫诺苷0.5694 mg·mL-1、马钱苷0.6891 mg·mL-1、山茱萸新苷mL-1的单一对照品溶液。
分别取莫诺苷、马钱苷和山茱萸新苷对照品适量,精密称定,加甲醇配制成每1 mL含莫诺苷32.39 μg、马钱苷33.90 μg、山茱萸新苷7.75 μg的混合对照品溶液。将上述混合对照品溶液于4 ℃保存,备用。
2.2 供试品溶液的制备取本品适量研细,取约3 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,加热回流提取1 h,取出冷却至室温,加入甲醇补足减失重量,摇匀,滤过,取续滤液,用0.45 μm微孔滤膜过滤,即得。
2.3 阴性对照溶液的制备按左归丸处方比例和制备方法,制备缺山茱萸的阴性对照药,按“2.2”节方法制备缺酒萸肉的阴性对照溶液。
2.4 液相色谱条件色谱柱:Phenomenex Luna C18(2)(250 mm×4.6 mm,5 μm);流动相:乙腈-0.3%磷酸水溶液;梯度洗脱程序见表 1;流速:1 mL·min-1;柱温:35 ℃;检测波长:0~65 min,240 nm,测定莫诺苷和马钱苷;66~80 min,218 nm测定山茱萸新苷;进样量:10 μL。
|
|
表 1 梯度洗脱程序 |
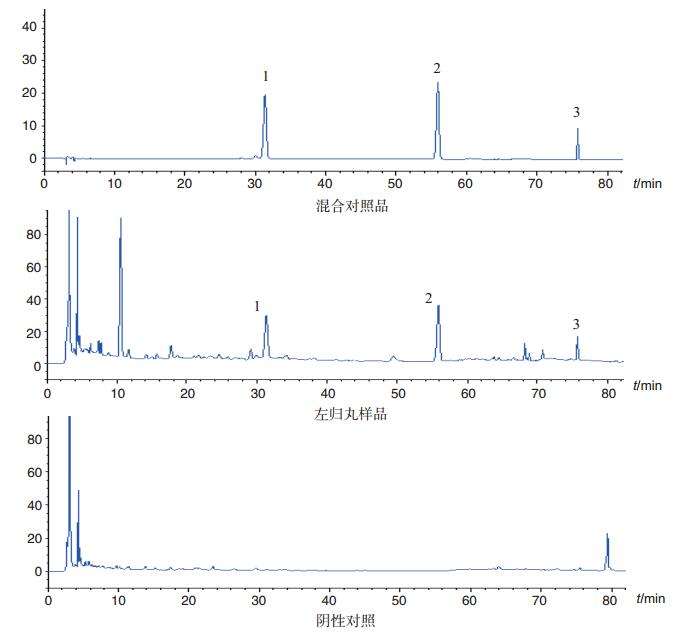
分别吸取混合对照品溶液、供试品溶液和阴性对照溶液,各10 μL,按上述色谱条件,进样测定,结果见图 1。由图 1可知,各待测色谱峰均达到基线分离,阴性对照色谱中,在与莫诺苷、马钱苷和山茱萸新苷相对应的保留时间处无干扰。
|
图 1 HPLC色谱图 1.莫诺苷;2.马钱苷;3.山茱萸新苷。 |
取莫诺苷、马钱苷、山茱萸新苷适量,加入适量甲醇,配制成浓度为莫诺苷180.40μg·mL-1、马钱苷171.22 μg·mL-1、山茱萸新苷76.30 μg·mL-1的混合对照品溶液。精密吸取混合对照品溶液1、2、5、8、10、12、15、20 μL,分别注入高效液相色谱仪,以对照品的进样量X(μg)为横坐标,对照品色谱峰面积Y为纵坐标,绘制标准曲线,计算回归方程。各成分回归方程、线性范围见表 2,结果表明各成分进样量在相应范围内与峰面积积分值呈良好的线性关系。
|
|
表 2 4种成分线性范围、回归方程和相关系数 |
精密吸取同一供试品溶液(批号:150208)10μL,连续进样6次,记录莫诺苷、马钱苷和山茱萸新苷峰面积积分值,计算RSD,结果各成分峰面积的RSD分别为1.26%、0.57%和0.83%。表明仪器精密度良好。
2.5.3 稳定性试验精密吸取同一供试品溶液(批号:150208)10μL,分别于配制后的0、2、4、8、10、15和24h, 测定峰面积积分值,计算RSD,结果莫诺苷、马钱苷和山茱萸新苷峰面积的RSD分别为1.53%、1.04%和0.93%。表明供试品溶液在24 h内稳定。
2.5.4 重复性试验称取同一批供试品粉末(批号:150208),约3 g,精密称定,按供试品制备方法制备6份供试品溶液,测定峰面积积分值,计算RSD,结果莫诺苷、马钱苷和山茱萸新苷平均含量分别为0.370、0.441和0.112 mg·g-1, RSD分别为2.10%、1.48%和2.52%。表明该方法的重复性良好。
2.5.5 加样回收率试验取已测知含量的供试品粉末(批号:150208)约1.5 g,共6份, 分别加入单一对照品溶液(莫诺苷0.5694 mg·mL-1、马钱苷0.6891 mg·mL-1、山茱萸新苷0.1648 mg·mL-1)各1 mL,按“2.2”节方法制备供试品溶液,“2.4”节色谱条件测定峰面积,计算各成分的平均加样回收率以及RSD。结果见表 3~5。
|
|
表 3 莫诺苷加样回收率试验结果(n=6) |
|
|
表 4 马钱苷加样回收率试验结果(n=6) |
|
|
表 5 山茱萸新苷加样回收率试验结果(n=6) |
采用Phenomenex Luna C18(2)(250 mm×4.6 mm,5 μm)色谱柱,Agilent 1260高效液相色谱系统,精密吸取混合对照品溶液1、2、5、8、10、12、15 μL,分别进样分析。以马钱苷为内参物,根据相对校正因子计算公式[17]:fsi= fs / fi =
|
|
表 6 相对校正因子 |
采用Phenomenex Luna C18(2)(250 mm×4.6 mm,5 μm)色谱柱,精密吸取混合对照品溶液1、2、5、8、10、12、15 μL,分别进样分析。考察了3种不同的高效液相色谱系统:Agilent 1260、岛津LC-20A和Waters 2695,对环烯醚萜苷类成分相对校正因子的影响,结果见表 7。由表 7可知,采用3个品牌的高效液相色谱仪求得各成分相对校正因子的相对平均偏差均<5%,不同的高效液相色谱仪对相对校正因子和相对保留时间的影响较小。
|
|
表 7 不同高效液相色谱仪对校正因子的影响 |
分别考察Agilent 1260、岛津LC-20A高效液相色谱仪和Phenomenex Luna C18(2)(250 mm×4.6 mm,5 μm)、Agilent ZORBAX SB-C18(250 mm×4.6 mm,5 μm)、Thermo ODS C18(250 mm×4.6 mm,5 μm)色谱柱,对相对校正因子的影响,结果见表 8。结果表明,不同的色谱仪和色谱柱对相对校正因子和相对保留时间的影响较小。
|
|
表 8 不同高效液相色谱仪及色谱柱对校正因子的影响 |
在2个实验室对所建立的“一测多评”校正因子进行复核试验。同为Agilent 1260高效液相色谱仪及Phenomenex Luna C18(2)(250 mm×4.6 mm,5 μm)色谱柱,2个实验室测得的莫诺苷和山茱萸新苷相对校正因子分别为1.048、1.390和1.035、1.376。各成分的相对校正因子的RSD均<5%。说明所建立的相对校正因子在不同的实验室有良好的可行性。
2.7 待测组分色谱峰的定位本研究分别考察了相对保留时间和保留时间差在不同品牌仪器和不同规格色谱柱中的重现性。结果表明,保留时间差的波动较为明显,RSD>5%;而相对保留时间的波动较小。因此,采用相对保留时间定位待测组分色谱峰,结果见表 9、10,莫诺苷和山茱萸新苷的相对保留时间分别为0.564、1.360。
|
|
表 9 不同仪器和色谱柱相对保留时间比较 |
|
|
表 10 不同仪器和色谱柱保留时间差比较 |
精密吸取7批供试品溶液各10 μL,分别注入高效液相色谱仪进行测定。采用外标法和一测多评法,计算左归丸中莫诺苷和马钱苷的含量,结果见表 11。结果表明2种含量测定方法无显著性差异,相对误差<5%。
|
|
表 11 QAMS法与ESM法测得的左归丸中3种成分的含量(n=2) |
由于马钱苷为《中国药典》2015年版规定的山茱萸质量控制指标性成分,性质稳定、市场流通性强、较易得到,且其出峰时间和峰面积适中;而莫诺苷和山茱萸新苷价格较昂贵。因此,选择马钱苷为内参物。
根据目标峰与内参峰之间的相对保留值,即能够正确判断出各目标峰的准确位置。
3.2 流动相及柱温的考察比较了甲醇和乙腈作为有机相、不同浓度的磷酸水溶液作为无机相的梯度洗脱效果,结果发现乙腈-0.3%磷酸水溶液洗脱分离效果较好,达到基线分离,所以选择乙腈-0.3%磷酸水溶液梯度洗脱系统为流动相。比较了4种不同的色谱柱温:25、30、35和40 ℃对分离效果的影响,结果当柱温为35 ℃时,各成分分离效果和峰形良好。
| [1] |
国家药典委员会. 中药成方制剂标准: 第一册[S]. 1998: 54.
|
| [2] |
王世全. 山茱萸主要化学成分及药理学研究进展[J]. 医学信息, 2010, 23(12): 4867. |
| [3] |
张丽, 叶翠飞, 张兰, 等. 山茱萸环烯醚萜苷对血栓形成和凝血功能的影响[J]. 中药新药与临床药理, 2008, 19(5): 363-366. |
| [4] |
张丽, 李春阳, 赵玲, 等. 山茱萸环烯醚萜苷对局灶性脑缺血模型大鼠神经功能和神经元损伤的影响[J]. 中国康复理论与实践, 2007, 13(3): 201-202. |
| [5] |
丁月霞, 张丽, 叶翠飞, 等. 山茱萸环烯醚萜苷对穹隆海马伞切断大鼠学习记忆能力和突触生长素的影响[J]. 中国新药杂志, 2010, 19(2): 133-138. |
| [6] |
中国药典: 一部[S]. 2015: 27.
|
| [7] |
宋顺宗. 山茱萸新苷和人参皂苷肝保护及抗肝纤维化作用的研究[D]. 吉林: 延边大学药学院, 2011.
|
| [8] |
范成杰. 一测多评法在中药质量评价和控制中的应用概况[J]. 中药与临床, 2013, 4(2): 18-20. |
| [9] |
何兵, 刘艳, 杨世艳, 等. 一测多评法同时测定双青咽喉片中10种成分[J]. 中草药, 2013, 44(8): 974-981. |
| [10] |
王钰莹, 冯伟红, 杨菲, 等. "一测多评"法测定三黄片中的大黄蒽醌类成分[J]. 中国中药杂志, 2012, 37(2): 212-217. |
| [11] |
李玲, 赵顺, 罗疆南, 等. 一测多评法测定胃苏颗粒中4种成分的含量[J]. 药物分析杂志, 2015, 35(4): 751-757. |
| [12] |
孟建升, 王伟丽, 杨文文, 等. HPLC法测定左归丸中马钱苷的含量[J]. 中国中医药现代远程教育, 2012, 10(18): 152-153. |
| [13] |
潘莹, 郭小龙, 陈勇, 等. HPLC法测定杞菊地黄丸中马钱苷、芍药苷和丹皮酚的含量[J]. 中国药科大学学报, 2007, 38(2): 133-135. DOI:10.11665/j.issn.1000-5048.20070209 |
| [14] |
孙琳林, 陈海玲, 卢林, 等. 高效液相色谱法测定左归丸中马钱苷的含量[J]. 中华中医药学刊, 2012, 30(8): 1792-1793. |
| [15] |
李桂本, 王海波, 李振国. HPLC波长切换技术同时测定知柏地黄丸(浓缩丸)中莫诺苷、芒果苷、马钱苷和丹皮酚的含量[J]. 药物分析杂志, 2015, 35(1): 125-128. |
| [16] |
李娴, 王本杰, 袁桂艳, 等. 六味地黄丸中四种活性成分的HPLC法测定[J]. 中国医药工业杂志, 2010, 41(2): 126-128. |
| [17] |
王智民, 钱忠直, 张启伟, 等. 一测多评法建立的技术指南[J]. 中国中药杂志, 2011, 36(6): 657-658. |
 2017, Vol. 31
2017, Vol. 31 
