2. 宁波出入境检验检疫局, 宁波 315000
2. Ningbo Entry-Exit Inspection and Quarantine Bureau, Ningbo 315000, China
医用疫苗是一种特殊的商品,其安全性直接影响人身健康。医用疫苗的包装材料,尤其是直接接触材料,对保证药品的稳定性、安全及可靠性起着极其重要的作用[1-4]。因此,药品包装材料的可靠性是评价疫苗质量的重要指标之一。目前市场上应用于药品包装中瓶装密封材料的合成橡胶主要是卤化丁基橡胶。卤化丁基橡胶有良好的化学稳定性,但其配方中添加了多种橡胶助剂,助剂的迁移可能会降低药物的浓度,甚至影响到药物的安全性。
2, 6-叔丁基-4-甲基-苯酚(BHT)是卤化丁基胶塞中常用的抗氧化剂[5-6]。研究表明,BHT对肺、肝等组织有直接损害作用,并有可能促进肿瘤发生[7]。部分国家已经禁止BHT作为食品当中的添加剂。疫苗当中的BHT的含量高低是评价药用卤化丁基胶塞与疫苗的相容性的重要指标。
迁移实验的目的是为了检测疫苗在有效期内真实的浸出物情况,并据此进行疫苗安全性评估。迁移浸出物研究重要的一个原则就是实验条件应该与药品的实际存放条件相同或相近。充分考虑药品的生产、贮存、运输及使用过程中可能会面临的最恶劣条件下进行加速及长期稳定性试验[8-12]。由于迁移浸出物的浓度较低,因此需要对分析方法进行全面验证,确认方法的专属性、灵敏度等,以证实该方法能准确灵敏地检测出疫苗中的浸出物[13-15]。本研究采用GC-MS法测定常温放置及加速试验条件下的两种医用疫苗中BHT的迁移量,前处理过程简单,灵敏度高,检出限低,可对药用卤化丁基胶塞的质量进行评估。
1 试验部分 1.1 仪器与试剂美国Agilent 7890B-5977A GC-MS气质联用仪,Milli-Q型纯水系统,KQ3200DE型超声波清洗器。
正己烷为HPLC级(Fisher公司,Lot Number:140101),试验用水为超纯水。样品溶液均用0.45μm滤膜过滤。对照品为2, 6-叔丁基-4-甲基-苯酚(BHT)(麦克林公司,分析标准品>99.7%,批号:C10029171)。
本实验共涉及2种侵袭性b型流感嗜血杆菌(Hib)和百白破两种医用疫苗,瓶身为透明西林瓶,胶塞为氯化丁基胶塞,各7生产批次样品,包括2015年度3批次和2016年4批,各3组加速试验(0、14、21天)。
1.2 GC-MS条件 1.2.1 GC色谱条件色谱柱:DB-WAX毛细管气相色谱柱(30.0 m×0.25 mm,0.25μm);载气:高纯氦气,流速:1 mL·min-1;进样口温度:240℃;程序升温条件:100℃,保持0 min,以10℃·min-1速度升温到200℃,保持0 min,以15℃·min-1速度升温到240℃,保持5 min;进样量:1μL,进样方式:不分流进样。
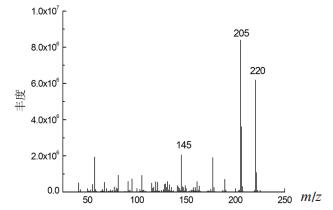
1.2.2 质谱条件电子轰击离子源(EI),轰击电压:70 eV,离子源温度:230 ℃,传输线温度:240 ℃;定性:全扫描方式,扫描质量范围:50~1050;定量:选取BHT质谱图中特征离子m/z 205进行扫描,m/z 220,m/z 145作为定性离子,监测模式:SIM。
1.3 标准溶液配制准确称取BHT对照品适量,置于容量瓶中,加正己烷稀释至刻度,配制成质量浓度为10、20、40、100、200、400μg·L-1的系列混合标准工作溶液。
1.4 试验方法取疫苗5支,倒出全部液体置50 mL样品瓶中,并用1 mL超纯水洗涤各空瓶,重复洗涤3次,转移置50 mL样品瓶中。另取1 mL正己烷洗涤各空瓶,重复洗涤3次,将溶液转移置25 mL容量瓶中,加正己烷至刻度后,将容量瓶中的溶液全部倒入50 mL样品瓶中,超声15 min(150 w),静置,取上清液1 mL作为供试品溶液。
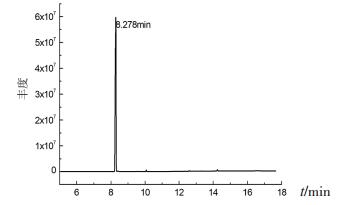
2 结果 2.1 定性分析按上述分析条件对样品及对照品进行GC-MS分析,对保留时间为8.278 min的总离子流图对应的质谱图进行谱库检索,并比较其丰度比,其与NIST11谱库中BHT相似度为83.2%,根据样品与对照品的保留时间与丰度比定性。见图 1、图 2。
|
图 1 BHT对照品的总离子流图 |
|
图 2 BHT的质谱图 |
精密称取BHT对照品50 mg,置于100 mL容量瓶中,加正己烷溶解,配制成500 mg·L-1的母液,然后逐级稀释至10、20、40、100、200、400 μg·L-1,摇匀,分别取1 μL进样,在上述GC-MS条件下进行测试。以对照品溶液浓度C(mg·L-1)为横坐标,峰面积A为纵坐标,绘制标准曲线并进行线性回归,得到BHT的回归方程:
A=363.2C-1435 r2=0.9993
表明BHT在10~400 μg ·L-1浓度范围内线性关系良好。采用空白基质加标的方法,依次稀释,照前述测定方法测定,计算其信噪比,得到BHT溶液的检出限(3S/N)为1 μg·L-1,定量限(10S/N)为2 μg·L-1,即每瓶疫苗BHT迁移量检出限为0.005 μg;每瓶疫苗迁移量定量限为0.01μg。
2.3 精密度和稳定性试验取线性范围内10 μg·L-1的BHT对照品溶液,分别在常温下放置0、24、48 h, 分别进行2次平行测定,计算其日间RSD为8.3%,表明样品在48 h内稳定。
2.4 回收率试验分别取Hib疫苗(批号:1#)及百白破疫苗(批号:8#)进行回收试验。每份取疫苗5支,倒出全部液体置50 mL样品瓶中,并分别加入BHT对照品溶液(使回收测定用的供试液中加入的BHT浓度分别为1.0、2.0、10.0 μg·L-1)作为供试品溶液。3个加样浓度,每个浓度分别制备3份,共9份,按前述测定方法测定,并计算其回收率。结果见表 1。
|
|
表 1 BHT加标回收试验结果 |
分别取7批次Hib疫苗及百白破疫苗,并参照文献《药品包装材料与药物相容性试验指导原则》,对14批次疫苗进行加速试验考察。加速试验的条件:40℃±2℃,RH 75%±5%, 放置0、14、21天,分别考察两种疫苗在不同加速时间段内BHT的迁移情况。由于疫苗为液体,在测放和倒立的过程中,胶塞被疫苗浸泡,为模拟实际运输及储存的极限情况,在上述加速试验过程中,样品的放置方式采用1/2的放置时间倒立,1/2的放置时间侧放。测试结果见表 2。
|
|
表 2 疫苗中BHT迁移量测定结果 |
迁移试验的目的是检测疫苗在有效期内真实的浸出物情况,并据此进行安全性评估。本试验考虑到药品的生产、贮存、运输及使用过程中所面临的最恶劣条件。据悉,医用疫苗在冷藏条件下的保质期为24个月,因此本文选用了临质保期和近期生产的样品批次进行加速试验,能真实反应样品的实际迁移量和迁移风险。结果表明,该公司生产的Hib疫苗及百白破疫苗,其包装使用药用氯化丁基胶塞,其胶塞中的BHT在40℃±2℃,RH 75%±5%,放置21天的情况下有痕量BHT迁移(折合每瓶0.005 µg),证明该药用胶塞与相容性较好,但仍存在迁移风险,因此应严格把控药用氯化丁基胶塞的质量。
本文建立的GC-MS方法可用于测定医用疫苗当中的BHT迁移量,灵敏度高,准确性好,有助于生产企业对疫苗进行安全性评估。
| [1] |
赵霞, 胡昌勤, 金少鸿. 药用丁基胶塞中易挥发性成分的成分分析[J]. 药物分析杂志, 2006, 26(3): 315-318. |
| [2] |
张芳艳, 赵欣欣, 余萍. 药品包装材料存在的问题及其对用药安全的影响[J]. 中国药业, 2012, 21(16): 10-11. DOI:10.3969/j.issn.1006-4931.2012.16.007 |
| [3] |
殷果, 秦斌, 王铁杰, 等. 药用丁基胶塞与注射用阿莫西林钠的相容性研究[J]. 中国抗生素杂志, 2012, 37(9): 699-701. |
| [4] |
林晨熙, 高丹玲. 注射用头孢唑林钠与卤化丁基胶塞相容性的加速试验[J]. 海峡药学, 2011, 23(1): 54-56. |
| [5] |
赵策强. 抗氧化剂BHT的研究与应用[J]. 中国高教杂志市场版, 2006, 42(4): 62-63. |
| [6] |
曲亚南, 徐苏华, 陈浩瀚, 等. 固相萃取-高效液相色谱法测定极性注射液中抗氧剂BHT含量[J]. 中国医疗器械信息, 2015, 12: 52-56. |
| [7] |
Powell C.J., Connelly J.C., Jones S.M., et al. Hepatic Responses to the Administration of High Doses of BHT to the Rat:Their Relevance to Hepatocarcinogenicity[J]. Food and Chmical Toxicology, 1986, 24(10-11): 1131-1143. DOI:10.1016/0278-6915(86)90299-1 |
| [8] |
国家食品药品监督管理局. 化学药品注射剂与塑料包装容器相容性研究技术指导原则(试行)[EB/OL]. (2012-09-07)[2017-02-10] http://www.sda.gov.cn/WS01/CL0844/75197.html.
|
| [9] |
张宇. 药用丁基胶塞与药物相容性研究现状和展望[J]. 天津药学, 2010, 22(1): 72-74. |
| [10] |
周劼, 殷果, 刘洪伟, 等. 药用胶塞及其与药品的相容性简述[J]. 中国医药工业杂志, 2013, 44(8): 801-803. |
| [11] |
李立根, 张毅兰. 药用胶塞及其与药品的相容性简述[J]. 中国医药工业杂志, 2015, 46(12): 1366-1371. |
| [12] |
赵霞, 胡昌勤, 金少鸿. 对考察药用丁基胶塞与药物相容性的思考与建议[J]. 中国药事, 2007, 21(10): 810-812. DOI:10.3969/j.issn.1002-7777.2007.10.013 |
| [13] |
杨洪贤, 高秀珊, 潘英新. 丁基胶塞与注射用青霉素钠相容性实验考察[J]. 实用药物与临床增刊, 2005(8): 8-9. |
| [14] |
魏宁漪, 庾莉菊, 余振喜, 等. GC-MS法测定注射用甲氨蝶呤中BHT的含量[J]. 中国药事, 2011, 25(6): 591-593. |
| [15] |
姜源, 程福军. 注射液用氯化丁基胶塞中的抗氧剂的测定和迁移测定[J]. 黑龙江医药, 2016, 29(3): 436-438. |
 2017, Vol. 31
2017, Vol. 31 