少腹逐瘀丸由当归、蒲黄、五灵脂、赤芍、延胡索、没药、川芎、肉桂、炮姜和小茴香10味中药组成。原方出自清朝老中医王清任的《医林改错》下卷,为汤剂,现为《中国药典》所收载,具有温经活血、散寒止痛之功效,用于治疗血瘀寒凝型月经不调、痛经的常用中成药[1],素有“妇科第一方”之称。药效学试验证实本品具有缓解子宫平滑肌收缩、抗炎、镇痛,降低全血粘度和改善子宫膜微循环的作用[2-3]。
没药为方中臣药,为橄榄科植物没药树Commiphoramyrrha Engl.或爱伦堡没药树的胶树脂。主产于索马里、埃塞尔比亚、土耳其等国家[4],富含挥发油[5],具有散血去瘀、消肿定痛之功效。没药作为一种重要的中药材绝大多数以配方的形式被广泛用于临床,其性能也越来越受到人们的关注[6]。由于本品来源有限、价格较贵,其药材、饮片的生产、经营中可能有掺假的现象,如掺石膏粉等,杨秀泽等[7-8]研究了其相应的鉴别方法。松香为常用的化工原料,主要成分为松香酸酐和游离松香酸[9],用于松香皂和甘油松香酯等[10],由于松香酸价廉易得,具特殊香气,常被不法分子作为中药乳香、没药等的造假材料。松香酸对局部组织有刺激作用,大量内服吸收后中枢神经先兴奋后麻醉,对身体会造成极大的危害。据报道,银屑敌胶囊因非法添加松香酸而造成了服用者视力下降、死亡等严重后果[11]。现行标准中没有少腹逐瘀丸松香酸的检查,参照药典方法,本试验对松香酸进行了薄层色谱鉴别,可能由于少腹逐瘀丸中没药经过炮制和粉碎,虽然检出了疑为松香酸的斑点,但分离效果不佳,因此本试验建立了灵敏度更高、准确性更强的HPLC法来检测少腹逐瘀丸中非法添加的松香酸,同时采用二极管阵列检测器(PDA)确定结果和HPLC/MS来加以验证[12-15]。
1 仪器和试药 1.1 仪器WATERS 2695-2996 / 2424-ELSD高效液相色谱仪;岛津2010高效液相色谱仪,2996PDA二极管阵列检测器,HPLC / MS-8030液质联用色谱仪(TSQ QUANTUM ACCESS MAX),BP211D电子天平(Sartorius)。HPLC用C18色谱柱(250 mm×4.6 mm,5μm;分别为岛津公司和戴安公司)。LC-MS用色谱柱为Accucore C18柱(100 mm×2.1 mm,2.6μm)。
1.2 试药松香酸(中国食品药品检定研究院,批号:111938-201201),少腹逐瘀丸为2014年国家药品监督抽验样品(A企业生产,批号为140408;B企业生产,批号为140101;C企业生产,批号为130106;D企业生产,批号为120114;E企业生产,批号为49140301;F企业生产,批号为7280003),占总批次的14%。乙腈、四氢呋喃(色谱纯,DIKMAPURE公司),甲酸(分析纯,国药集团化学试剂有限公司),水为超纯水。
2 方法与结果 2.1 HPLC-PDA鉴别 2.1.1 色谱条件与系统适用性试验色谱柱:C18(4.6 mm×250 mm,5 μm),流动相:乙腈-四氢呋喃-0. 1 %甲酸水溶液(35:25:40),PDA波长扫描范围:190~ 300 nm,检测波长241 nm;进样量为供试品溶液20 μL,对照试剂溶液10μL,柱温为30℃;流速:1 mL·min-1;理论塔板数按松香酸对照品溶液色谱中的主峰计算,应不低于2000;松香酸峰与相邻峰的分离度应大于1.5。
2.1.2 对照试剂溶液的制备精密称取松香酸对照试剂10 mg置10 mL量瓶中,加甲醇使溶解并稀释至刻度,摇匀,即得。
2.1.3 供试品溶液的制备取少腹逐瘀丸供试品1丸,加硅藻土适量,碾匀研细,置锥形瓶中,加甲醇35 mL,超声处理30 min(250 W,33 kHz),静置,取上清液,0.45μm滤膜滤过,即得。
2.1.4 阴性对照溶液取原料药药材,按处方制得不加没药和加没药对照药材两种阴性样品,按供试品制备方法制备相应的阴性对照溶液。
2.1.5 HPLC-PDA检测吸取供试品溶液、阴性对照溶液20μL与对照试剂溶液10μL,注入液相色谱仪,结果阴性样品在松香酸峰相应位置上无吸收峰,阳性样品与松香酸对照试剂光谱图与色谱图一致,表明样品中其他成分对松香酸的测定无干扰。检测结果见图 1。

|
图 1 阴性样品及阳性样品与松香酸对照试剂的色谱和光谱图比较 |
色谱柱为Accucore C18柱(2.1 mm×100 mm,2.6μm);流动相为乙腈-0.1%甲酸水(75:25)等度洗脱。
2.2.2 质谱条件离子源:电喷雾离子源,离子化模式ESI+;喷雾器压力:60 psi,干燥气(N2),干燥气温度:350 ℃,毛细管电压:4000 V,碎片电压:100 V,柱流量:0.2 mL·min-1;进样量:1μL;柱温:30℃。扫描离子范围:105~500 m/z。
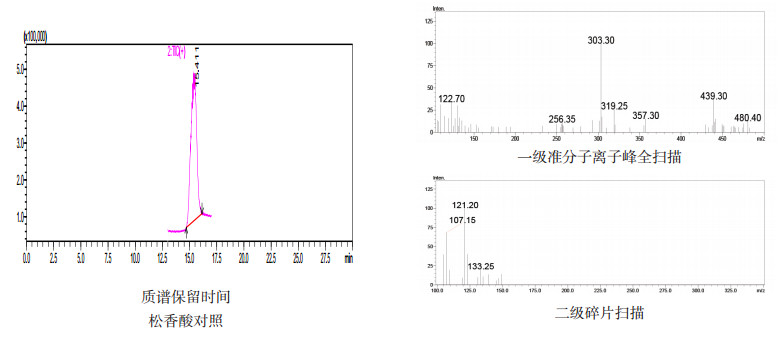
2.2.3 HPLC-MS检测分别精密吸取“2.1.2”节下的对照试剂溶液10μL与“2.1.3”节下的供试品溶液20μL,注入液相色谱-质谱仪,进行质谱分析。分析显示,松香酸对照试剂溶液准分子离子峰[M+1]+=303.30,碎片离子m/z为107.15和121.20,测定结果见图 2~5。
|
图 2 松香酸对照试剂质谱确认图谱 |
|
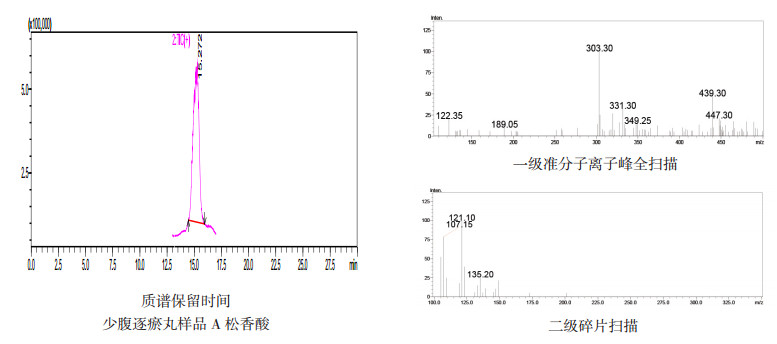
图 3 A公司生产的少腹逐瘀丸中松香酸检查LC/MS质谱图 |
|
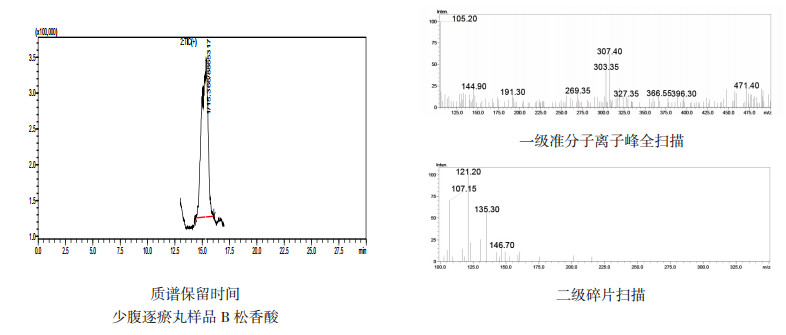
图 4 B公司生产的少腹逐瘀丸中松香酸检查LC/MS质谱图 |
|
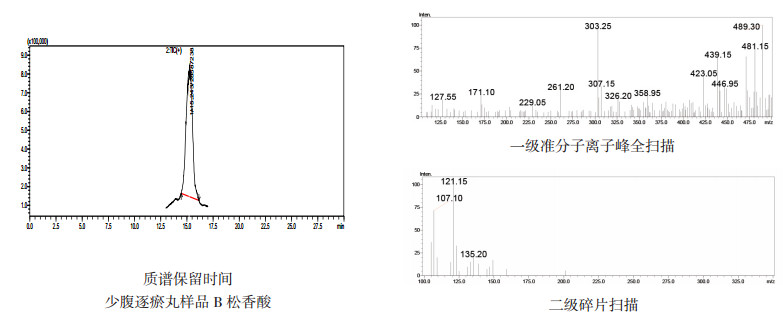
图 5 C公司生产的少腹逐瘀丸中松香酸检查LC/MS质谱图 |
精密称取松香酸对照试剂10 mg置10 mL量瓶中,加甲醇使溶解并稀释至刻度,摇匀,即得。
2.3.2 供试品溶液的制备取少腹逐瘀丸供试品1丸,加硅藻土适量,碾匀研细,精密称取0.3 g,置锥形瓶中,加甲醇35 mL,超声处理30 min(250 W,33 kHz),静置,取上清液,0.45μm滤膜滤过,即得。
2.3.3 测定法吸取供试品溶液、阴性对照溶液各20μL与对照试剂溶液10μL,注入液相色谱仪,测定,即得。
2.3.4 线性关系考察取松香酸对照试剂适量,精密称定,加甲醇制成每1 mL含0.1582 mg的溶液,摇匀,即得。分别取1、2、3、5、10μL注入液相色谱仪,记录色谱图,以各自的峰面积对其质量数(mg)进行线性回归,回归方程:
Y=5977.4X-5157.3,r=0.999
结果表明在0.1582 ~1.582μg·mL-1松香酸峰面积与其质量呈良好线性关系。
2.3.5 精密度试验精密吸取对照试剂溶液10μg·mL-1,按上述色谱条件连续进样6次,测定待测组分的峰面积,计算松香酸峰面积的RSD(n=6)为0.97%
2.3.6 重复性试验取同一批样品(批号140408)共6份,按“ 2. 1. 3 ”节下方法制备供试品溶液,进样量20μg·mL-1,测定峰面积,计算样品中待测组分含量及其RSD,结果样品中松香酸的平均含量(n=6)为917.8 mg/丸,RSD为0.95%。
2.3.7 检测限在阴性样品(批号7280003)中精密加入质量浓度为0.9562 μg·mL-1的松香酸对照试剂溶液,照供试品溶液的制备方法制备,根据峰高以信噪比S/N=3确定松香酸的检测限为0.64μg·g-1。
2.3.8 回收率试验按照“2.1.3”节下供试品溶液制备方法精密称取样品(批号140101)和硅藻土9 g,按处方量分别加入等浓度的松香酸对照试剂6份,照供试品溶液的制备方法制备6份回收率测试溶液,测定,计算回收率,测得回收率为99.8%,RSD=0.23%(n=6)。
2.4 样品测定采用液相色谱外标法对含有松香酸的样品定量测定,结果见表 1。
|
|
表 1 少腹逐瘀丸中松香酸含量测定结果(n=2) |
使用WATERS 2695-2996高效液相色谱仪、戴安C18(4.6 mm×250 mm,5μm)色谱柱及岛津2010高效液相色谱仪、岛津C18(4.6 mm× 250 mm,5μm)色谱柱,按“2.1.1”节方法测定批号为140408的供试品溶液。结果表明使用不同型号的仪器和不同型号的色谱柱均能获得良好的分离效果且松香酸含量测定结果一致。
3.2 质谱验证结果液相色谱-质谱联用由于具有高度的专属性,目前成为检查非法掺伪类现象的主要手段,本试验利用液相保留时间(RT=15 min)和松香酸正离子([M+1]+=303.30)模式下不同碰撞能量产生的2个特征子离子(107.15和121.20)来判断是否含有松香酸,有效地避免了假阳性结果的出现。为保证检测结果的准确性,利用液质联用法,对HPLC检测出的松香酸阳性样品采用HPLC/MS/MS进行验证,试验采用ESI+扫描方式进行定性,同时进行一级质谱全扫描、二级全扫描,扫描范围:105~500 m/z,能够更准确地确定检测结果。
3.3 样品基本情况少腹逐瘀丸为2014年国家药品监督抽验样品,共抽取样品21批次,涉及6家生产企业。其中有3家生产企业,共3批次样品检出为阳性样品,并经液质联用验证确认,占企业总数的50%,占样品总批次的14%。
3.4 样品处理方法取少腹逐瘀丸供试品1丸,加硅藻土适量,碾匀研细,置锥形瓶中,加甲醇35 mL,超声处理30 min(250 W,33 kHz),静置,取上清液,0.45μm滤膜滤过,即得。
3.5 检测方法从表 1的检验结果可见,对于掺伪的少腹逐瘀丸,仅按《中国药典》目前现有的检测项目,还不能完全控制其质量。没药原药材松香酸的补充检验方法中,国家规定为不得检出。本方法阴性样品加松香酸对照试剂溶液色谱中松香酸色谱峰的峰高均大于3倍基线噪音,即制剂中松香酸的含量为万分之一时,该方法可检出松香酸,作为该方法的报告限。
本文建立的少腹逐瘀丸中松香酸HPLC检查法结果准确、方法可行,具有较好的实用价值,可满足少腹逐瘀丸定性定量检测的要求,作为该药品的补充检验方法。
| [1] |
中国药典: 一部[S]. 2010: 514.
|
| [2] |
吴丽丽. 少腹逐瘀丸治疗痛经和月经不调的药效学研究[J]. 时珍国医国药, 2003, 14(10): 595-596. DOI:10.3969/j.issn.1008-0805.2003.10.005 |
| [3] |
中华人民共和国药典临床用药须知: 中药成方制剂卷[S]. 2010.
|
| [4] |
江苏新医学院. 中药大辞典:上册[M]. 上海: 上海人民出版社, 1977: 1167, 1255, 1379.
|
| [5] |
王艳艳, 王团结, 宿树兰, 等. 乳香没药药对配伍挥发油成分的GC-MS分析[J]. 现代中药研究与实践, 2011, 25(2): 31-34. |
| [6] |
韩淑芬, 金仲品. 没药的药理活性研究进展[J]. 时珍国医国药, 2008, 19(6): 1502-1503. |
| [7] |
杨秀泽, 周汉华. 一种掺伪品乳香的鉴别研究[J]. 江苏中医药, 2010, 42(5): 65-68. |
| [8] |
刘松明, 高万山. 一种伪品乳香的鉴别研究[J]. 基层中药杂志, 1999, 1(3): 33-34. |
| [9] |
郇义才, 牛保春. 轻量方剂的使用范围[J]. 新疆中医药, 2003, 21(6): 37-40. |
| [10] |
王箴. 化工辞典[M]. 北京: 化学工业出版社, 2000: 881-882.
|
| [11] |
张亚双, 闵春艳. 沉香、乳香和没药中非法添加松香酸的研究与讨论[J]. 西北药学杂志, 2013, 28(2): 133-136. |
| [12] |
钟名诚, 饶伟文, 肖聪. 乳香的商品调查与质量检测方法研究[J]. 中国现代应用药学, 2012, 29(5): 409-414. |
| [13] |
李莉. 麝香接骨胶囊中掺假物松香酸的检查[J]. 药学与临床研究, 2010, 18(5): 499-500. |
| [14] |
国家食品药品监督管理局药品检验补充检验方法和检验项目批准件2011006: 没药[S]. 2011.
|
| [15] |
张亚双, 闵春艳. 小活络丸中非法添加松香酸的检查方法研究[J]. 中成药, 2013, 35(4): 867-869. |
 2017, Vol. 31
2017, Vol. 31 
