2014年12月,ICH指导委员会批准了ICH Q3D元素杂质指南(Current Step 4 Version),该指南目的是提供一份全球性指导原则来定性和定量限制药品和药品组分中金属杂质。由于元素杂质并不给患者提供任何治疗益处,其在药品中的水平应被控制在可接受限度以内。本指南分为3个部分:潜在元素杂质毒性数据的评估,为每个毒性关注元素建立PDE值,以及应用基于风险评估的方法来控制药品中的元素杂质。如果药品中的元素杂质没有超过PDE阈值,申报人不需要根据其工艺能力严加限度。元素根据其毒性(PDE)及在药品中出现的可能性分为3类:1类、2类(2A和2B)和3类。其中,钯元素属于2B类,即为由于自然含量较低,与其他物料共存可能性较低,在药品中出现的可能性较低的元素。因此,除非其在原料药、辅料或药品其他成分中有意加入,否则可能被排除在风险评估以外。
2013年9月30日,美国食品药品管理局(FDA)批准将氢溴酸沃替西汀(Vortioxetine,商品名:Brintellix)用于治疗成人重型抑郁症(MDD)[1-2]。鉴于其对认知的积极影响及可耐受的副作用属性,氢溴酸沃替西汀将成为治疗单相抑郁症药物中最成功的新药。然而,在氢溴酸沃替西汀原料药的合成工艺中,用到了钯催化剂,基于安全性和质控的需求,需要对氢溴酸沃替西汀原料药的钯残留进行严格控制。
微量钯的测定主要采用石墨炉原子吸收光谱仪(GFAAS)[3]、电感耦合等离子体-质谱仪(ICP-MS)[4]、全反射X射线荧光仪(TXRF)[5]、中子活化分析仪(INAA)[6]、分光光度法[7]和离子交换树脂比色法[8]等。石墨炉原子吸收光谱仪具有运行成本较低、操作简单、进样量小和对基质要求相对较低的优点[9-11]。本试验应用石墨炉原子吸收法测定氢溴酸沃替西汀原料药中残留的钯,灵敏度高,干扰少,方法简便快速[12-15]。
1 仪器与试剂TAS-990原子吸收光谱仪(配石墨炉原子化器和ASC-990自动进样系统,北京普析通用仪器有限责任公司);Med-C型微波消解仪(配高温聚四氟乙烯消解罐,上海屹尧仪器科技发展有限公司);DKQ控温电热板(上海屹尧仪器科技发展有限公司);空心阴极灯(钯灯,北京曙光明电子光源仪器有限公司)。
氢溴酸沃替西汀原料药(山西振东制药股份有限公司,批号:20150420),单元素钯溶液[1.000 μg·mL-1, 国家实物标准号:GSB G 62038-90(4601),国家钢铁材料测试中心钢铁研究总院];硝酸、盐酸(BV-Ⅲ级,北京化学试剂研究所);实验用水为高纯水(电阻率为18.0 M Ω·cm)。
2 方法和结果 2.1 光谱条件光源:空心阴极灯(钯灯);灯电流:2 mA;波长:247.6 nm;通带:0.4 nm;进样量:20 μL;石墨管类型:横向平台;保护气:氩气;氩气压力:0.4 MPa;石墨炉程序参数见表 1。
|
|
表 1 石墨炉程序参数设置 |
取本品0.2 g于聚四氟乙烯高压消化罐中,加入5 mL硝酸,2 mL双氧水,加盖密封并将高压消化罐放入微波消解仪中,按设定的程序进行消解:120 ℃消解2 min,150 ℃消解3 min,165 ℃消解3 min,180 ℃消解5 min。消解完成后,待温度降至60 ℃后,取出,将澄清溶液转移置量瓶中,用去离子水定容至50 mL,摇匀待测。
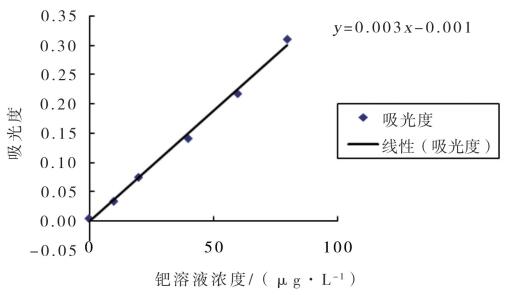
2.3 线性关系考察用1000 μg·mL-1的钯标准溶液和10%硝酸稀释液配制成10、20、40、60、80 μg·L-1的标准溶液,以10%硝酸溶液做空白液,试液的进样体积为20 μL,每个标准工作点均为2次进样。以钯溶液浓度为横坐标,原子吸光度为纵坐标,制作标准工作曲线,见图 1。此标准曲线的线性方程:
| $ y=0.003x-0.001 \;\;r=0.9995 $ |
|
图 1 钯溶液标准工作曲线 |
说明钯浓度在0 ~ 80 μ·L-1线性关系良好。
2.4 精密度试验取20 μg·L-1标准钯溶液,连续进样测定6次,记录吸光度,计算得出RSD为1.73%。表明仪器精密度良好。
2.5 检测限与定量限取10%硝酸溶液平行进样11次,记录吸光度,以吸光度标准偏差的3倍与标准曲线的斜率比值,计算得到仪器的检测限;以吸光度标准偏差的10倍与标准曲线的斜率比值,计算得到仪器的定量限。结果检测限为0.59 μg·L-1,定量限为1.96 μg·L-1。
2.6 重复性试验取样品(批号:20150420)6份,各约0.2 g,精密称定,制备供试品溶液,进样测定,6次测定溶液的平均钯含量为0.52 μg·L-1,RSD为6.77%,表明方法的重复性良好。
2.7 稳定性试验取同一份供试品溶液,于配制后室温放置0、1、2、4、6、8 h,分别测定吸光度,吸光度RSD为4.61%。结果表明供试品溶液室温放置8 h稳定性良好。
2.8 回收率试验取样品9份,各约0.2 g,精密称定,置烧杯中,分为3组,每组各3份,分别精密加入钯标准溶液(500 μg·L-1)1.0、1.5、2.0 mL,按供试品溶液的制备方法制备测试溶液,分别进样测定,采用工作曲线计算回收率。结果见表 2。
|
|
表 2 回收率试验测定结果(n=9) |
取3批氢溴酸沃替西汀样品(批号:20150501、20150502、20150503),每批各3份,按“2.2”节方法制备供试品溶液,测定吸光度,并带入工作曲线进行计算。得到3批氢溴酸沃替西汀原料药中钯含量分别为0.348、0.316、0.230 μg·g-1。
3 讨论与结论 3.1 灯电流的选择试验以钯灯为光源,波长为247.6 nm,通带为0.4 nm,石墨管类型为横向平台,保护气为氩气,以20 μg·L-1的钯溶液为标准溶液对灯电流进行了考察,具体考察结果见表 3。
|
|
表 3 灯电流与吸光度关系 |
从表 3发现,当灯电流为3 m A以上时,20 μg·L-1钯溶液的吸光度为0,而将灯电流降低至1 mA及2 mA时,钯溶液的吸光度较好。然而灯电流为1 mA时,吸光度基线的噪声较大,影响钯含量的检测限和定量限,所以选择灯电流的大小为2 mA。
3.2 原子化温度的选择分别考察了原子化温度为1700、1800、2200、2300 ℃条件下,20 μg·L-1钯溶液的吸光度,具体结果见表 4。
|
|
表 4 原子化温度与吸光度关系 |
如表 4所示,当原子化温度从1700 ℃逐渐升高时,吸光度值逐渐增大,当原子化温度为2200 ℃时,吸光度值达到最大,继续升高原子化温度,吸光度值没有相应的增加,因此,选择2200 ℃的原子化温度为最佳原子化吸收温度。
3.3 供试品溶液制备方法的比较制备法一:取本品0.2 g于聚四氟乙烯高压消化罐中,加入5 mL硝酸,加盖密封并将高压消化罐放入微波消解仪中,按设定的程序进行消解:120 ℃消解2 min, 150 ℃消解3 min,165 ℃消解3 min,180 ℃消解5 min。消解完毕后,在150 ℃的加热板上加热至溶液快干,然后加5%硝酸定容至50 mL,作为测试液。
制备法二:取本品0.2 g于聚四氟乙烯高压消化罐中,加入5 mL硝酸,2 mL双氧水,加盖密封并将高压消化罐放入微波消解仪中,按设定的程序进行消解:120 ℃消解2 min,150 ℃消解3 min,165 ℃消解3 min,180 ℃消解5 min。消解完成后,待温度降至60 ℃后,取出,将澄清溶液转移置量瓶中,用去离子水定容至50 mL,摇匀待测。
采用制备法一消解完毕后,溶液呈棕色,定容时有黄色固体析出,不适合作为待测液;采用制备法二消解完毕后,溶液呈棕色,定容时无黄色固体析出,定容后的溶液为淡黄色的澄清液,适合作为待测液。因此,选择制备法二制备供试品溶液;而且,回收率试验结果表明,此制备方法所制得样品的回收率良好。
制备法一与制备法二的主要区别:制备法二中除了加硝酸外,还加入了双氧水,双氧水在酸性条件下氧化性很强,能够更彻底地分解有机物,从而达到更好的消解效果。
理想消解方法的标志:1)避免待测组分遭受损失;2)消解后的溶液便于检测;3)安全快速;4)不得引进干扰物质[16]。本文选择的消解溶剂能很好地破坏有机物,所用的微波消解仪,设定了梯度加热的方法,使样品的消解能够完全、快速、有效地完成,因此是较为理想的消解方法。
3.4 钯残留的限度《中国药典》2015年版尚未对钯残留进行单一限定,只是对总重金属进行了限定:不超过百万分之二十(20 µg·g-1)。ICH Q3D元素杂质指南规定,口服制剂中钯元素的PDE标准(每日允许暴露量)为100 μg·d-1。氢溴酸沃替西汀作为口服制剂,推荐开始剂量为10 mg • d-1,耐受剂量为20 mg·d-1,因此,氢溴酸沃替西汀的钯含量限度为100 μg/20 mg = 5000 µg·g-1。本试验3批氢溴酸沃替西汀原料药中的钯含量分别为0.348、0.316、0.230 µg • g-1,远低于这个限度。
| [1] |
Bidzan L, Mahableshwarkar AR, Jacobsen P, et al. Vortioxetine (Lu AA21004) in Generalized Anxiety Disorder:Results of An 8-week, Multinational, Randomized, Double-blind, Placebo-controlled Clinical Trial[J]. European Neuropsychopharmacology, 2012, 22(12): 847-857. DOI:10.1016/j.euroneuro.2012.07.012 |
| [2] |
Mahableshwarkar AR, Jacobsen PL, Chen Y, et al. A Randomised, Double-blind, Placebo-controlled, Duloxetine-referenced Study of the Efficacy and Tolerability of Vortioxetine in the Acute Treatment of Adults with Generalised Anxiety Disorder[J]. The International Journal of Clinical Practice, 2014, 68(1): 49-59. DOI:10.1111/ijcp.12328 |
| [3] |
Zhang GR, Ma Q, Zhang L, et al. Determination of Palladium in 32 Phenylpropenoate by Graphite Furnace Atomic Absorption Spectrometry[J]. Chin J Anal Lab, 2007, 26(3): 43-46. |
| [4] |
张振兴, 王强, 杨凤, 等. 微波消解-ICP-MS法测定利奈唑胺中残留钯[J]. 化学研究与应用, 2013, 25(1): 134-136. |
| [5] |
Qian CY. Environment PGE Determination of Palladium[D]. Beijing:Capital Normal University, 2003.
|
| [6] |
Luo WZ, Chen LZ, Jin LY. Neutron Activation Analysis of the Progress of Our Country[J]. Chin J Anal Chem, 1979, 7(5): 400-406. |
| [7] |
曾佐涛, 王双印. 新显色剂5-APAQ分光光度法直接测定药品中的残留钯[J]. 中国药学杂志, 1997, 32(10): 611-613. DOI:10.3321/j.issn:1001-2494.1997.10.012 |
| [8] |
Zhang GZ, Shi HM. Study on Ion-exchange Resin Colorimetry of Palladium[J]. Ion Exch Adsorp, 1900, 6(3): 189-194. |
| [9] |
陈阳, 彭茗, 杨永健. 石墨炉原子吸收光谱法测定棕榈酸中镍残留量[J]. 中国药房, 2012, 26(5): 393-395. |
| [10] |
李浩, 朱斌, 黄宝贵. 石墨炉原子吸收光谱法测定枸橼酸中的铝[J]. 药物分析杂志, 2010, 30(3): 530-533. |
| [11] |
程小宁, 余敏灵, 黄琳. 石墨炉原子吸收分光光度法测定维生素C原料中微量铅、镉含量[J]. 中国药业, 2012, 21(3): 12-14. |
| [12] |
郭旭光, 郑子栋, 郭毅. 阿加曲班原料药中催化剂钯残留监测方法建立[J]. 中国药事, 2014, 28(9): 1018-1020. |
| [13] |
齐鹏成, 付炎, 周娜, 等. 硫酸特布他林原料药中催化剂钯残留监测方法建立[J]. 中国药事, 2016, 30(3): 281-284. |
| [14] |
袁利月, 杨荷友, 许玉丽. 石墨炉原子吸收光谱法测定泛昔洛韦中的痕量钯[J]. 中国医药工业杂志, 2006, 37(8): 555-556. |
| [15] |
王湘波, 马晓宁, 范亚, 等. 石墨炉原子吸收光谱法测定替加环素中钯的残留量[J]. 中南药学, 2015, 13(9): 977-979. DOI:10.7539/j.issn.1672-2981.2015.09.021 |
| [16] |
朱先磊, 董德明, 刘淼, 等. 大豆样品干法与湿法消解的比较[J]. 吉林大学自然科学学报, 1996, 5(2): 104-106. |
 2017, Vol. 31
2017, Vol. 31 
