乙型肝炎病毒(hepatitis B virus, HBV)感染是全球公共的卫生问题,全球每年约有100万的乙型肝炎患者死于肝病末期的并发症,包括肝硬化、肝细胞癌和肝衰竭。我国亦是HBV感染的高发区,乙肝表面抗原携带率约为7.18%。前列地尔(alprostadil),又称前列腺素E1,是一种广泛存在于体内的生物活性物质,其治疗肝炎的具体机制:1)促进胰高血糖素的释放及其对肝内胆管的局部刺激,使胆汁分泌增加,加速肝内毒性物质的排泄,保护肝脏;2)通过舒张血管、抗凝血、调节前列环素与血栓素A2平衡,起到改善肝微循环作用;3)稳定肝细胞膜,促进肝细胞再生;4)具有免疫调节作用,抑制和消除免疫复合物,减轻肝炎病毒感染后激发的免疫损伤[1-2]。临床上开始在综合治疗的基础上加用前列地尔治疗乙型肝炎,但目前尚无确切的循证学依据,不能对前列地尔的临床应用做出明确指导;鉴于此,本文对国内外发表的前列地尔治疗乙型肝炎的17篇文献进行Meta分析,以了解前列地尔治疗乙型肝炎的临床价值,客观评价其安全性和有效性。
1 材料与方法 1.1 资料来源以所有已发表的前列地尔治疗乙型肝炎的随机对照试验或半随机对照试验为研究对象。文献来源包括:以“alprostadil or prostaglandin(MeSH Major Topic) AND hepatitis(MeSH Major Topic)”为检索式,检索Pubmed数据库、EMBASE数据库、Cochrane数据库;以“题名或关键词=前列地尔或前列腺素E1或凯时与题名或关键词=肝炎”为检索式,检索万方、维普、CNKI。检索时间区间均设定为从建库时间起至2014年4月。
1.2 试验纳入标准 1.2.1 设计类型国内外已经发表的前列地尔治疗乙型肝炎的随机对照试验或半随机对照试验,不限制语种及疗程。
1.2.2 研究对象按照1995年或2000年中华医学会传染病与寄生虫病学分会、肝病学分会联合修订的病毒性肝炎防治方案诊断标准[3]。具有明确诊断的乙型肝炎患者,年龄、性别、种族、教育程度等不限。
1.2.3 干预措施试验组采用前列地尔,对照组采用安慰剂或空白治疗;基础治疗和其他干预措施在两组间必须相同,综合治疗加用前列地尔与未使用前列地尔对照。综合治疗方案包括抗病毒、保肝退黄、营养支持等治疗。
1.2.4 疗效观察指标临床总有效率:对乙型肝炎的治疗,目前尚没有统一的疗效评估标准,因此,判断有效和无效的标准由纳入文献作者自定义。肝功能检查:谷丙转氨酶(ALT)和总胆红素(TBil)。凝血功能检查:凝血酶原活动度(PTA)。不良反应:与前列地尔有关的不良反应。
1.3 试验排除标准1)研究试验为非临床试验,研究设计为非随机或半随机临床对照试验及无对照的临床试验。2)研究对象为乙型肝炎合并其他病毒如巨细胞病毒、EB病毒、HCV、HDV、HIV重叠感染,原发性肝癌或肝移植患者,自身免疫性肝病、酒精性肝炎、药物性肝炎者。3)治疗组和对照组中的辅助干预措施不完全相同或对照组中的干预措施含有前列地尔或其衍生物。4)排除重复发表的文献。
1.4 文献质量评价和资料提取采用牛津评分系统(Jadad量表)对纳入文献进行质量评价,其内容包括随机序列的产生、分配隐藏、盲法的使用、对退出及失访人数及原因的描述,总分为7分,≥4分被认为是高质量研究。资料提取包括:纳入研究一般信息,样本量,干预特征(措施、剂量、疗程),患者的一般信息(种族、平均年龄、ALT和TBil水平、血清抗原及病毒载量),不良反应描述及试验结果。
1.5 统计学处理[4]采用Cochrane协作网提供的RevMan 5.0软件和Stata 12.0软件进行分析。分别进行异质性检验、亚组分析、敏感性分析及偏倚分析。
2 结果 2.1 检索结果最初共检索出187篇文献(其中中文文献178篇、外文文献9篇),采用Endnote X7对检索文献进行管理,通过阅读标题、摘要和全文浏览后,纳入52篇合格的随机对照试验,其中26篇因研究疾病非乙型肝炎而排除,6篇因干预措施与纳入标准不符而排除,2篇为重复研究而排除,1篇因结局指标与纳入标准不符而排除。最后,纳入17篇文献,总共包括1535例患者。文献基本情况见表 1。
|
|
表 1 文献基本情况 |
纳入的17篇文献总体上干预措施平行,17篇文献均提及综合治疗为保肝退黄、营养支持治疗,只有1篇文献在此基础上进行抗病毒治疗;对其进行Jadad评分,17组试验均未提及盲法;对于分配隐藏的方法均未有描述;1组试验采用随机数字表法进行随机分组,1组采用按住院时间随机分组,其余均未描述随机分组;1组试验对脱落及失访进行描述,其余试验均未描述。质量评价结果表明纳入文献质量不高,会在一定程度上影响本研究的证据强度。
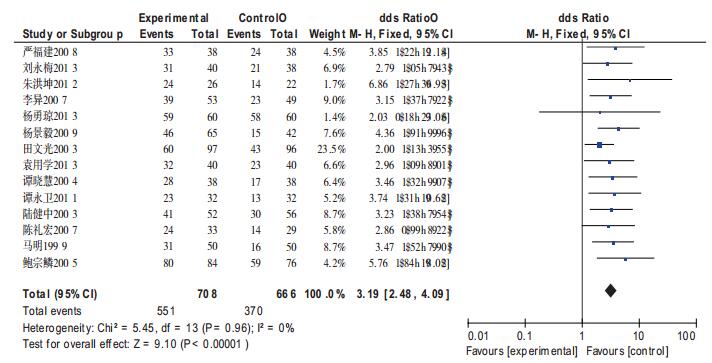
2.2 疗效分析 2.2.1 临床总有效率17组试验中有14组提及临床总有效率,共1374例患者被纳入。16组试验将有效标准定义为临床症状、体征明显改善或消失,肝功能(ALT、AST、TBil)和PTA较治疗前改善50%以上;1组试验没有说明其判定标准。但14组试验的效应量无统计学异质性(χ2=5.45,df=13,P=0.96,I2=0%),故选用固定效应模型进行分析。结果显示,前列地尔治疗乙型肝炎的有效率为77.82%,对照组治疗乙型肝炎的有效率为55.55%,其差异有统计学意义[OR=3.19,95% CI(2.48,4.09),Z=9.10,P<0.00001]。结果见图 1。
|
图 1 试验组与对照组关于临床总有效率的meta分析 |
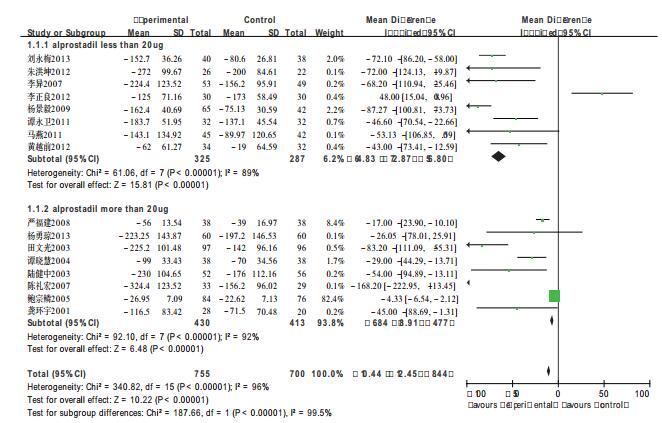
17组试验均提及了总胆红素的改善情况,共纳入1455例患者,各试验组间存在统计学异质性(χ2=340.82,df=15,P<0.00001,I2=96%),故选用随机效应模型进行分析。由于各试验组间异质性较大,根据使用前列地尔剂量的不同进行亚组分析。合并结果提示产生异质性的来源与前列地尔的应用剂量无关,前列地尔对降低乙型肝炎患者总胆红素有统计学差异。结果见图 2。
|
图 2 试验组与对照组关于总胆红素改善情况的meta分析 |
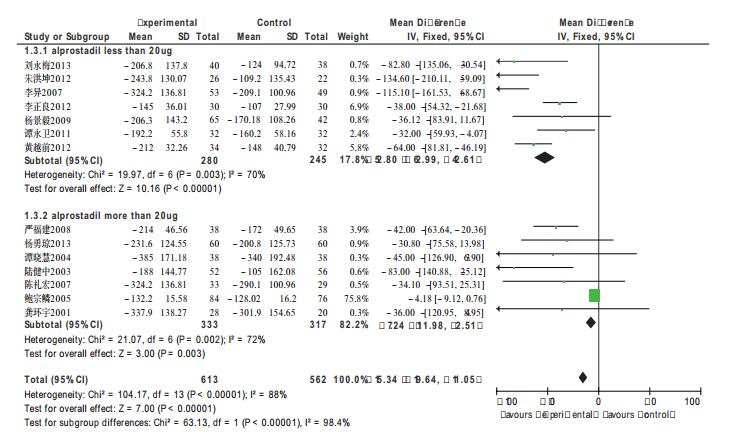
17组试验均提及了谷丙转氨酶的改善情况,共纳入1157例患者,各试验组之间存在统计学异质性(χ2=86.96,df=13,P<0.00001,I2=85%),故选用随机效应模型进行分析。由于各试验组间异质性较大,根据使用前列地尔剂量的不同进行亚组分析。合并结果提示产生异质性的来源与前列地尔的应用剂量有关,前列地尔对降低乙型肝炎患者谷丙转氨酶有统计学差异。结果见图 3。
|
图 3 试验组与对照组关于谷丙转氨酶改善情况的meta分析 |
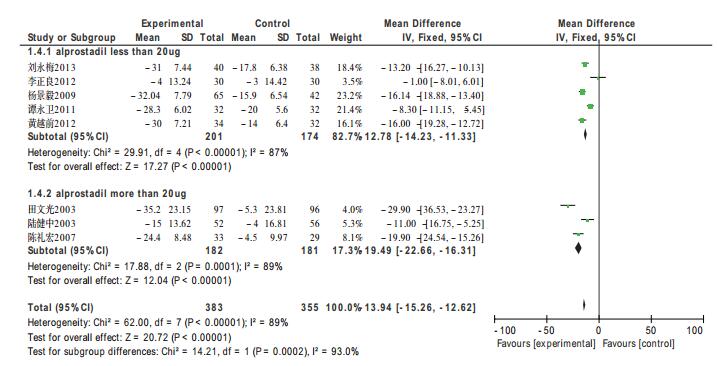
17组试验中有8组试验提及了凝血酶原活度的改善情况,共纳入1455例患者,各试验组之间存在统计学异质性(χ2=62.00,df=7,P<0.00001,I2=89%),故选用随机效应模型进行分析。由于各试验组间异质性较大,根据使用前列地尔剂量不同进行亚组分析。合并结果提示产生异质性的来源与前列地尔的应用剂量无关,前列地尔对降低乙型肝炎患者凝血酶原活度有统计学差异。结果见图 4。
|
图 4 试验组与对照组关于凝血酶原活度改善的meta分析 |
分别对所有结局指标的Meta分析结果及其亚组分析结果进行敏感性分析,同时,均采用随机效用模型和固定效应模型进行分析。结果显示:总胆红素、谷丙转氨酶、凝血酶原活度改善情况及临床总有效率的Meta分析结果及其亚组分析结果均未被逆转,表明研究结果比较稳健。
2.4 偏倚分析通过stata 12.0软件对结果进行偏倚分析,结果显示:临床总有效率Begg法:z = 0. 7 9,Pr>z = 0.428>0.05;Eegg法:t=2.09,P>|t |=0.06>0.05,95%CI[-0.61,2.41]包含0,可认为无发表偏倚;总胆红素(TBil)Begg法:z=1.40,Pr>z=0.163>0.05,Eegg法:t=2.09,P>|t|=0.06>0.05,95%CI[-0.61,2.41]包含0,可认为无发表偏倚;z=0.163>0.05,Eegg:t=1.15,P>|t|=0.271>0.05,95%CI[-3.20,10.54]包含0,可认为无发表偏倚;谷丙转氨酶(ALT)Begg法:z = 3.07,Pr>z = 0.002<0.05;Eegg法:t=-2.90,P>|t|=0.013<0.05,95%CI[-9.74,-1.39]不包含0,可认为有发表偏倚;凝血酶原活度(PTA)Begg法:z = 0.87,Pr>z = 0.386>0.05;Eegg法:t=1.17,P>|t|=0.285>0.05,95%CI[-5.56,15.82]包含0,可认为无发表偏倚。
2.5 不良反应17组试验(共1535例患者)中,有4组试验(共280例患者)没有报道发生不良反应,2组试验(共377例患者)明确说明没有不良反应的发生。前列地尔临床上常见的不良反应有注射部位血管疼痛、静脉炎、面色潮红、头晕心悸、皮肤瘙痒等;在其余11组试验中22例患者出现注射部位血管痛、15例患者出现头晕头痛,因患者对以上不良反应耐受性良好,减慢给药速度后症状消失,亦没有患者终止试验。
3 讨论 3.1 前列地尔治疗乙型肝炎的文献特点前列地尔治疗肝炎在临床应用近30年[22],本次研究的目的是进一步探讨前列地尔对乙型肝炎的疗效,所纳入的文献均为中文文献。从文献质量评价结果来看,目前前列地尔治疗乙型肝炎的相关文献属低质量文献,存在一些质量缺陷,包括:1)大多数试验未提及是否采用盲法,可能会使统计效能下降,结果受人为因素影响较大。2)大多数文献未对脱落及失访人数及原因进行描述,可能导致失访偏倚的产生。3)大多数试验没有描述具体的随机方法,只简单提及为随机试验,从而无法判断试验是否正常进行、分配方案隐藏是否完善。而分配方案隐藏不完善会在一定程度上夸大试验结果。4)文献对于计量资料的处理尚不完善,文献只给出了两组试验治疗前后的平均值及标准差,未给出治疗前后指标变化的平均值及标准差,只能通过公式计算,此过程中会使计算误差增大。5)文献对于综合治疗的介绍比较粗略,仅描述为进行抗病毒、保肝退黄、营养支持等治疗,未提及具体应用的药物品种,可能导致研究基线不稳定,降低研究结果的可靠性。
3.2 前列地尔治疗乙型肝炎Meta分析结果的意义及评价对本次研究结果进行分析,计量资料结局指标异质性较大(TBil:96%,ALT:85%,PTA:89%),而计数资料异质性相对较小(临床总有效率:0%)。对计量资料以使用前列地尔不同剂量为亚组进行分析,各亚组间ALT异质性有所下降[(PEG E1<20μg):54%, ALT(PEG E1≥20μg):72%],表明异质性的产生与前列地尔的剂量有关;而TBil和PTA的异质性未有下降。亚组分析结果提示前列地尔可以降低患者的TBil、ALT、PTA指标。各结局指标的Meta分析结果在敏感性分析中没有发生逆转,提示结果稳健性较高。通过Stata 12.0软件分析纳入文献的发表偏倚,结果提示除谷丙转氨酶(ALT)外,其余各项结局指标发表偏倚较小,可能与各研究机构生化检验试剂盒规格、仪器参数、实验人员操作等因素有关,结合敏感性分析结果,本研究结果相对可靠。
综上所述,本次系统评价结果显示,在综合治疗基础上加用前列地尔治疗乙型肝炎是安全、有效的;前列地尔可以明显改善患者的临床症状、体征及肝功能指标,并且不良反应发生率低,可以在临床上进行推广。笔者建议,为进一步评价前列地尔对乙型肝炎的疗效,应进一步完善实验设计,通过多中心、大样本、随机双盲的临床试验,以获得更加准确的临床数据,并且增加病理学指标更加准确地评估和考核前列地尔临床应用的安全性和有效性[23]。
| [1] |
Quintero A, Pedraza CA, Siendones E, et al. PEG1 Protection Against Apoptosis Induced by D-galaetOsamine Is Not Related to the Modulation of Intracellular Free Radical Production in Primary Culture of Rat Hepatocytes[J]. Free Radic Ras, 2002, 36(3): 345-355. DOI:10.1080/10715760290019372 |
| [2] |
Reus S, Priego M, Boix V, et al. Can Alprostadil Improve Liver Failure in HIV-induced Patients with Acute Viral Hepatitis[J]. J Infect, 1998, 37(1): 84-86. DOI:10.1016/S0163-4453(98)91163-X |
| [3] |
中华医学会. 病毒性肝炎防治方案[J]. 中华肝病杂志, 2005, 8(5): 329-342. |
| [4] |
周旭毓, 方积乾, 宇传华, 等. 现代医学统计学[M]. 北京: 人民卫生出版社, 2002: 150-158.
|
| [5] |
田文广, 何平. 前列腺素E1治疗193例重型病毒性肝炎[J]. 现代医药卫生, 2003, 19(10): 1242-1244. DOI:10.3969/j.issn.1009-5519.2003.10.010 |
| [6] |
龚环宇, 万克清. 前列腺素E1对慢性乙型肝炎肝功能和肝纤维化指标的影响[J]. 湖南医科大学学报, 2001, 26(5): 445-446. |
| [7] |
陆健中. 凯时治疗慢性重型肝炎52例临床观察[J]. 徐州医学院学报, 2003, 23(4): 340-342. |
| [8] |
刘永梅. 慢性重型肝炎临床治疗效果观察[J]. 中国农村卫生, 2013(08): 117-119. |
| [9] |
袁用学. 前列地尔对乙型重型肝炎疗效观察[J]. 中国实用医药, 2013, 8(17): 143-145. DOI:10.3969/j.issn.1673-7555.2013.17.106 |
| [10] |
谭晓慧, 蒋道荣, 徐芳芹, 等. 前列地尔对重度乙型肝炎疗效观察[J]. 中国交通医学杂志, 2004, 18(3): 263-264. |
| [11] |
姬长县, 鲍宗鳞. 前列地尔联合甘利欣治疗慢性乙型肝炎84例[J]. 中西医结合肝病杂志, 2005, 15(1): 54-55. |
| [12] |
李异, 蒋永芳. 前列地尔脂微球载体制剂注射液配合血浆置换治疗重型肝炎临床研究[J]. 中国新药杂志, 2007, 16(8): 641-642. |
| [13] |
严福建, 陈士淼. 前列地尔治疗慢性乙型病毒性肝炎近期疗效观察[J]. 浙江临床医学, 2008, 10(1): 4-6. |
| [14] |
黄越前, 符业阳. 前列地尔治疗慢性乙型肝炎肝硬化的疗效观察[J]. 临床与实践, 2012, 9(22): 27-28. |
| [15] |
朱洪坤. 前列地尔治疗慢性乙型淤胆型肝炎的临床观察[J]. 肝脏, 2013, 18(8): 587-588. |
| [16] |
杨景毅, 倪辉, 冼永超, 等. 前列地尔治疗慢性重型肝炎65例临床疗效观察[J]. 中国现代药物应用, 2009, 3(16): 101-102. DOI:10.3969/j.issn.1673-9523.2009.16.077 |
| [17] |
马燕. 前列地尔注射液对治疗慢性乙型淤胆型肝炎疗效观察[J]. 中国美容医学, 2001, 20(1): 358-35. |
| [18] |
邹敏, 杨永琼, 徐辉, 等. 前列地尔注射液辅助治疗慢性乙型重度肝炎的疗效观察[J]. 当代医学, 2013, 19(8): 143-144. |
| [19] |
陈礼宏, 李德辉, 杨春芳. 前列地尔注射液联合血浆置换治疗重型肝炎33例[J]. 世界华人消化杂志, 2007, 15(36): 3864-3865. DOI:10.3969/j.issn.1009-3079.2007.36.018 |
| [20] |
李正良. 前列地尔注射液治疗重型病毒性肝炎30例临床观察[J]. 临床医学, 2012, 32(4): 43-45. |
| [21] |
谭永卫, 蒋芳清. 前列地尔注射液治疗重型肝炎32例临床疗效观察[J]. 中国医师杂志, 2011, 13(1): 133-134. |
| [22] |
Flisiak R, Prokopowicz R. Effect of Misoprostol on the Course of Viral Hepatitis B[J]. Hepatogastroenterology, 1997, 44(17): 1419-1420. |
| [23] |
罗瑞虹, 姚集鲁, 赵志新, 等. 前列腺素E治疗病毒性肝炎的中文文献评价[J]. 中华肝脏病杂志, 2014, 12(2): 116-117. |
 2017, Vol. 31
2017, Vol. 31 
